网址:http://m.1010jiajiao.com/timu_id_262909[举报]
一、选择题(每小题3分,共51分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
答案
A
C
C
C
C
C
B
D
A
B
B
D
B
C
A
C
D
二、填空题(21题(1)问每空1分,其余每空2分,共19分)
18.(10分)(1)① (2)①⑤ (3)4 (4)>7 (5)D
19.(8分)(1)

(2)
(3)
 20.(9分)(1)
20.(9分)(1)

 (各1分)
(各1分)
(2)
(3) (4)
(4)

21.(14分)(1)试管上部充满红棕色气体
(2)无; 与水反应生成了足量的
与水反应生成了足量的 ,中和了
,中和了
(3)
 只写第一个给全分
只写第一个给全分
(4) ;
; ;小
;小
22.(8分)(1)
(2)A、D
(3)3 

(4分)下列反应在210℃时达到平衡:
①PCl5(g) PCl3(g)+Cl2(g);
△H1>0 K1=10
PCl3(g)+Cl2(g);
△H1>0 K1=10
②CO(g)+Cl2(g) COCl2(g);△H1<0 K2= 5×103
COCl2(g);△H1<0 K2= 5×103
③PCl5(g) +CO(g) COCl2(g) + PCl3(g)
K3
COCl2(g) + PCl3(g)
K3
(1)反应③的平衡常数K3 = 。
(2)要使反应①和反应②的K数值相等,可采取的措施是 (填序号)。
A.降低反应①、②体系中Cl2浓度 B.反应①、②选择不同的催化剂
C.反应①、反应②同时升高温度 D.降低反应①、反应②的体系压强
E.反应①降低温度,反应②维持210℃
【解析】当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值称作平衡常数。①+②即得到③,所以③的平衡常数为10×5×103= 5×104.。反应①是吸热反应,②是放热反应,所以要使反应①和反应②的K数值相等,则反应①要向正反应方向移动,反应②要向逆反应方向移动,所以答案是C。
查看习题详情和答案>>
(4分)下列反应在210℃时达到平衡:
①PCl5(g)PCl3(g)+Cl2(g);△H1>0 K1=10
②CO(g)+Cl2(g)COCl2(g);△H1<0 K2= 5×103
③PCl5(g) +CO(g) COCl2(g) + PCl3(g) K3
(1)反应③的平衡常数K3= 。
(2)要使反应①和反应②的K数值相等,可采取的措施是 (填序号)。
A.降低反应①、②体系中Cl2浓度 B.反应①、②选择不同的催化剂
C.反应①、反应②同时升高温度 D.降低反应①、反应②的体系压强
E.反应①降低温度,反应②维持210℃
【解析】当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值称作平衡常数。①+②即得到③,所以③的平衡常数为10×5×103= 5×104.。反应①是吸热反应,②是放热反应,所以要使反应①和反应②的K数值相等,则反应①要向正反应方向移动,反应②要向逆反应方向移动,所以答案是C。
查看习题详情和答案>>
 催化剂中毒是微量杂质和催化剂活性中心的某种化学成分作用,形成没有活性的物质.CO会使合成氨的催化剂(还原铁)中毒,CO易与Fe发生反应Fe+5CO═Fe(CO)5.除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3═Cu(NH3)3(CO)Ac.
催化剂中毒是微量杂质和催化剂活性中心的某种化学成分作用,形成没有活性的物质.CO会使合成氨的催化剂(还原铁)中毒,CO易与Fe发生反应Fe+5CO═Fe(CO)5.除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3═Cu(NH3)3(CO)Ac.请回答下列问题:
(1)C、N、O的第一电离能由小到大的顺序为
(2)写出基态Fe的核外电子排布式
(3)配合物Cu(NH3)3(CO)Ac中含有的化学键是
A.金属键 B.离子键 C.非极性键 D.配位键 E.氢键 F.极性键
(4)等电子体指价电子数和原子数(氢等轻原子不计在内)相同的分子、离子或基团.写出与CO互为等电子体的离子
(5)在一定条件下NH3与CO能合成化肥尿素[CO(NH2)2],尿素中C原子轨道的杂化类型为
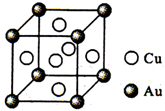
(6)铜金合金形成的晶胞如图所示.其中Cu、Au原子个数比为
请回答下列问题:
(1)C、N、O的第一电离能由小到大的顺序为______.
(2)写出基态Fe的核外电子排布式______.
(3)配合物Cu(NH3)3(CO)Ac中含有的化学键是______.
A.金属键 B.离子键 C.非极性键 D.配位键 E.氢键 F.极性键
(4)等电子体指价电子数和原子数(氢等轻原子不计在内)相同的分子、离子或基团.写出与CO互为等电子体的离子______(任写一个).
(5)在一定条件下NH3与CO能合成化肥尿素[CO(NH2)2],尿素中C原子轨道的杂化类型为______.
(6)铜金合金形成的晶胞如图所示.其中Cu、Au原子个数比为______,预测其熔点比铜的______(填“高”“相等”或“低”).
 查看习题详情和答案>>
查看习题详情和答案>>
A.滴定用的锥形瓶和滴定管都要用所盛溶液润洗
B.在粗盐的提纯实验中,溶解、过滤、蒸发都用到了玻璃棒
C.配制一定浓度的溶液时,俯视容量瓶的刻度线,会使配制的浓度偏高
D.配制FeCl3溶液时,将FeCl3固体溶于较浓盐酸中,然后再用水稀释到所需的浓度E.在铁粉存在下用溴水和苯反应制取溴苯时,无需加热
F.取1mL 20%蔗糖溶液,加入适量稀硫酸,水浴加热约5min后,再加入少量新制的Cu(OH)2,悬浊液加热,可检验蔗糖是否发生了水解
G.物质溶于水的过程中,一般有放热或吸热现象,若热效应不明显,溶解的操作可以在量筒中进行
Ⅱ在中学化学实验中,通常用无水硫酸铜来检验少量水的存在,然而,无水硫酸铜的吸湿性很强,需要时须现制现用.
方法Ⅰ:取2药匙细小的硫酸铜晶体置于
方法Ⅱ:取2药匙研碎的硫酸铜晶体于小烧杯中,加入20mL浓硫酸(质量分数不低于98%),并用玻璃棒搅拌,静置5min后倾去浓硫酸,用无水乙醇洗涤数次,倒在滤纸上晾干.
【交流与讨论】
(1)方法Ⅰ中,加热温度稍高时会出现变黑现象,原因是
| ||
| ||
| ||
| ||
(2)方法Ⅱ中,浓硫酸的作用是
(3)用制得的无水硫酸铜检验某双氧水中是否含水时,除了发现固体变蓝外,还发现该双氧水中有气泡产生,对此你有何猜想