摘要:主要考点:1. 常识:核外电子排布.原子结构示意图.原子团的概念 ① 核外电子的分层排布.能量低的靠近原子核,第一层(K层)最多排2个电子.第二层(L层)最多排8个电子.最外层最多排8个电子,先排满内层.在排外层, 原子团在化学变化中.有可能改变 ② 硝酸根离子NO3-,氯酸根离子ClO3-,氢氧根离子OH-,碳酸氢根离子HCO3-,碳酸根离子CO32-,硫酸根离子SO42-,锰酸根离子MnO42-,高锰酸根离子MnO4-,磷酸根离子PO43-,铵根离子NH4+ ③ 注意原子结构示意图与离子结构示意图之间的区别:判断元素种类.根据核内质子数,判断是离子还是原子.根据核外电子总数与核内质子数 ④ 地壳中含量前四位:氧,空气中含量最多的元素:氮(N),海洋中含量最多的元素:氧(O) ⑤ 原子的最外层的电子数决定了:元素的化学性质.元素的分类.元素的化合价
网址:http://m.1010jiajiao.com/timu_id_2519085[举报]
20、钠元素与氯元素在元素周期表中位于同一周期,图㈠是钠原子的结构示意图,图㈡是氯离子的结构示意图,图㈢是钠与氯气反应的模拟微观示意图.

(1)图㈠中X为
(2)与氯离子具有相同核外电子排布的原子符号为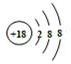 .
.
(3)由图㈢可知,钠原子在化学反应中易
查看习题详情和答案>>

(1)图㈠中X为
11
,图㈡中Y为
8
.(2)与氯离子具有相同核外电子排布的原子符号为
Ar
,原子结构示意图为

(3)由图㈢可知,钠原子在化学反应中易
失
电子(填“得”或“失”),说明元素的性质与
最外层电子
有密切的关系.如图是元素周期表中1-18号元素的原子结构示意图,观察图,探究下列问题:

(1)核外电子是
(2)周期数═
②
(3)族数═
(4)填充下表:
(5)最外层为
结论:元素的化学性质与
查看习题详情和答案>>

(1)核外电子是
分层
分层
排布的.第一层电子数不超过2
2
个;第二层电子数不超过8
8
个;最外层电子数不超过8
8
个.(2)周期数═
原子的电子层数
原子的电子层数
.同一周期的元素,①原子的电子层数
原子的电子层数
相同;②
从左到右原子的最外层电子数
从左到右原子的最外层电子数
逐渐递增;③每周期开头的是金属
金属
类型的元素,靠近尾部的是非金属
非金属
类型的元素,结尾的是稀有气体
稀有气体
类型的元素.(3)族数═
原子的最外层电子数
原子的最外层电子数
.同族元素,①原子的最外层电子数
原子的最外层电子数
相同;②元素的化学性质
元素的化学性质
相似;③从上到下原子的电子层数
从上到下原子的电子层数
逐渐递增.(4)填充下表:
| 元素种类 | 举 例 | 原子的最外层电子数 | 得失电子的趋势 | 元素的化学性质 |
| ①金属元素 | Na、Mg、Al | 一般少于4个 一般少于4个 |
失电子 失电子 |
不稳定 不稳定 |
| ②非金属元素 | O、Cl、S、P | 一般多于或等于4个 一般多于或等于4个 |
得电子 得电子 |
不稳定 不稳定 |
| ③稀有气体元素 | He、Ne、Ar | 8个电子(He为2个) 8个电子(He为2个) |
一般不得失电子 一般不得失电子 |
比较稳定 比较稳定 |
8
8
个电子(只有1个电子层时2
2
个)的结构称为稳定结构.在化学反应中,元素的原子通过得或失电子形成相对稳定结构.结论:元素的化学性质与
其原子的核外电子排布
其原子的核外电子排布
,特别是最外层电子的数目
最外层电子的数目
有密切的关系.即原子的最外层电子数
原子的最外层电子数
决定元素的化学性质.
钠元素与氯元素在元素周期表中位于同一周期,图㈠是钠原子的结构示意图,图㈡是氯离子的结构示意图,图㈢是钠与氯气反应的模拟微观示意图.

(1)图㈠中X为,图㈡中Y为.
(2)与氯离子具有相同核外电子排布的原子符号为,原子结构示意图为.
(3)由图㈢可知,钠原子在化学反应中易电子(填“得”或“失”),说明元素的性质与有密切的关系. 查看习题详情和答案>>

(1)图㈠中X为,图㈡中Y为.
(2)与氯离子具有相同核外电子排布的原子符号为,原子结构示意图为.
(3)由图㈢可知,钠原子在化学反应中易电子(填“得”或“失”),说明元素的性质与有密切的关系. 查看习题详情和答案>>

