题目内容
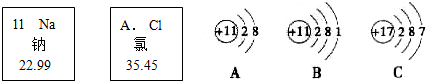
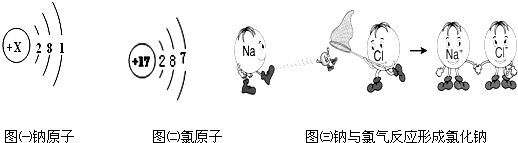
20、钠元素与氯元素在元素周期表中位于同一周期,图㈠是钠原子的结构示意图,图㈡是氯离子的结构示意图,图㈢是钠与氯气反应的模拟微观示意图.

(1)图㈠中X为
(2)与氯离子具有相同核外电子排布的原子符号为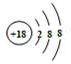 .
.
(3)由图㈢可知,钠原子在化学反应中易

(1)图㈠中X为
11
,图㈡中Y为
8
.(2)与氯离子具有相同核外电子排布的原子符号为
Ar
,原子结构示意图为

(3)由图㈢可知,钠原子在化学反应中易
失
电子(填“得”或“失”),说明元素的性质与
最外层电子
有密切的关系.分析:(1)钠原子中,质子数等于核外电子数;氯离子最外层达8电子稳定结构;
(2)氯离子核外18个电子分三层排布,氩原子核外18个电子也分三层排布;氩原子有18个质子,核外电子以2、8、8的形式分布在三个电子层上;
(3)图三表示钠原子失去一个电子变成稳定的钠离子,元素的性质与最外层电子关系密切.
(2)氯离子核外18个电子分三层排布,氩原子核外18个电子也分三层排布;氩原子有18个质子,核外电子以2、8、8的形式分布在三个电子层上;
(3)图三表示钠原子失去一个电子变成稳定的钠离子,元素的性质与最外层电子关系密切.
解答:解:(1)原子结构示意图中,质子数等于核外电子数,因此,X=2+8+1=11;氯离子具有稳定结构,即最外层有8个电子,因此,最外层上的电子数Y=8;
故答案为:11;8;
(2)氯离子核外有18个电子分三层排布,其排布方式为2、8、8结构;与氯离子具有相同的电子排布的原子核外也应为18个电子,则该原子质子数也为18,质子数为18的是氩元素,符号为Ar;
故答案为:Ar;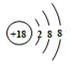 ;
;
(3)钠原子最外层有1个电子,易失去电外层电子而使次外层变成最外层,达到8电子稳定结构;由此可见,元素的性质特别是化学性质主要取决于最外层电子数;
故答案为:失;电外层电子.
故答案为:11;8;
(2)氯离子核外有18个电子分三层排布,其排布方式为2、8、8结构;与氯离子具有相同的电子排布的原子核外也应为18个电子,则该原子质子数也为18,质子数为18的是氩元素,符号为Ar;
故答案为:Ar;
 ;
;(3)钠原子最外层有1个电子,易失去电外层电子而使次外层变成最外层,达到8电子稳定结构;由此可见,元素的性质特别是化学性质主要取决于最外层电子数;
故答案为:失;电外层电子.
点评:最外层电子为8,为稳定结构,既不易得也不易失电子;最外层电子小于4,易失去电外层电子而使次外层为最外层,达到稳定结构;最外层电子大于4,易得电子而使最外层电子达8电子稳定结构.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目