网址:http://m.1010jiajiao.com/timu_id_244971[举报]
13.D 14.AC 15. C 16.C 17.D 18.D
.files/image107.jpg)
19、
Ⅱ、(10分)(1)②.files/image109.gif) (2分)③
(2分)③.files/image111.gif) (2分)④斜面倾角(或填h的数值)(3分)
(2分)④斜面倾角(或填h的数值)(3分)
(2) 不能(3分)
20.(15分)解:(1)设绳断后小球以速度v1平抛
竖直方向上:2R=.files/image113.gif) g t2
(3分)
g t2
(3分)
水平方向上:4R=v1t (3分)
解得v1=2.files/image115.gif) (1分)
(1分)
(2)小球从最低点到最高点过程,小球机械能守恒(选地面为零势能面)
.files/image117.gif) (3分)
(3分)
合力提供向心力有:F-mg = m.files/image119.gif) (3分)
(3分)
解得F=9mg (2分)
21(1)由前三列数据可知物体在斜面上匀加速下滑时的加速度为a1==
(2)由后二列数据可知物体在水平面上匀减速滑行时的加速度大小为a2==
(3)由2+5t=1.1+2(0.8-t),解得t=0.1s,即物体在斜面上下滑的时间为0.5s。
22.(1)洛仑兹力不做功,由动能定理得,mgy=.files/image121.gif) mv2
mv2.files/image123.gif) ……①
……①
得 v=.files/image125.gif)
.files/image123.gif) ……②
……②
(2)设在最大距离ym处的速率为vm,根据圆周运动有,qvmB-mg=m.files/image127.gif) ……③
……③
且由②知 .files/image123.gif)
.files/image130.gif) ……④
……④
由③④及R=2ym得 .files/image132.gif) ……⑤
……⑤
(3)小球运动如图所示,当它运动到最高点时速度最大,设为vm,此时小球在最高点的曲率半径也为该点到x轴距离的2倍,
.files/image133.gif) 由动能定理 (qE-mg)|ym|=
由动能定理 (qE-mg)|ym|=.files/image135.gif) ……⑥
……⑥
由圆周运动 qvmB+mg-qE=m.files/image127.gif) ……⑦
……⑦
qE =2mg ……⑧
且由⑥⑦⑧及R=2|ym|解得vm=.files/image137.gif)
29.(12分)
(1)B (2)A
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 |
3.0×10-8 |
(1)物质的量浓度为0.1mol/L的下列四种物质:a.Na2CO3,b.NaClO,c.CH3COONa d.NaHCO3;pH由大到小的顺序是:
(2)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是:
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)?c(OH-) D.c(OH-)/c(H+)
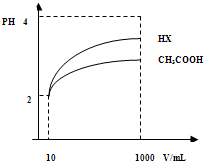
(3)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图.则HX的电离平衡常数
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中
c(CH3COO-)-c(Na+)=
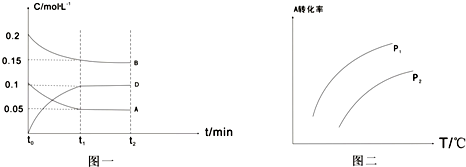
(1)t1=5min,则t0~t1阶段以C的浓度变化表示反应速率为v(C)=
(2)根据图二分析,温度升高,该反应的平衡常数将
(3)若上述反应在T1℃、恒压下进行,A的转化率会
(4)在相同条件下(T1℃时,体积不变的密闭容器中),若起始时容器中加入2molD、
①PCl5(g)?PCl3(g)+Cl2(g);△H1>0 K1=1mol?L-1
②CO(g)+Cl2(g)?COCl2(g);△H1<0 K2=5×104L?mol-1
③COCl2(g)?CO(g)+Cl2(g)
④2SO2(g)+O2(g)?2SO3(g);△H4<0
(1)反应③的平衡常数K3为
(2)要使反应①和反应②的K数值相等,可采取的措施是
A.降低反应①、②体系中Cl2浓度B.反应①、②选择不同的催化剂
C.反应①、反应②同时升高温度D.反应①、反应②同时降低温度
E.反应①降低温度,反应②维持210℃
(3)在甲、乙两容器中分别发生反应④,甲恒容、乙恒压,温度相同且恒定.起始时甲中加入0.02molSO2和0.01molO2,乙中加入0.02molSO3气体,开始时两容器压强相等,最后分别达到平衡.下列有关它们达到平衡状态后的叙述正确的是
A.体积:甲可能小于乙
B.SO3的物质的量:甲一定小于乙
C.压强:甲可能大于乙
D.浓度比c(SO2)/c(SO3):甲一定小于乙
(4)丙容器为容积不变的反应容器,要求通过调节体系的温度使反应④达到平衡时,保持容器内气体总物质的量为12mol.现向容器中加xmolSO2,6.5mol O2,2.0molSO3.
①若x=5.5,需要
②欲使起始反应维持向逆反应方向移动,则x的取值范围为
(8分)下列反应在210℃时达到平衡:
①PCl5(g)PCl3(g)+Cl2(g);△H1>0 K1=1mol·L—1
②CO(g)+Cl2(g)COCl2(g);△H2<0 K2=5×104L·mol—1
③COCl2(g) CO(g)+Cl2(g) △H3 K3
④2SO2(g)+O2(g)2SO3(g);△H4<0
(1)反应③的平衡常数K3为 。
(2)要使反应①和反应②的K数值相等,可采取的措施是 (填序号)。
A.降低反应①、②体系中Cl2浓度 B.反应①、②选择不同的催化剂
C.反应①、反应②同时升高温度 D.反应①、反应②同时降低温度
E.反应①降低温度,反应②维持210℃
(3)在甲、乙两容器中分别发生反应④,甲恒容、乙恒压,温度相同且恒定。起始时甲中加入0.02molSO2和0.01molO2,乙中加入0.02molSO3气体,开始时两容器压强相等,最后分别达到平衡。下列有关它们达到平衡状态后的叙述正确的是 (填序号)。
A.体积:甲可能小于乙 B.SO3的物质的量:甲一定小于乙
C.压强:甲可能大于乙 D.浓度比c(SO2)/c(SO3):甲一定小于乙
(4)丙容器为容积不变的反应容器,要求通过调节体系的温度使反应④达到平衡时,保持容器内气体总物质的量为15mol。现向容器中加入xmolSO2,6.5mol O2,2.0molSO3。
①若x=5.5,需要 (填“降低”“升高”或“保持”)体系温度,使反应在平衡时达到题设要求;
②欲使起始反应维持向逆反应方向移动,则x的取值范围为 。
查看习题详情和答案>>
(8分)下列反应在210℃时达到平衡:
①PCl5(g)PCl3(g)+Cl2(g);△H1>0 K1=1mol·L—1
②CO(g)+Cl2(g)COCl2(g);△H2<0 K2=5×104L·mol—1
③COCl2(g) CO(g)+Cl2(g) △H3 K3
④2SO2(g)+O2(g)2SO3(g);△H4<0
(1)反应③的平衡常数K3为 。
(2)要使反应①和反应②的K数值相等,可采取的措施是 (填序号)。
A.降低反应①、②体系中Cl2浓度 B.反应①、②选择不同的催化剂
C.反应①、反应②同时升高温度 D.反应①、反应②同时降低温度
E.反应①降低温度,反应②维持210℃
(3)在甲、乙两容器中分别发生反应④,甲恒容、乙恒压,温度相同且恒定。起始时甲中加入0.02molSO2和0.01molO2,乙中加入0.02molSO3气体,开始时两容器压强相等,最后分别达到平衡。下列有关它们达到平衡状态后的叙述正确的是 (填序号)。
A.体积:甲可能小于乙 B.SO3的物质的量:甲一定小于乙
C.压强:甲可能大于乙 D.浓度比c(SO2)/c(SO3):甲一定小于乙
(4)丙容器为容积不变的反应容器,要求通过调节体系的温度使反应④达到平衡时,保持容器内气体总物质的量为15mol。现向容器中加入xmolSO2,6.5mol O2,2.0molSO3。
①若x=5.5,需要 (填“降低”“升高”或“保持”)体系温度,使反应在平衡时达到题设要求;
②欲使起始反应维持向逆反应方向移动,则x的取值范围为 。
查看习题详情和答案>>