摘要:氰(CN)2.硫氰(SCN)2的化学性质和卤素很相似.化学上称为拟卤素.如:(CN)2 + H2O = HSCNO + HSCN .它们阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-.试写出:2与KOH溶液反应的化学方程式: .(2)NaBr和KSCN的混合溶液中加入(CN)2反应的离子方程式: .
网址:http://m.1010jiajiao.com/timu_id_239081[举报]
氰气(CN)2、硫氰气(SCN)2的化学性质与X2(卤素)很相似,化学上称为“拟卤素”,如:(SCN)2+H2O=HSCN+HSCNO。它们阴离子的还原性强弱顺序为:Cl-
(1)(CN)2与KOH溶液的反应。
(2)在NaBr和KSCN的混合溶液中通入(CN)2。
氰(CN)2、硫氰(SCN)2的化学性质和卤素很相似,化学上称为“类卤素”,它们阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-.
试写出:
(1)(CN)2与KOH(aq)反应的化学方程式:
(2)NaBr和KSCN的混合溶液中加入足量(CN)2反应的离子方程式:
查看习题详情和答案>>
试写出:
(1)(CN)2与KOH(aq)反应的化学方程式:
(CN)2+2KOH=KCN+KCNO+H2O
(CN)2+2KOH=KCN+KCNO+H2O
;(2)NaBr和KSCN的混合溶液中加入足量(CN)2反应的离子方程式:
2SCN-+(CN)2=(SCN)2+2CN-
2SCN-+(CN)2=(SCN)2+2CN-
.氰(CN)2、氧氰(OCN)2、硫氰(SCN)2、硒氰(SeCN)2的性质相似,在化学上称为拟卤素,CN-、OCN-、SCN-、SeCN一的性质与卤离子相似,已知(OCN)2的电子式为: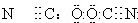 ,则下列电子式正确的是( )
,则下列电子式正确的是( )
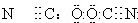 ,则下列电子式正确的是( )
,则下列电子式正确的是( )A、(CN)2  | B、OCN- 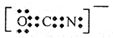 | C、SCN一 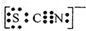 | D、SeCN- |
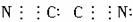 ?
?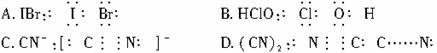 ?
?