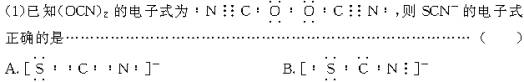题目内容
氰(CN)2和硫氰(SCN)2的性质相似,在化学上称为拟卤素。CN-、SCN-及OCN-的性质与卤素离子相似。已知:不同卤素原子能组成卤素互化物一类卤素,如IBr。完成下列问题:(1)已知(OCN)2的电子式为:![]() ?
?
则SCN-的电子式正确的是( )?
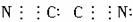 ?
?
(2)下列物质的电子式错误的是( )?
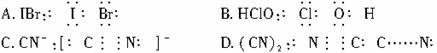 ?
?
解析:(1)有两种解法。
方法1(排除法):根据题给信息,(OCN)2分子中C、N原子间共用3个电子对,这样,A、B选项首先被排除;又因为SCN-是阴离子而非分子,所以D选项也被排除。C可选。
方法2(类比法):由(OCN)2的电子式得OCN-的电子式,由于S、O同主族,所以SCN-电子式同OCN-电子式。
(2)由Br2或I2的电子式:![]() ,可知A选项正确。B正确,较易判定。根据C、N原子间共用3个电子对,可知C正确、D错误。(CN)2的正确电子式是∶
,可知A选项正确。B正确,较易判定。根据C、N原子间共用3个电子对,可知C正确、D错误。(CN)2的正确电子式是∶![]() 。
。
答案:(1)C (2)D

练习册系列答案
相关题目
多原子分子氰(CN)2、硫氰(SCN)2和(OCN)2的性质与卤素单质(Cl2、Br2等)相似,故称它们为拟卤素.它们可以生成酸和盐(见下表,表中X代表F、Cl、Br或I).
(1)在表中①②空格处应分别填写 、 .
(2)①(CN)2和KOH溶液反应的化学方程式为: .
②已知阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-.试写出在NaBr和KSCN的混合溶液中加入(CN)2反应的离子方程式: .
| 卤素 | 氰 | 硫氰 | ① | |
| “单质” | X2 | (CN)2 | (SCN)2 | (OCN)2 |
| 酸 | HX | HCN | ② | HOCN |
| 盐 | KX | KCN | KSCN | KOCN |
(2)①(CN)2和KOH溶液反应的化学方程式为:
②已知阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-.试写出在NaBr和KSCN的混合溶液中加入(CN)2反应的离子方程式: