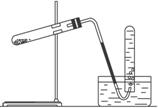
摘要:验室制溴一般用NaBr.浓H2SO4.MnO2共热.即:
网址:http://m.1010jiajiao.com/timu_id_239056[举报]
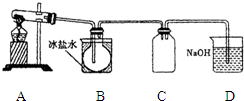 室验室制N2O4需用NO2时,可用无水硝酸盐加热分解获得.已知硝酸盐分解时NO3-完全转化为NO2,现有硝酸盐:a Cu (NO3)2、b Mn (NO3)2、c Hg (NO3)2,若利用加热分解方法制NO2,已知它们分解后的固体生成物为CuO、MnO2、Hg等,并按以下装置(如图所示)制取N2O4;
室验室制N2O4需用NO2时,可用无水硝酸盐加热分解获得.已知硝酸盐分解时NO3-完全转化为NO2,现有硝酸盐:a Cu (NO3)2、b Mn (NO3)2、c Hg (NO3)2,若利用加热分解方法制NO2,已知它们分解后的固体生成物为CuO、MnO2、Hg等,并按以下装置(如图所示)制取N2O4;(1)三种硝酸盐分解时氧化产物与还原产物物质的量之比等于1:4的是
Cu (NO3)2
Cu (NO3)2
.(2)在A中试管内应装入的上述硝酸盐粉末(使产生的NO2最纯净)中应选用的是(写化学式)
Mn (NO3)2
Mn (NO3)2
,其反应的化学方程式为Mn(NO3)2
MnO2+2NO2↑
| ||
Mn(NO3)2
MnO2+2NO2↑
,不应该用的硝酸盐是
| ||
Hg(NO3)2和Cu(NO3)2
Hg(NO3)2和Cu(NO3)2
,理由是因为Hg(NO3)2分解会产生Hg蒸气和O2,Cu(NO3)2分解会产生O2而使NO2不纯
因为Hg(NO3)2分解会产生Hg蒸气和O2,Cu(NO3)2分解会产生O2而使NO2不纯
.(3)B中的烧瓶得到的气体应为
棕黄
棕黄
色,理由是NO2存在平衡:2NO2?N2O4
NO2存在平衡:2NO2?N2O4
.(4)C装置的作用是
起安全瓶作用,防止D中的碱液倒吸至B中
起安全瓶作用,防止D中的碱液倒吸至B中
.(5)D装置的作用是
吸收尾气
吸收尾气
,其中反应的离子方程式为2NO2+2OH-=NO3-+NO2-+H2O
2NO2+2OH-=NO3-+NO2-+H2O
.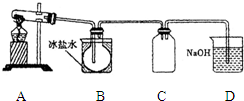 室验室制N2O4需用NO2时,可用无水硝酸盐加热分解获得.已知硝酸盐分解时NO3-完全转化为NO2,现有硝酸盐:a Cu (NO3)2、b Mn (NO3)2、c Hg (NO3)2,若利用加热分解方法制NO2,已知它们分解后的固体生成物为CuO、MnO2、Hg等,并按以下装置(如图所示)制取N2O4;
室验室制N2O4需用NO2时,可用无水硝酸盐加热分解获得.已知硝酸盐分解时NO3-完全转化为NO2,现有硝酸盐:a Cu (NO3)2、b Mn (NO3)2、c Hg (NO3)2,若利用加热分解方法制NO2,已知它们分解后的固体生成物为CuO、MnO2、Hg等,并按以下装置(如图所示)制取N2O4;