网址:http://m.1010jiajiao.com/timu_id_234880[举报]
(1)用金属钠制取Na2O通常采用以下方法:2NaNO3+10Na![]() 6Na2O+N2↑.试说明不用钠在氧气中燃烧而采用此法的原因:________.
6Na2O+N2↑.试说明不用钠在氧气中燃烧而采用此法的原因:________.
(2)金属钠在700℃~800℃时与四氯化钛(TiCl4)反应可以制取金属钛,该反应的化学方程式为________.
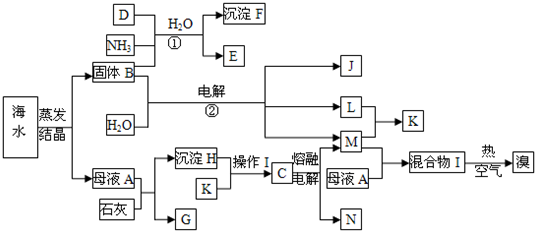
试填写下列空白:
(1)写出反应①②的化学方程式
(2)由沉淀H与K反应得到的溶液中如何得到纯净的C固体?
(3)在工业上反应②主要采用离子交换膜法,下列关于离子交换膜电解槽的叙述错误的是
A.精制饱和固体B溶液进入阳极室
B.纯水(加少量NaOH)进入阴极室
C.阴极产物为氢氧化钠和氢气D.电解槽的阳极用金属铁网制成
(4)工业上制取单质溴,通常是向混合物I中通入热的空气再用SO2吸收,然后经过氯化、蒸馏、分液等操作,简述工业上为什么不用CCl4萃取的方法得到单质溴?
(1)天然水在净化处理过程中加入的混凝剂可以是(写名称)____,其净化水的原理是____。
(2)水的净化和软化的区别是____。
(3)氯碱工业是重要的化学工业,目前工业上主要采用离子交换膜法电解饱和食盐水,下列叙述错误的是___。
A.精制饱和食盐水进入阳极室
B.纯水(加少量NaOH)进入阴极室
C.阴极产物为氢氧化钠和氢气
D.电解槽的阳极用金属铁网制成
(4)从海水中得到的粗盐中含Ca2+、Mg2+、SO42-等杂质离子,这些离子的存在除了会影响电解所得产品的纯度外,还会___,所以电解用食盐水要求对粗盐水进行精制,请将精制时通常加入的化学试剂按加入的先后顺序依次写出:____。
某铜矿石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以此铜矿石为原料制备CuSO4·5H2O及CaCO3,部分步骤如下:
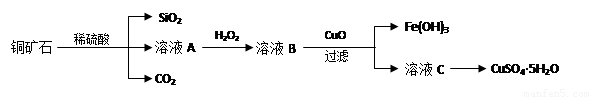
请回答下列问题:
(1)溶液A除含有Cu2+外,还可能含有的金属离子有________(填离子符号);在溶液A中加入H2O2反应的离子方程式是______________。
(2)可用生成的CO2制取优质碳酸钙。制备时,先向氯化钙溶液中通入氨气,再通入CO2。
①实验室通常采用加热氯化铵和氢氧化钙混合物的方法制取氨气。某学习小组选取下图所给部分装置制取并收集纯净的氨气。

如果按气流方向连接各仪器接口,你认为正确的顺序为a→______、______→______、______→ i。其中与i相连漏斗的作用是______________。
②实验室中还可用固体氢氧化钠和浓氨水制取少量氨气,下列最适合完成该实验的简易装置是
_________(填编号)

(3)测定铜矿石中Cu2(OH)2CO3质量百分含量的方法是:a.将1.25g铜矿石制取的CuSO4·5H2O于锥形瓶中,加入适量水完全溶解;b.向溶液中加入100mL0.25mol/L的氢氧化钠溶液使Cu2+完全沉淀;c.过滤;d.滤液中的氢氧化钠溶液用0.5mol/L盐酸滴定至终点,耗用10mL盐酸。则铜矿石中Cu2(OH)2CO3质量分数为_____________。
查看习题详情和答案>>