摘要:A.3.5g
网址:http://m.1010jiajiao.com/timu_id_233600[举报]
a.化学药品与人类健康息息相关.
(1)利用化学合成药物,可保障人体健康.
①青霉素是良好的抗生素,在使用前一定要
②碳酸氢钠[NaHCO3]是某些抗酸药的有效成分.碳酸氢钠与胃酸反应的化学方程式为:
③“OTC”表示
(2)钢铁的生产与使用是人类文明和生活进步的一个重要标志.
①工业炼铁的主要反应方程式为:
②写出铁溶于FeCl3溶液的离子方程式
③为防止轮船的船体在海水中腐蚀,一般在船身连接
b.糖类是人体需要的重要营养素,淀粉是重要的一类糖.
在试管中加入0.5g淀粉和4mL20%的H2SO4溶液,加热3~4min,然后用碱液中和试管中的H2SO4溶液.请回答下列问题:
(1)下列物质富含淀粉的是
(2)淀粉完全水解生成有机物的化学式为
(3)若要检验淀粉没有完全水解,可取少量上述溶液加入
查看习题详情和答案>>
(1)利用化学合成药物,可保障人体健康.
①青霉素是良好的抗生素,在使用前一定要
皮试
皮试
.②碳酸氢钠[NaHCO3]是某些抗酸药的有效成分.碳酸氢钠与胃酸反应的化学方程式为:
HCO3-+H+=H2O+CO2↑
HCO3-+H+=H2O+CO2↑
.胃溃疡的病人能否使用碳酸氢钠不能
不能
(填“能”或“不能”).③“OTC”表示
非处方
非处方
(填“处方药”或“非处方”,下同)药物,消费者不需要持有医生处方就能直接从药房或药店购买的是非处方药物
非处方药物
.(2)钢铁的生产与使用是人类文明和生活进步的一个重要标志.
①工业炼铁的主要反应方程式为:
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.
| ||
②写出铁溶于FeCl3溶液的离子方程式
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
.③为防止轮船的船体在海水中腐蚀,一般在船身连接
镁块
镁块
(填“镁块”或“铜块”).b.糖类是人体需要的重要营养素,淀粉是重要的一类糖.
在试管中加入0.5g淀粉和4mL20%的H2SO4溶液,加热3~4min,然后用碱液中和试管中的H2SO4溶液.请回答下列问题:
(1)下列物质富含淀粉的是
面粉
面粉
(填“面粉”或“青菜”或“猪肉”)(2)淀粉完全水解生成有机物的化学式为
C6H12O6
C6H12O6
.(3)若要检验淀粉没有完全水解,可取少量上述溶液加入
碘水
碘水
(填试剂的名称),应观察到溶液变蓝
溶液变蓝
.
a.化学药品与人类健康息息相关.
(1)利用化学合成药物,可保障人体健康.
①青霉素是良好的抗生素,在使用前一定要 .
②碳酸氢钠[NaHCO3]是某些抗酸药的有效成分.碳酸氢钠与胃酸反应的化学方程式为: .胃溃疡的病人能否使用碳酸氢钠 (填“能”或“不能”).
③“OTC”表示 (填“处方药”或“非处方”,下同)药物,消费者不需要持有医生处方就能直接从药房或药店购买的是 .
(2)钢铁的生产与使用是人类文明和生活进步的一个重要标志.
①工业炼铁的主要反应方程式为: .
②写出铁溶于FeCl3溶液的离子方程式 .
③为防止轮船的船体在海水中腐蚀,一般在船身连接 (填“镁块”或“铜块”).
b.糖类是人体需要的重要营养素,淀粉是重要的一类糖.
在试管中加入0.5g淀粉和4mL20%的H2SO4溶液,加热3~4min,然后用碱液中和试管中的H2SO4溶液.请回答下列问题:
(1)下列物质富含淀粉的是 (填“面粉”或“青菜”或“猪肉”)
(2)淀粉完全水解生成有机物的化学式为 .
(3)若要检验淀粉没有完全水解,可取少量上述溶液加入 (填试剂的名称),应观察到 . 查看习题详情和答案>>
(1)利用化学合成药物,可保障人体健康.
①青霉素是良好的抗生素,在使用前一定要 .
②碳酸氢钠[NaHCO3]是某些抗酸药的有效成分.碳酸氢钠与胃酸反应的化学方程式为: .胃溃疡的病人能否使用碳酸氢钠 (填“能”或“不能”).
③“OTC”表示 (填“处方药”或“非处方”,下同)药物,消费者不需要持有医生处方就能直接从药房或药店购买的是 .
(2)钢铁的生产与使用是人类文明和生活进步的一个重要标志.
①工业炼铁的主要反应方程式为: .
②写出铁溶于FeCl3溶液的离子方程式 .
③为防止轮船的船体在海水中腐蚀,一般在船身连接 (填“镁块”或“铜块”).
b.糖类是人体需要的重要营养素,淀粉是重要的一类糖.
在试管中加入0.5g淀粉和4mL20%的H2SO4溶液,加热3~4min,然后用碱液中和试管中的H2SO4溶液.请回答下列问题:
(1)下列物质富含淀粉的是 (填“面粉”或“青菜”或“猪肉”)
(2)淀粉完全水解生成有机物的化学式为 .
(3)若要检验淀粉没有完全水解,可取少量上述溶液加入 (填试剂的名称),应观察到 . 查看习题详情和答案>>
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
如图所示装置中,甲、乙、丙三个烧杯分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极.接通电源,经过一段时间后,测得乙中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系如图.据此回答下列问题:

(1)M为电源的
(2)计算电极e上生成的气体在标准状况下的体积
(3)写出乙烧杯中发生电解的总反应化学方程式
(4)如果电解过程中B溶液中的金属离子全部析出,此时电解能否继续进行
(5)此时要使丙中溶液恢复到原来的状态,操作是
查看习题详情和答案>>
| 阳离子 | Na+、K+、Cu2+ | ||
| 阴离子 | SO
|

(1)M为电源的
负
负
极(填写“正”或“负”);电极b上发生的电极反应式为4OH--4e-=O2↑+2H2O
4OH--4e-=O2↑+2H2O
.(2)计算电极e上生成的气体在标准状况下的体积
5.6L
5.6L
.(3)写出乙烧杯中发生电解的总反应化学方程式
2CuSO4+2H2O
2Cu+O2↑+2H2SO4
| ||
2CuSO4+2H2O
2Cu+O2↑+2H2SO4
.
| ||
(4)如果电解过程中B溶液中的金属离子全部析出,此时电解能否继续进行
能
能
(填写“能”或“否”)原因为电解硫酸溶液
电解硫酸溶液
.(5)此时要使丙中溶液恢复到原来的状态,操作是
加入4.5g水
加入4.5g水
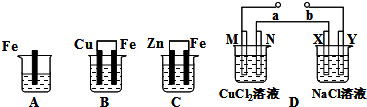
.A、B、C三个烧杯中分别盛有相同物质的量浓度的硫酸铜溶液.D为电解池,其中电极材料均为惰性物质,通过导线与直流电源相连.实验开始时,同时在XY两边各滴入几滴酚酞试液,X极附近首先变红.

请回答以下问题:
(1)B中Cu极电极反应式为
(2)A、B、C三个烧杯中Fe的反应速率最快的是
(3)若C中被腐蚀金属的质量是32.5g,则反应中转移的电子的物质的量是
(4)D中直流电源a为
(5)电池D中N极上的电极反应式为:
(6)D中在M、N、X、Y各电极上析出生成物的物质的量之比为
查看习题详情和答案>>

请回答以下问题:
(1)B中Cu极电极反应式为
Cu2++2e-=Cu
Cu2++2e-=Cu
.(2)A、B、C三个烧杯中Fe的反应速率最快的是
B
B
.(3)若C中被腐蚀金属的质量是32.5g,则反应中转移的电子的物质的量是
1mol
1mol
.(4)D中直流电源a为
负
负
极.(5)电池D中N极上的电极反应式为:
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
.(6)D中在M、N、X、Y各电极上析出生成物的物质的量之比为
1:1:1:1
1:1:1:1
.