网址:http://m.1010jiajiao.com/timu_id_233515[举报]

A.原子得到电子所放出的能量
B.原子半径的大小
C.原子逐个失去电子所吸收的能量
D.原子及形成不同分子的半径的大小
(2)分析同周期自左向右各元素原子的第一个数据:
①总体变化趋势是________(填“增大”或“减小”);
②与前后元素相比,由于该元素的数值增大较多而变得反常的元素位于元素周期表的某些族,分析它们的原子核外电子排布,指出造成上述反常情况的可能原因是______(填序号)。
A.它们的原子半径突然变小些
B.它们的核外电子排布处于饱和状态
C.它们的原子半径突然变大些
D.电子填充时,某些原子轨道达到半充满或全满时,体系稳定性提高
根据以上规律,请推测镁和铝的第一个数据的大小关系为:Mg(1)____Al(1)(填“>”或“<”或“=”)。
(3)每种元素的一组数据中个别地方增大的比例特别大,形成突跃(大幅度增大),请找出这些数据,并根据这些数据出现的规律,你认为氧元素出现该情况的数据应该是氧元素8个数据中的第______个。上述规律可以证明原子结构中____________________的结论。
(14分)
室温下,已知HCl溶液与NaOH溶液的酸碱滴定曲线如下图所示:

(1)向一定量的NaOH溶液中滴加HCl溶液的曲线为图中 (填“实线”或“虚线”)。
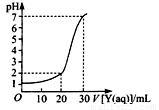
(2)上图为对10mL一定物质的量浓度的NaHSO4溶液X用一定物质的量浓度的氢氧化钠溶液Y滴定的图象,依据图象推出X和Y的物质的量浓度分别是 和 。
(3)某研究性学习小组的研究课题:食醋中总酸量(g/100mL)的测定。他们进行以下滴定操作:
A.取某品牌白醋25.00mL置于 (填仪器名称)中,用蒸馏水稀释10倍。
B.用 (填仪器名称)量取稀释后的白醋溶液20.00mL,置于250mL锥形瓶中,滴入 (填指示剂名称)1~2滴。
C.用0.05 mol·L−1NaOH标准溶液滴定,至终点。记下初始与终点读数。
(注意:滴定重复进行3次。)
根据以上操作,请你继续回答下列问题。
①操作(C)中,滴定时,两眼注视 ;终点现象是 。
②误差分析:下列操作中能使测定结果偏高的是 。
a.稀释白醋的蒸馏水预先未经过煮沸处理
b.盛NaOH溶液的碱式滴定管未用标准液润洗
c.滴定前读数正确,滴定终点时俯视读数
d.接近终点时,用少量蒸溜水洗涤锥形瓶
③如果该小组检测结果与该品牌商标上所注不一致,可能的原因之一是 。
查看习题详情和答案>>
(14分)
室温下,已知HCl溶液与NaOH溶液的酸碱滴定曲线如下图所示:
(1)向一定量的NaOH溶液中滴加HCl溶液的曲线为图中 (填“实线”或“虚线”)。
(2)上图为对10mL一定物质的量浓度的NaHSO4溶液X用一定物质的量浓度的氢氧化钠溶液Y滴定的图象,依据图象推出X和Y的物质的量浓度分别是 和 。
(3)某研究性学习小组的研究课题:食醋中总酸量(g/100mL)的测定。他们进行以下滴定操作:
A.取某品牌白醋25.00mL置于 (填仪器名称)中,用蒸馏水稀释10倍。
B.用 (填仪器名称)量取稀释后的白醋溶液20.00mL,置于250mL锥形瓶中,滴入 (填指示剂名称)1~2滴。
C.用0.05 mol·L−1NaOH标准溶液滴定,至终点。记下初始与终点读数。
(注意:滴定重复进行3次。)
根据以上操作,请你继续回答下列问题。
①操作(C)中,滴定时,两眼注视 ;终点现象是 。
②误差分析:下列操作中能使测定结果偏高的是 。
a.稀释白醋的蒸馏水预先未经过煮沸处理
b.盛NaOH溶液的碱式滴定管未用标准液润洗
c.滴定前读数正确,滴定终点时俯视读数
d.接近终点时,用少量蒸溜水洗涤锥形瓶
③如果该小组检测结果与该品牌商标上所注不一致,可能的原因之一是 。
查看习题详情和答案>>
(14分)
室温下,已知HCl溶液与NaOH溶液的酸碱滴定曲线如下图所示: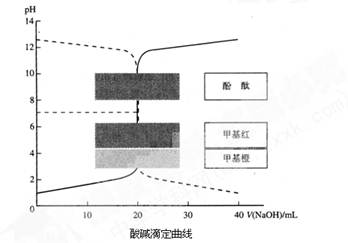
(1)向一定量的NaOH溶液中滴加HCl溶液的曲线为图中 (填“实线”或“虚线”)。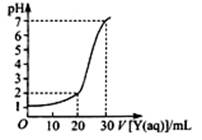
(2)上图为对10mL一定物质的量浓度的NaHSO4溶液X用一定物质的量浓度的氢氧化钠溶液Y滴定的图象,依据图象推出X和Y的物质的量浓度分别是 和 。
(3)某研究性学习小组的研究课题:食醋中总酸量(g/100mL)的测定。他们进行以下滴定操作:
A.取某品牌白醋25.00mL置于 (填仪器名称)中,用蒸馏水稀释10倍。
B.用 (填仪器名称)量取稀释后的白醋溶液20.00mL,置于250mL锥形瓶中,滴入 (填指示剂名称)1~2滴。
C.用0.05 mol·L?1NaOH标准溶液滴定,至终点。记下初始与终点读数。
(注意:滴定重复进行3次。)
根据以上操作,请你继续回答下列问题。
①操作(C)中,滴定时,两眼注视 ;终点现象是 。
②误差分析:下列操作中能使测定结果偏高的是 。
a.稀释白醋的蒸馏水预先未经过煮沸处理
b.盛NaOH溶液的碱式滴定管未用标准液润洗
c.滴定前读数正确,滴定终点时俯视读数
d.接近终点时,用少量蒸溜水洗涤锥形瓶
③如果该小组检测结果与该品牌商标上所注不一致,可能的原因之一是 。

(2)下图为对10mL一定物质的量浓度的NaHSO4溶液X用一定物质的量浓度的氢氧化钠溶液Y滴定的图象,依据图象推出X和Y的物质的量浓度分别是_________ 和__________ 。

A.取某品牌白醋25.00mL置于___________(填仪器名称)中,用蒸馏水稀释10倍。
B.用____________(填仪器名称)量取稀释后的白醋溶液20.00mL,置于250mL锥形瓶中,滴入______________(填指示剂名称)1~2滴。
C.用0.05 mol·L-1 NaOH标准溶液滴定,至终点。记下初始与终点读数。(注意:滴定重复进行3次。)根据以上操作,请你继续回答下列问题。
①操作(C)中,滴定时,两眼注视___________;终点现象是_________ 。
②误差分析:下列操作中能使测定结果偏高的是____________。
a.稀释白醋的蒸馏水预先未经过煮沸处理
b.盛NaOH溶液的碱式滴定管未用标准液润洗
c.滴定前读数正确,滴定终点时俯视读数
d.接近终点时,用少量蒸溜水洗涤锥形瓶
③如果该小组检测结果与该品牌商标上所注不一致,可能的原因之一是_______________ 。