网址:http://m.1010jiajiao.com/timu_id_231835[举报]
| 族 周期 |
IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | A | ||||||
| 2 | B | C | D | E | J | K | L |
| 3 | F | G | H | I | |||
| M |
A.第一电离能:A>B>E>J>K B.电负性:B>C>D>E>J
C.原子半径:F>G>H>E D.D、I分别与L形成的简单分子均为非极性分子
(2)表中A与E可形成A2E=E=EA2分子,有关该分子的说法不正确的是
A.分子中有6个σ键和2个π键
B.三个E原子都是sp2杂化
C.四个A原子不在同一平面内
D.三个E原子在同一条直线上
(3)F晶体的晶胞结构如图,
 它的空间利用率为
它的空间利用率为(4)字母K表示的元素原子基态时的价层电子排布式为
(5)MAL2晶体中包含的微粒间作用力有(填序号)
①离子键 ②极性键 ③分子间作用力 ④金属键
(6)BHA4是一种络合物,中心原子配位数为
①基态Fe3+的M层电子排布式为
②尿素(H2NCONH2)分子中C、N原子的杂化方式分别是
③配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图1,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为
(3)下列说法正确的是
A.第一电离能大小:S>P>Si
B.电负性顺序:C<N<O<F
C.因为晶格能CaO比KCl高,所以KCl比CaO熔点低
D.SO2与CO2的化学性质类似,分子结构也都呈直线型,相同条件下SO2的溶解度更大
E.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
(4)图2是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体.
①图中d单质的晶体堆积方式类型是
②单质a、b、f 对应的元素以原子个数比1:1:1形成的分子中含
③图3是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:
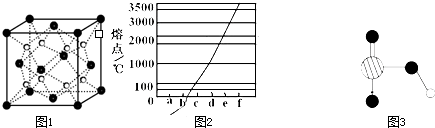
(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6] (NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等。
① 基态Fe3+的M层电子排布式为 。
② 尿素(H2NCONH2)分子中C、N原子的杂化方式分别是 、 ;
③ 配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x= 。 Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于 (填晶体类型)

(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如右图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为 。已知该晶胞的密度为ρ g/cm3,阿伏加德罗常数为NA,求晶胞边长a= cm。 (用含ρ、NA的计算式表示)
(3)下列说法正确的是 _。
A.第一电离能大小:S>P>Si
B.电负性顺序:C<N<O<F
C.因为晶格能CaO比KCl高,所以KCl比CaO熔点低
D.SO2与CO2的化学性质类似,分子结构也都呈直线型,相同条件下SO2的溶解度更大
E.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
(4)图1是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。

① 图中d单质的晶体堆积方式类型是 。
② 单质a、b、f 对应的元素以原子个数比1:1:1形成的分子中含 个σ键, 个π键。
③ 图2是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因: 。
查看习题详情和答案>>
(1)下列说法正确的是_______。
A.全棉是指天然棉花产品
B.涤纶是合成纤维,很难降解
C.保暖内衣有三层,所以保温效果都很好
D.保暖内衣不能透气,否则保暖效果不好
(2)聚乙烯薄膜、涤纶和丙纶复合绒的制造都是以石油作为原料,写出以石油产品乙烯为原料合成聚乙烯的化学方程式______________________________。
(3)上述保暖内衣能否称为环保内衣?为什么?
查看习题详情和答案>>在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
|
物质 |
X |
Y |
Z |
|
初始浓度/mol·L-1 |
0.1 |
0.2 |
0 |
|
平衡浓度/mol·L-1 |
0.05 |
0.05 |
0.1 |
 下列说法正确的是:
下列说法正确的是:
 A.反应达到平衡时,X的转化率为60%
A.反应达到平衡时,X的转化率为60%
B.反应可表示为X+3Y 2Z,其平衡常数为1600
2Z,其平衡常数为1600
 C.增大压强使平衡向生成Z的方向移动,平衡常数增大
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
查看习题详情和答案>>