网址:http://m.1010jiajiao.com/timu_id_216451[举报]
生物答案
1--
30题【答案】(每空2分,共26 分)
(1)ACDE (2)缺氧不能进行有氧呼吸,产生能量少,抑制了根对矿质元素的吸收 右移(3)细胞质基质 线粒体(顺序可调,每个1分) (4)③
(5)下移 右移 下移
(6)唾液中形成的是唾液淀粉酶,是通过脱水缩合形成的;尿液中形成的是尿素,是通过脱氨基作用形成的
(7)B
(8) ①土壤微生物分解有机物产生植物光合作用所需原料CO2
②土壤微生物分解有机物产生植物所需矿质元素。
31题【答案】
(二)3.都注射大量并等量胰岛素溶液(3分),大白鼠都出现四肢无力,活动减少,甚至昏迷等低血糖症状(2分)
4.将昏迷的大白鼠每2只一组,每组分别注射胰高血糖素溶液、葡萄糖溶液和生理盐水(3分),除了注射生理盐水的一组仍然昏迷外,其余2组的大白鼠都苏醒过来(2分)
(三)分析预期的实验结果
当给动物注射大剂量的胰岛素时,动物因血糖下降使脑供能不足而昏迷,在注射葡萄糖后动物苏醒,说明胰岛素具有降低血糖的作用,(3分);同时注射胰高血糖素动物苏醒,从而说明胰高血糖素具有升高血糖的作用(3分)。
化学答案
题号
6
7
8
9
10
11
12
13
答案
A
D
C
B
D
D
B
C
26、(14分)
1)①
 ②
②
 ③
③

2)

3)④C Si ⑤O S (其它合理答案也行)
27、(14分)
1)< < 2)DE ADE
3)> < 4)C
28、(18分)
1)①A ②B
2)③在蓝色沉淀中加入过量稀 ,若完全溶解则证明无铜生成。
,若完全溶解则证明无铜生成。
④
⑤4
3)⑥将铁片和铜片连在一起投入硫酸铜溶液中。
⑦

4)D
29、(14分) Be 1.8g
物理答案
(每小题6分,共48分)
题号
14
15
16
17
18
19
20
21
答案
B
C、D
C、D
D
A
D
A、C
B、D
22(18分)
(Ⅰ)(6分)A.② B.① C.①②③ (每空2分,C答案不完整不给分)
(Ⅱ)(12分)⑴外接,分压式(每空2分)⑵电路图略(3分)⑶连线(3分)⑷大于(2分)
23.(16分)
解: ⑴设经时间 两球相碰,则
两球相碰,则  (5分)
(5分)
 (2分)
(2分)
⑵在竖直方向上  (6分)
(6分)
即  (负解舍去) (3分)
(负解舍去) (3分)
24.(18分)
解:(1)物块恰能通过最高点C时,圆弧轨道与物块之间没有力作用,物块受到重力和电场力提供向心力。mg-qE=mvc2/R (4分)
物块在由A运动到C的过程中,设物块克服摩擦力做的功为W,根据动能定理有 qE2R-W-mg2R=mvC2/2-mv02/2 (4分)
解得W= mv02/2+5(qE-mg)R/2 (2分)
(2)物块离开半圆形轨道后做类平抛运动,设水平位移为S,则水平方向有S=vCt (3分)
竖直方向有2R=(g-qE/m)t2/2 (3分) 解得 S=2R
因此物块离开轨道落回水平面的水平距离与场强E大小无关,大小为2R. (2分)
25.(20分) w.w.w.k.s.5.u.c.o.m
解:①设A物块碰撞B物块前后的速度分别为v1和v2,碰撞过程中动量守恒,
 代入数据得:
代入数据得:  (4分)
(4分)
②设A、B两物块碰撞前后两物块组成的系统的机械能分别为E1和E2,机械能的损失为 ,根据能的转化和守恒定律:
,根据能的转化和守恒定律: 

 %
(6分)
%
(6分)
③设物块A的初速度为v0,轮胎与冰面的动摩擦因数为µ,A物块与B物块碰撞前,根据动能定理:
 (2分)
(2分)
碰后两物块共同滑动过程中根据动能定理:
 (2分)
(2分)
由 、
、  及(1)、(2)得:
及(1)、(2)得: (2分)
(2分)
设在冰面上A物块距离B物块为L′时,A物块与B物块不相撞,
则: (2分)
(2分)
 (2分)
(2分)
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
甲:向两只试管中,分别注入0.8mol/L的乙醇和苯酚溶液3mL,各放入一小块金属钠,观察反应产生H2的速率.
乙:在两只试管中,分别放入1g乙醇和苯酚晶体,各注入3mL蒸馏水,振荡,得到乙醇溶液和苯酚浊液,再向两试管中逐滴加入5molL的NaOH溶液,观察其中的变化.
(1)苯酚溶液与钠反应的离子方程式为
(2)对于甲、乙两个实验方案,他们能否达到实验目的?理由各是什么?
(Ⅱ)在分析甲、乙两同学实验方案的基础上,丙同学进行了下列对比实验:
在两只试管中,分别放入2g无水乙醇和苯酚晶体,用约60℃的水浴加热,待苯酚熔成液态后,再向两试管中各放入一小块金属钠.在乙醇中,钠块能与乙醇反应产生气体,约3min后钠块消失,溶液保持澄清;在苯酚中,钠块表面有少量气泡,约2min后出现少量白色悬浮物,10min后白色悬浮物充满苯酚熔融液,振荡后发现钠块尚未完全消失.
(3)丙同学的实验表明,苯酚熔融液与钠的反应速率不如无水乙醇与钠的反应快,其主要原因是
(4)请你设计一个探究苯酚和乙醇分子中羟基上氢原子活泼性的实验方案:
 含钡化合物在实验室和工业生产中都有广泛的用途.
含钡化合物在实验室和工业生产中都有广泛的用途.
(1)过氧化钡(BaO2)是一种常用的氧化剂,还可用于生产钡盐.工业上制取过氧化钡的方法之一是2BaO+O2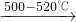 2BaO2.现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨.那么实际参加反应的氧化钡的质量为______吨.
2BaO2.现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨.那么实际参加反应的氧化钡的质量为______吨.
(2)某同学查得Ba(OH)2?8H2O晶体在20℃时的溶解度为3.9g/100g水,则20℃时,Ba(OH)2饱和溶液的质量分数为______(答案保留2位小数).
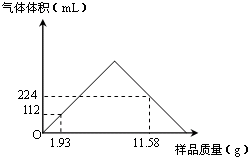
(3)取不同质量由Ba(OH)2?nH2O和BaCO3组成的样品,加水溶解后加入80mL 1.0mol/L的盐酸,并不断地搅拌,所得CO2气体的体积(已换算为标准状况)与加入样品的质量关系通过描点得到下图(在此过程中不考虑Ba(HCO3)2的生成和CO2的溶解).请计算:
①在11.58g样品中BaCO3的质量为多少g?
②化学式Ba(OH)2?nH2O中n的值为多少?
(4)含钡的矿物大多是重晶石(主要成分是BaSO4),工业上常用天然气在850~900℃的条件下还原BaSO4生产BaS.发生反应的化学方程式有:
BaSO4+CH4(少量)→BaS+CO2+2H2O
3BaSO4+4CH4(足量)→3BaS+4CO+8H2O
①若反应后混合气体中CO2的体积分数为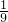 ,求该反应条件下混合气体的平均式量?
,求该反应条件下混合气体的平均式量?
(假设每步反应都完全.答案保留2位小数)
②实际工业生产中,天然气很难反应完全.现有2.0×106 mol的CH4,若CH4的利用率为95%,且反应结束后高温气体中CO的体积分数为0.02,求能生产多少吨BaS?(答案保留2位小数)
查看习题详情和答案>>
某同学查阅有关资料,了解到以下相关信息:
亚硝酸及亚硝酸盐的资料:
(1)HNO2是一种弱酸(比醋酸略强),且不稳定,易分解生成NO和NO2
(2)HNO2能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把氧化成I2
(3)AgNO2种难溶于水易溶于酸的化合物
(4)NaNO2制备:
2NaOH+NO+NO2═2NaNO2+H2O
2NO2+2NaOH═NaNO3+NaNO2+H2O
2NaNO3
| ||
试回答下列问题:
(1)人体正常的血红蛋白中应含Fe2+.若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是
A.亚硝酸盐是还原剂 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐被还原
(2)下列方法中,不能用来区别NaNO2和NaCl的是
A.测定这两种溶液的pH
B.用AgNO3和HNO3两种试剂来区别
C.在酸性条件下加入KI淀粉试液来区别
D.分别在这两种溶液中滴加甲基橙
(3)为了测定某样品中NaNO2的含量,可以使用标准KMnO4溶液进行滴定,试回答:
①KMnO4溶液在滴定过程中作
②若滴定终点读数时目光俯视,则所得结果
(4)某同学在家中欲进行鉴别NaCl与NaNO2的实验,但他家中只有浓醋酸,请问该实验能否成功?说明理由.
(5)现有氮的三种常见氧化物组成的混和气体44.8L(体积已换算成标准状态),其中N2O4、NO体积分数都为20%.
①将该气体通入适量的NaOH溶液中恰好反应,则溶液中NaNO2的质量是
②反应后的溶液蒸干灼烧则NaNO2物质的量
A.元素的单质可由氧化或还原该元素的化合物来制得
B.在氧化还原反应中,有一种元素被氧化,肯定有另一种元素被还原
C.阳离子只能得到电子被还原,失电子难的原子获得电子的能力一定强
D.含有最高价元素的化合物不一定具有强氧化性 查看习题详情和答案>>
(6分)下列说法正确的是 (填序号)。
①由于碘在酒精中的溶解度大,所以可用酒精将碘水中的碘萃取出来
②水的沸点是100℃,酒精的沸点是78.5℃,用直接蒸馏法能使含水酒精变为无水酒精
③由于胶粒的直径比离子大,所以淀粉溶液中混有的碘化钾可用渗析法分离
④分离苯和苯酚的混合液,先加入适量浓溴水,再过滤、分液,即可实现
⑤由于高级脂肪酸钠盐在水中的分散质微粒直径在1nm~100 nm之间,所以可用食盐使高级脂肪酸纳从皂化反应后的混合物中析出
⑥不慎把苯酚溶液沾到皮肤上,应立即用酒精洗涤
⑦用稀溴水滴入苯酚溶液中制备2,4,6-三溴苯酚
⑧实验室使用体积比为1:3的浓硫酸与乙醇的混合溶液制乙烯时,为防加热时反应混合液出现暴沸现象,除了要加沸石外,还应注意缓慢加热让温度慢慢升至170℃
17..(18分)某化学小组采用类似制乙酸乙酯的装置(如右图),以环己醇制备环己烯:
 已知:
已知:
| 密度 | 熔点 | 沸点 | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是 ,
导管B除了导气外还具有的作用是 。
②试管C置于冰水浴中的目的是 。
 (2)制备精品
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和
食盐水,振荡、静置、分层,环己烯在 层(填
“上”或“下”),分液后用 (填入编号)洗涤。
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液
②再将环己烯按右图装置蒸馏,冷却水从 口进入。
蒸馏时要加入生石灰,目的是: 。
③收集产品时,控制的温度应在 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是 ( )
A.蒸馏时从70℃开始收集产品 B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是 ( )
A.用酸性高锰酸钾溶液 B.用金属钠 C.测定沸点
18.(12分)有机
物A的结构简式为![]() ,它可通过不同化学反应分别制得B、C、D和E四种物质。
,它可通过不同化学反应分别制得B、C、D和E四种物质。

请回答下列问题:
(1)指出反应的类型:A→C: 。
(2)在A~E五种物质中,互为同分异构体的是 (填代号)。
(3)写出由A生成B的化学方程式
。
(4)已知HCHO分子中所有原子都在同一平面内,则在上述分子中所有的原子有可能都在同一平面的物质是 (填序号)。
(5)C能形成高聚物,该高聚物的结构简式为 。
(6)写出D与NaOH溶液共热反应的化学方程式
。
19.(16分)肉
桂酸甲酯( )常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精
)常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精
⑴肉桂酸甲酯的分子式是 ;
 ⑵下列有关肉桂酸甲酯的叙述中,正确的是 填字母);
⑵下列有关肉桂酸甲酯的叙述中,正确的是 填字母);
A.能与溴的四氯化碳溶液发生加成反应
B.无法使酸性高锰酸钾溶液褪色
C.在碱性条件下能发生水解反应
D.不可能发生加聚反应
⑶G为肉桂酸甲酯的一种同分异构体,其分子结构模型如右图所示(图中球与球之间连线表示单键或双键)。则G的结构简式为 ;
⑷用芳香烃A为原料合成G的路线如下:

①化合物E中的官能团有 (填名称)。
②F→G的反应类型是 ,该反应的化学方程式为 _ _ 。
③C→D的化学方程式为 _。
④写出符合下列条件的F的同分异构体的结构简式 。O%M
ⅰ.分子内含苯环,且苯环上只有一个支链;
ⅱ.一定条件下,1mol该物质与足量银氨溶液充分反应,生成4mol银单质。
20.(10分)有机物A的蒸汽对同温同压下氢气的相对密度为31,取3.1克A物质在足量氧气中充分燃烧,只生成2.7克水和标准状况下CO22.24L,求有机物的分子式;若该有机物0.2mol恰好与9.2克金属钠完全反应,请写出有机物的结构简式并命名。
查看习题详情和答案>>