网址:http://m.1010jiajiao.com/timu_id_199270[举报]
选择题
题号
1
2
3
4
5
6
7
8
9
10
答案
D
B
D
D
D
D
C
A
D
B
题号
11
12
13
14
15
16
17
18
19
20
答案
C
A
C
B
A
D
B
C
B
D
21.(1)24FeSO4+30HNO3→8Fe(NO3)3+8Fe2(SO4)3+3N2O+15H2O
(2)FeSO4 +5价N (3) 得到 4
22.(1)>。在亚硫酸氢钠溶液中,存在HSO3-的电离平衡:HSO3-  H++SO32-,还有HSO3-的水解平衡:HSO3-+H2O
H++SO32-,还有HSO3-的水解平衡:HSO3-+H2O H2SO3+OH-。由题给信息[SO32-]>[H2SO3]可得出,其水解程度比电离程度弱,所以可确定[H+]>[OH-]。
H2SO3+OH-。由题给信息[SO32-]>[H2SO3]可得出,其水解程度比电离程度弱,所以可确定[H+]>[OH-]。
 (2)含酚酞的氢氧化钠溶液的红色褪去,溶液呈无色。加入少量氢氧化钠溶液时,只有HSO3-反应,反应的离子方程式为:HSO3-+OH-=SO32-+H2O。
(2)含酚酞的氢氧化钠溶液的红色褪去,溶液呈无色。加入少量氢氧化钠溶液时,只有HSO3-反应,反应的离子方程式为:HSO3-+OH-=SO32-+H2O。
23.(1) 0.01mol/L. min
(2) a=0.05 mol/L 图象如右
(3) BD
24.(1)Br2 ;Fe3+
(2)
乙 同学正确
选用试剂
实验现象
第一种方法
C
有机层无色
第二种方法
D
溶液变红
(3)Fe2+;不可以,因为Br2和Fe3+都能把I―氧化成I2
25.(1)b;
(2)将亚铁离子氧化为铁离子;
(3)除去过量的硫酸;不引入新的杂质;
(4)Fe3++3H2O=Fe(OH)3↓+3H+;(条件:加热)
(5)抑制Cu2+的水解;产生污染环境的二氧化硫,硫酸利用率低;加热,并在稀硫酸中通入氧气。(注:本题为发散性试题,如有其它合理答案,酌情给分)
 26.
26. ⑴ C6H5-CH-18OH CH3CH2- -18OH
⑴ C6H5-CH-18OH CH3CH2- -18OH

 ⑵C6H5-CH-18OH+HCOOH
⑵C6H5-CH-18OH+HCOOH HCO18O-CH-C6H5+H2O
HCO18O-CH-C6H5+H2O
⑶

计算题
27.(1)0.8mol/L (2)29.6%
附加题
1.B
2.C
3.(1)除去混在氢气中的酸性气体
(2)A B、C; 将E中的产生的硫酸亚铁溶液压入D中
(3)②
(4)用氢氧化钠溶液除去混在氢气中的酸性气体;氢氧化钠溶液重复使用;用氢气驱赶氧气,防止亚铁盐被氧化;等其它合理答案
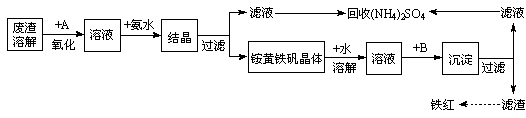
工业上利用硫酸渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3 )和回收(NH4)2SO4,具体生产流程如下:
回答下列问题:
(1)在废渣溶解操作时,为了加速废渣溶解的措施是:___________________、__________________(任写两点)
(2)物质A是一种氧化剂
①工业上最好选用 (填序号)
| A.空气 | B.Cl2 | C.MnO2 | D.H2O2, |
③写出A参与反应的离子方程式为__________________________________________
(3根据下图有关数据,你认为工业上氧化操作时应控制的条件是__________________。
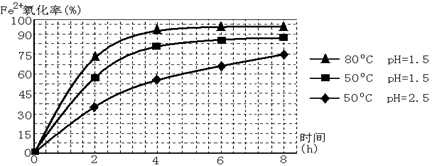
(4)往铵黄铁矾溶液(含Fe3+)中加入溶液B至pH为5时产生沉淀,请写出产生沉淀的离子方程式:_______________________________________________________。
(5)写出铵黄铁矾晶体溶于适量蒸馏水中,往其中加入过量Ba(OH)2溶液,发生反应的离子方程式为:_____________________________________________________
(6)回收所得的(NH4)2SO4晶体可能含有的杂质是:___________________________ 查看习题详情和答案>>
回答下列问题:
(1)在废渣溶解操作时,为了加速废渣溶解的措施是:___________________、__________________(任写两点)
(2)物质A是一种氧化剂
①工业上最好选用 (填序号)
| A.空气 | B.Cl2 | C.MnO2 | D.H2O2, |
③写出A参与反应的离子方程式为__________________________________________
(3根据下图有关数据,你认为工业上氧化操作时应控制的条件是__________________。
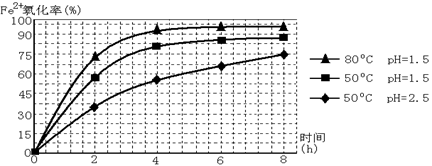
(4)往铵黄铁矾溶液(含Fe3+)中加入溶液B至pH为5时产生沉淀,请写出产生沉淀的离子方程式:_______________________________________________________。
(5)写出铵黄铁矾晶体溶于适量蒸馏水中,往其中加入过量Ba(OH)2溶液,发生反应的离子方程式为:_____________________________________________________
(6)回收所得的(NH4)2SO4晶体可能含有的杂质是:___________________________
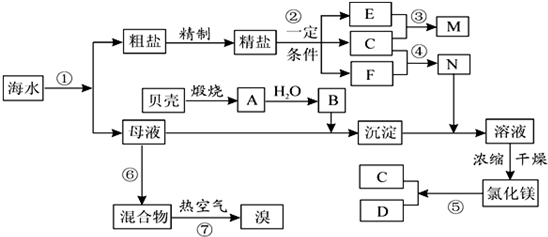
请根据以上信息回答下列问题:
I(1)写出N的化学式和B的名称:N
(2)写出反应②的化学方程式
| ||
| ||
(3)写出反应③的离子方程式:
Ⅱ粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液
③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为
A.②③④①B.③④②①C.④③②①D.③②④①
Ⅲ提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2.
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是
A.分解反应B.化合反应C.置换反应 D.复分解反应
(2)氮气和氩是两种化学性质相对稳定的气体,都可用做白炽灯的填充气体.但工业上冷却电解无水氯化镁所得的镁蒸气时,却选择稀有气体氩.试用化学反应方程式解释不选用氮气的原因:
| ||
| ||
(3)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是
A.从外地购买B.在当地新建生产厂
C.从本厂生产烧碱处循环D.从本厂生产镁单质处循环
流程⑦将溴单质从混合物中分离出来是基于溴单质具有
(4)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2
乙:母液先提取Br2,后提取Mg
请你判断哪个更合适?
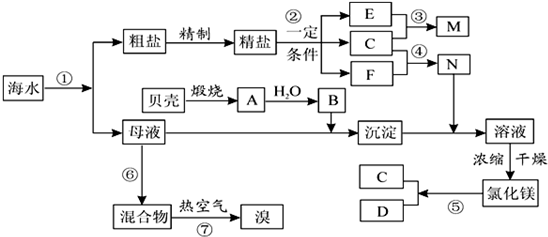
请根据以上信息回答下列问题:
I(1)写出N的化学式和B的名称:N______、B______.
(2)写出反应②的化学方程式______
(3)写出反应③的离子方程式:______,
Ⅱ粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液
③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为______.
A.②③④①B.③④②①C.④③②①D.③②④①
Ⅲ提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2.
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是______.
A.分解反应B.化合反应C.置换反应 D.复分解反应
(2)氮气和氩是两种化学性质相对稳定的气体,都可用做白炽灯的填充气体.但工业上冷却电解无水氯化镁所得的镁蒸气时,却选择稀有气体氩.试用化学反应方程式解释不选用氮气的原因:______.
(3)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是______.
A.从外地购买B.在当地新建生产厂
C.从本厂生产烧碱处循环D.从本厂生产镁单质处循环
流程⑦将溴单质从混合物中分离出来是基于溴单质具有______性.
(4)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2
乙:母液先提取Br2,后提取Mg
请你判断哪个更合适?______(填“甲”或“乙”),理由是______.

请根据以上信息回答下列问题:
I(1)写出N的化学式和B的名称:N 、B .
(2)写出反应②的化学方程式
(3)写出反应③的离子方程式: ,
Ⅱ粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液
③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为 .
A.②③④①B.③④②①C.④③②①D.③②④①
Ⅲ提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2.
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是 .
A.分解反应B.化合反应C.置换反应 D.复分解反应
(2)氮气和氩是两种化学性质相对稳定的气体,都可用做白炽灯的填充气体.但工业上冷却电解无水氯化镁所得的镁蒸气时,却选择稀有气体氩.试用化学反应方程式解释不选用氮气的原因: .
(3)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是 .
A.从外地购买B.在当地新建生产厂
C.从本厂生产烧碱处循环D.从本厂生产镁单质处循环
流程⑦将溴单质从混合物中分离出来是基于溴单质具有 性.
(4)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2
乙:母液先提取Br2,后提取Mg
请你判断哪个更合适? (填“甲”或“乙”),理由是 . 查看习题详情和答案>>