摘要:4表2:备选试剂 序号ABCDE化学式CuOH2O2稀HNO3KMnO4回答下列问题:(1)X:――――――Y:――――――(2)沉淀Ⅱ的化学式为 .证明步骤③中沉淀是否完全的操作方法是 . (3)写出步骤②反应的离子方程式 . (4)为了获得更多较纯的无水CuCl2.步骤⑤在加热的同时.还需要 理由是 : .
网址:http://m.1010jiajiao.com/timu_id_18839[举报]
某化学兴趣小组拟用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水CuCl2。实验步骤如下所示:

表1 物质沉淀时的pH
物 质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀时的pH | 2.7 | 7.6 | 5.2 |
完全沉淀的pH | 3.7 | 9.6 | 6.4 |
表2 备选试剂
序 号 | A | B | C | D | E |
化学式 | NaOH | CuO | H2O2 | 稀HNO3 | KMnO4 |
回答下列问题:
(1)X_________;Y_________。(填写备选试剂中的序号)
(2)沉淀(Ⅱ)的化学式_____,证明步骤③中沉淀是否完全的操作方法是____________。
(3)第⑤步骤操作中,所需装置如图所示:

按气流从左至右的方向,各装置接口的连接顺序为_________。
D装置的作用是______________________;理由______________________。
查看习题详情和答案>>(每空2分 共14分)现有NaCl、Na2SO4和NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl—、SO42-、NO3—的相互分离,实验过程如图所示: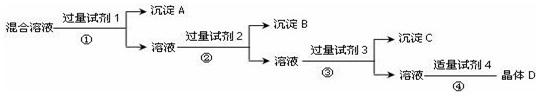
请回答下列问题:
(1)写出实验过程中所用试剂为:
试剂1__________试剂2___________试剂3__________试剂4____________
(2)加入试剂3过量的目的是____________________________________________
(3)操作①的名称是_____________
(4)在加入试剂4后,获得晶体D的实验操作④的名称是_____________
(2009?东城区二模)某化学课外活动小组设计实验探究氮的化合物的性质,装置如图所示(A装置未画出),其中A为气体发生装置.A中所用试剂从下列固体物质中选取:a.NH4HCO3、b.NH4Cl、c.Ca(OH)2、d.NaOH
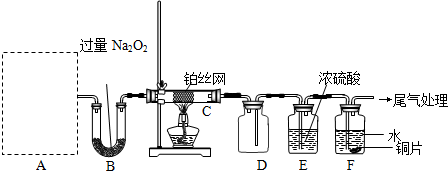
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯.部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:
(3)对于C中发生的可逆反应,下列说法正确的是
a.增大一种反应物的浓度可以提高另一种反应物的转化率
b.工业上进行该反应时,可采取高压的条件提高反应物转化率
c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
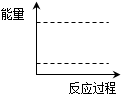
(4)请在下图坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式
 .
.
(5)待实验结束后,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是
查看习题详情和答案>>

检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯.部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
a
a
(填备选试剂的字母);此时A中主要的玻璃仪器有试管、酒精灯
试管、酒精灯
(填名称).(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:
2Na2O2+2H2O=4NaOH+O2 或2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2H2O=4NaOH+O2 或2Na2O2+2CO2=2Na2CO3+O2
.(3)对于C中发生的可逆反应,下列说法正确的是
a
a
.a.增大一种反应物的浓度可以提高另一种反应物的转化率
b.工业上进行该反应时,可采取高压的条件提高反应物转化率
c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
(4)请在下图坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式



(5)待实验结束后,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是
0.25
0.25
mol,甲在标准状况下是2.8
2.8
L(忽略气体的溶解).某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:

部分阳离子以氢氧化物形式完全沉淀时溶液的pH见上表,请回答下列问题:
(1)“浸出”步骤中,为提高镁的浸出率,该工业流程中采取的措施是
(2)以MgCO3和MgSiO3为例,写出“浸出”步骤发生反应的离子方程式:
(3)第一次加NaOH溶液调整pH到5.5的目的是
(4)在实验室中从Mg(OH)2获得无水MgCl2的操作如下:把Mg(OH)2溶解在过量的
(5)Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
MgCl2+2NaClO3═Mg(ClO3)2+2NaCl已知四种化合物的溶解度(S)随温度(T)变化曲线如图所示:将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2.简述可制备Mg(ClO3)2的原因:
查看习题详情和答案>>

| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| pH | 3.4 | 5.2 | 12.4 |
(1)“浸出”步骤中,为提高镁的浸出率,该工业流程中采取的措施是
研磨固体废料
研磨固体废料
,你认为还可以采取的措施有增大硫酸浓度
增大硫酸浓度
、加热升高温度、边加硫酸边搅研拌
加热升高温度、边加硫酸边搅研拌
(写出两条).(2)以MgCO3和MgSiO3为例,写出“浸出”步骤发生反应的离子方程式:
MgCO3+2H+=Mg2++CO2↑+H2O
MgCO3+2H+=Mg2++CO2↑+H2O
,MgSiO3+2H+=Mg2++H2SiO3↓
MgSiO3+2H+=Mg2++H2SiO3↓
(3)第一次加NaOH溶液调整pH到5.5的目的是
使Fe3+、Al3+全部转化为氢氧化物沉淀与Mg2+分离
使Fe3+、Al3+全部转化为氢氧化物沉淀与Mg2+分离
,控制pH的方法是通过pH计控制溶液的pH
通过pH计控制溶液的pH
,滤渣I的主要成分有Fe(OH)3、Al(OH)3
Fe(OH)3、Al(OH)3
.(4)在实验室中从Mg(OH)2获得无水MgCl2的操作如下:把Mg(OH)2溶解在过量的
盐酸
盐酸
(填写试剂的名称)中;加热浓缩,冷却结晶,过滤
过滤
,洗涤
洗涤
(填操作名称)可得到MgCl2?6H2O;在干燥的HCl气流中加热脱水
在干燥的HCl气流中加热脱水
(填写具体操作),即可得到无水的MgCl2.
(5)Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
MgCl2+2NaClO3═Mg(ClO3)2+2NaCl已知四种化合物的溶解度(S)随温度(T)变化曲线如图所示:将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2.简述可制备Mg(ClO3)2的原因:
该反应的生成物为Mg(ClO2)2和NaCl的混合溶液,NaCl的溶解度随温度变化不大,Mg(ClO2)2的溶解度随温度升高而升高,利用两物质的溶解度差异,通过加热蒸发浓缩,冷却结晶,过滤,将Mg(ClO2)2与NaCl分离,制得Mg(ClO2)2;
该反应的生成物为Mg(ClO2)2和NaCl的混合溶液,NaCl的溶解度随温度变化不大,Mg(ClO2)2的溶解度随温度升高而升高,利用两物质的溶解度差异,通过加热蒸发浓缩,冷却结晶,过滤,将Mg(ClO2)2与NaCl分离,制得Mg(ClO2)2;
.蛇纹石矿可以看做MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制取碱式碳酸镁的实验步骤如图所示.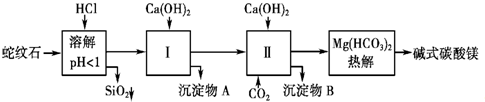
(1)蛇纹石加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见上表)Ca(OH)2不能过量,若Ca(OH)2过量可能会导致
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入
(4)物质循环使用,能节约资源.上述实验中,可以循环使用的物质是
(5)现设计一个实验,确定产品aMgCO3?bMg(OH)2?cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量
②高温分解
③
④
⑤MgO称量
(6)18.2g产品完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:
a=
查看习题详情和答案>>

(1)蛇纹石加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是
Fe3+、Al3+
Fe3+、Al3+
.| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
Al(OH)3
Al(OH)3
溶解、Mg(OH)2
Mg(OH)2
沉淀.(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入
NaOH或Ca(OH)2
NaOH或Ca(OH)2
(填入物质的化学式),然后过滤、洗涤、灼烧
过滤、洗涤、灼烧
(依次填写实验操作名称).(4)物质循环使用,能节约资源.上述实验中,可以循环使用的物质是
CaCO3或CO2
CaCO3或CO2
(填写物质化学式).(5)现设计一个实验,确定产品aMgCO3?bMg(OH)2?cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量
②高温分解
③
用浓硫酸吸收水蒸气
用浓硫酸吸收水蒸气
.④
称量碱石灰吸收CO2前后的质量
称量碱石灰吸收CO2前后的质量
.⑤MgO称量
(6)18.2g产品完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:
a=
3
3
,b=1
1
,c=3
3
.