网址:http://m.1010jiajiao.com/timu_id_186909[举报]
下列事实不能用化学平衡移动原理来解释的是
- A.在强碱存在的条件下,酯在水中的溶解度增大
- B.加催化剂,使氮气和氢气在一定条件下转化为氨
- C.可用浓氨水和氢氧化钠固体快速制取氨气
- D.加压有利于二氧化硫与氧气反应生成三氧化硫
下列事实不能用化学平衡移动原理来解释的是( )
A.在强碱存在的条件下,酯在水中的溶解度增大
B.加催化剂,使氮气和氢气在一定条件下转化为氨
C.可用浓氨水和氢氧化钠固体快速制取氨气
D.加压有利于二氧化硫与氧气反应生成三氧化硫
查看习题详情和答案>>
A.在强碱存在的条件下,酯在水中的溶解度增大
B.加催化剂,使氮气和氢气在一定条件下转化为氨
C.可用浓氨水和氢氧化钠固体快速制取氨气
D.加压有利于二氧化硫与氧气反应生成三氧化硫
查看习题详情和答案>>
(1)金属活动性顺序是学习“金属及其化合物”的重要工具,许多“金属及其化合物”的知识规律可以通过金属活动性顺序来掌握.例如,工业上冶炼金属,根据金属活动性顺序可以采用不同的冶炼方法.其中可以用“热分解法”冶炼的金属是
工业上又常用下列反应进行金属钾的冶炼:Na+KCl
| ||
(2)在实践中发现还有许多化学事实“违背”金属活动性顺序,但这些“反常”现象都可以通过化学原理得到合理解释.某学生在做探究实验时,把锌粒投入1mol?L-1氯化铁溶液中,观察到如下实验现象:锌粒表面有一定量气泡产生,溶液颜色逐渐变浅,一段时间后溶液逐渐浑浊,试用相关反应方程式进行解释
(3)研究金属活动性顺序还可以指导对金属阳离子氧化性强弱的认识,工业上用氯化铁溶液腐蚀铜制电路板.
①请根据金属活动性顺序结合该反应原理,比较Cu2+、Fe3+、Fe2+的氧化性强弱
②请运用原电池原理设计实验验证Cu2+、Fe3+氧化性强弱的结论.
方案:
(Ⅰ)下图甲和乙是某学校王老师制备NH3并进行性质实验时的改进装置。按图甲把仪器安装好,称取2g固体氯化铵装入试管底部,再快速称取2g氢氧化钠覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL浓氨水);烧杯内盛滴有酚酞试液的水;把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡。
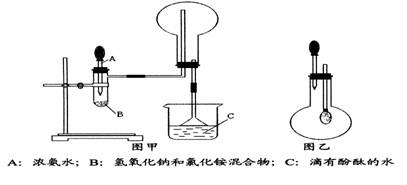
(Ⅱ)将Ⅰ中收满NH3的圆底烧瓶取下,改装成图乙所示的装置,胶头滴管内事先预吸入2mLH2O,此时小气球系在玻璃棒上呈自然松弛状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质。按要求回答下列问题:
(1)中学化学教材中是用与制O2相同的制备装置来加热制取NH3的,该化学方程式为______________________________________________________________;
(2)下面是某同学关于王老师能用图甲制取NH3的原因分析,有道理的是_____________
①在NH3?H2O中有平衡NH3+H2O![]() NH3?H 2O
NH3?H 2O![]() NH4++OH-,加NaOH使平衡向左移动
NH4++OH-,加NaOH使平衡向左移动
②在NH3?H2O中有平衡NH3+H2O![]() NH3?H2O
NH3?H2O![]() NH4++OH-,加NH4Cl使平衡向左移动
NH4++OH-,加NH4Cl使平衡向左移动
③NaOH溶于水时放热,使体系的温度升高,NH3的溶解度减小,会有部分NH3逸出
④NH4Cl与NaOH在此情况下可反应生成NH3,即NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
⑤NH4Cl会分解释放出NH3
(3)图甲中的NH4Cl与NaOH固体混合物能否用CaO固体代替?___(填“能”或“不能”)。
(4)如何判断图甲中烧瓶已收满NH3?________________________________________。
(5)图乙中胶头滴管中的水挤入烧瓶中,观察到的现象是_________,它说明了NH3__________。
查看习题详情和答案>>