摘要:C. 0.2molㄍL Na2S2O3和0.1molㄍL H2SO4溶液各5mL,加水10mL,反应温度30 0C
网址:http://m.1010jiajiao.com/timu_id_186904[举报]
盐酸、硫酸和硝酸是中学阶段常见的三种强酸.
Ⅰ.请就三者与金属铜的反应情况,回答下列问题:
(1)在100mL、18mol?L-1 的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准情况下的体积可能是
A.40.32L B.30.24L C.20.16L D.6.72L
(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是
A.0.1mol B.0.15mol C.0.2mol D.0.25mol
(3)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为
Ⅱ.用如下装置可以完成HCl的制取及后续一系列的性质实验(图中夹持装置已略去).
请回答下列问题:
(1)装置A选用浓硫酸和浓盐酸混合制取HCl气体,p中盛装试剂为
(2)装置B中的四处棉花依次做了如下处理:①包有某潮湿的固体物质 ②蘸有KI溶液③蘸有石蕊溶液 ④蘸有浓NaOH溶液.反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式
a.MnO2 b.KmnO4 C.KCl d.Cu
(3)在整个实验过程中,在③处能观察到的现象是
查看习题详情和答案>>
Ⅰ.请就三者与金属铜的反应情况,回答下列问题:
(1)在100mL、18mol?L-1 的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准情况下的体积可能是
D
D
A.40.32L B.30.24L C.20.16L D.6.72L
(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是
NO2、NO
NO2、NO
,反应中所消耗的硝酸的物质的量可能为B
B
.A.0.1mol B.0.15mol C.0.2mol D.0.25mol
(3)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为
Cu+H2O2+2HCl=CuCl2+2H2O
Cu+H2O2+2HCl=CuCl2+2H2O
.Ⅱ.用如下装置可以完成HCl的制取及后续一系列的性质实验(图中夹持装置已略去).

请回答下列问题:
(1)装置A选用浓硫酸和浓盐酸混合制取HCl气体,p中盛装试剂为
浓硫酸
浓硫酸
.(2)装置B中的四处棉花依次做了如下处理:①包有某潮湿的固体物质 ②蘸有KI溶液③蘸有石蕊溶液 ④蘸有浓NaOH溶液.反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式
CI2+2I-=2Cl-+I2
CI2+2I-=2Cl-+I2
.在①处包有的固体物质可能是a.MnO2 b.KmnO4 C.KCl d.Cu
(3)在整个实验过程中,在③处能观察到的现象是
先变红后褪色
先变红后褪色
.过量的硝酸和6.4g铜充分反应,向反应后的溶液中滴加5 mol·L-1的氢氧化钠溶液,加入氢氧化钠溶液的体积与生成沉淀的关系如图所示,则反应后溶液中所含NO3-的物质的量为
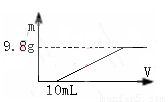
A.0.05mol B.0.1mol
C.0.2mol D.0.25mol
查看习题详情和答案>>
(12分)某研究性小组进行如下实验:常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
请回答:
(1)从①组情况分析,HA是强酸还是弱酸?__________(填“强酸”或“弱酸”)。
(2)②组情况表明,c____ 0.2mol/L(填﹥、﹤或=)。混合液中离子浓度c(A-) c(Na+)(填﹥、﹤或=)。
(3)从③组实验结果分析,说明HA的电离程度______NaA的水解程度 (填﹥、﹤或=),该混合溶液中离子浓度由大到小的顺序是_____ ___。
(4)①组实验所得混合溶液中由水电离出的c(OH-)=____________mol·L-1。
查看习题详情和答案>>