摘要:37.将98g质量分数为10%的硫酸跟一定质量的氢氧化钠溶液恰好完全反应.在得到的溶液中.硫酸钠的质量分数8%.试求:(1)硫酸钠溶液的质量,(2)氢氧化钠溶液中溶质的质量分数. (易)
网址:http://m.1010jiajiao.com/timu_id_18661[举报]
按要求填空:
(1)将80g质量分数为35%的浓盐酸,稀释成10%的稀盐酸,需加水的质量为
(2)简述在实验室如何稀释浓硫酸:
查看习题详情和答案>>
(1)将80g质量分数为35%的浓盐酸,稀释成10%的稀盐酸,需加水的质量为
200
200
g;(2)简述在实验室如何稀释浓硫酸:
将浓硫酸沿烧杯壁缓慢地注入水中,用玻璃棒不断搅动
将浓硫酸沿烧杯壁缓慢地注入水中,用玻璃棒不断搅动
.(1)欲将80g质量分数为20%的NaOH溶液稀释到质量分数为10%NaOH溶液,需要加水的质量为
(2)配制100mL溶质质量分数为20%的NaOH溶液,需NaOH质量
查看习题详情和答案>>
80
80
g,(2)配制100mL溶质质量分数为20%的NaOH溶液,需NaOH质量
22
22
g,水的质量88
88
g,(溶液密度为1.1g/mL).29、某校课外兴趣小组对一批粗锌样品进行分析
(1)他们先将100g质量分数为98%的硫酸稀释成19.6%的稀硫酸,需加水
(2)实验测得:15g粗锌和100g溶质质量分数为19.6%的稀硫酸恰好完全反应(粗锌中所含杂质不溶于水,也不参与反应),请你计算:
①15g粗锌的中锌的质量
②恰好完全反应时所得溶液的溶质质量分数(计算结果保留到0.1%)
查看习题详情和答案>>
(1)他们先将100g质量分数为98%的硫酸稀释成19.6%的稀硫酸,需加水
400
g;(2)实验测得:15g粗锌和100g溶质质量分数为19.6%的稀硫酸恰好完全反应(粗锌中所含杂质不溶于水,也不参与反应),请你计算:
①15g粗锌的中锌的质量
②恰好完全反应时所得溶液的溶质质量分数(计算结果保留到0.1%)
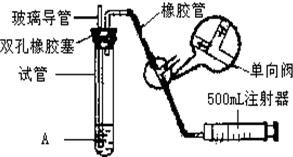 二氧化硫是大气污染物之一,为粗略地测定周围环境中的SO2含量,某学生课外活动小组设计了如图的实验装置.
二氧化硫是大气污染物之一,为粗略地测定周围环境中的SO2含量,某学生课外活动小组设计了如图的实验装置.表1 我国环境空气质量标准中对每次空气质量测定中的S02最高浓度限值
| S02最高浓度限值(单位mg?m-3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
向外轻轻拉动注射器的活塞
向外轻轻拉动注射器的活塞
(填写实验操作方法),将会看到浸没在水中的玻璃导管口有气泡冒出
浸没在水中的玻璃导管口有气泡冒出
(填写实验现象),则证明该装置的气密性良好.(2)已知二氧化硫与碘水的反应为:SO2+I2+2H2O═H2SO4+2HI.向试管中加入1.0mL溶质质量分数为1.27×10-4的碘水(此时溶液的密度与水的密度近似),用适量的蒸馏水稀释后再加入2-3滴淀粉溶液,配制成溶液A.测定指定地点的空气中SO2的含量时,推拉注射器的活塞反复抽气,A溶液由
蓝
蓝
色变为无
无
色时反应恰好完全进行.(3)课外活动小组分成第一小组和第二小组,使用相同的实验装置和溶液A,在同一地点、同时测量空气中的S02含量(两个小组所用时间相同、所用装置和药品均无问题).当反应恰好完全进行,记录抽气次数如下(假设每次抽气500mL).请将表填写完整(计算时保留二位有效数字).
表2 不同组别的测量值:
| 分组 | 第一小组 | 第二小组 |
| 抽气次数 | 120 | 140 |
| 空气中S02的含量(单位:mg?m-3) | 0.53 0.53 |
0.46 0.46 |
三级
三级
标准(填表3中所列举的等级),你认为第一
第一
小组(填“第一”或“第二”)小组的测定结果更接近实际值,原因是第二小组的抽气速度过快,造成空气中SO2与碘未充分反应,产生较大误差
第二小组的抽气速度过快,造成空气中SO2与碘未充分反应,产生较大误差
.