网址:http://m.1010jiajiao.com/timu_id_181209[举报]
一、 B 8.B 9.D 10.C 11.D 12.C 13.A
25.(14分)
(1)25%
(2)增大
(3)6
(4)41%
26.(14分)
(1)①铁屑 ②稀硫酸 ③稀硝酸 ④氢氧化钠 ⑤氢氧化钠
(2)Fe+2H+=Fe2++H2↑ 2Fe3++Fe=3Fe2+
Cu2++Fe=Cu+Fe2+ 2Au3++3Fe=2Au+3Fe2+
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(3)Fe2O3 用作红色涂料 用作制造铜盐的原料
27.(15分)
(1)2 10 8 5 2 1 8
(2)碱 KmnO4是强氧化剂,它会腐蚀乳胶管
(3)

(4)
①不一定准确 如果铁片中存在与稀硫酸反应并能生成氢气的其他金属,会导致结果偏高;铁片中存在与稀硫酸反应而溶解、但不产生氢气的铁的氧化物,会导致结果偏低;如果上述情况均不存在,则结果准确
②不一定准确 如果铁片中存在与稀硫酸反应而溶解的其他金属,生成的金属离子在酸性溶液中能被高锰酸钾氧化,会导致结果偏高;如果铁片中存在与稀硫酸反应而溶解的铁的氧化物,生成的Fe3+离子在酸性溶液中不能被高锰酸钾氧化,会导致结果偏低;如果上述情况均不存在,则结果准确
注:本小题属于开放性试题,若考生回答“准确”或“不准确”且理由合理,可酌性给分。例如:考生回答
方案一准确,因为铁片中不存在能与稀硫酸反应并能生成氢气的其他金属,也不存在铁的氧化物
方案一不准确,如果铁片中存在与稀硫酸反应生成氢气的其他金属,会导致结果偏高;如果存在与稀硫酸反应而溶解、但不产生氢气的铁的氧化物,会导致结果偏低
方案二准确,铁片溶于稀硫酸后,除Fe2+外,其他可能存在的金属离子在酸性溶液中均不能被高锰酸钾氧化,也不存在氧化铁
方案二不准确,如果铁片中存在与稀硫酸反应而溶解的其他金属,生成的金属离子在酸性溶液中能被高锰酸钾氧化,会导致结果偏高;如果存在与稀硫酸反应而溶解的铁的氧化物,千百万的Fe3+离子在酸性溶液中不能被高锰酸钾氧化,会导致结果偏低
34. [化学――选修化学与技术](15分)
(1)①造纸厂排放的碱性污水使X处河水pH升高,火力发电厂净化烟气的酸性废水治理未达标就排放,造成Y处等的河水,pH降低(或火力发电厂燃烧产生的SO2会导致酸雨,飘落后使Y处等的河水pH降低)
②化肥厂、农田及生活污水使Z处河水富营养化,水温较高,适于藻类等水生植物生长,河水中溶解氧被大量消耗,导致鱼类死亡
(2)①发电厂 焦化厂 炼铁厂 水泥厂
②Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
CaCO3+SiO2  CaSiO3+CO2
CaSiO3+CO2
③
用炼铁厂的炉渣(或CaSiO3)作为水泥厂的原料
用发电厂的煤矸石和粉煤灰作为水泥厂的原料
将石灰石煅烧成生石灰,用于吸收发电厂和焦化厂烯煤时产生的SO2,减少对空气的污染
建立污水处理系统
35. [化学――选修物质结构与性质](15分)
(1)S C
(2)V形 直线形 SO2 因为CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”原理,SO2在H2O中的溶解度较大
(3)Cr 四 1s22s22p63s23p63d54s1 +6
(4)F-H…F F-H…O O-H…F O-H…O
36. [化学――选修有机化学基础](15分)
(1)C6H8O7
(2)

(3)酯化反应

(4)

碳碳双键 羧基
酯基 羧基 (结构简式 分,官能团 分)
如写出下列结构简式和相应官能团,同样给分

酯基 羧基
羟基 羧基 酸酐基
羟基 羧基 酸酐基
羟基 羧基 碳碳双键 羰基
(12分)过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。请填写下列空白:
(1)取10.00 mL密度为dg/mL的过氧化氢溶液,稀释至250 mL后,取出25.00 mL溶液至锥形瓶中,加入稀硫酸酸化,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在横线上。
____MnO4- +____H2O2+____H+![]() ____Mn2++____H2O+___ ______
____Mn2++____H2O+___ ______
(3)滴定时,将高锰酸钾标准溶液注入_______(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是_____________________________________
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为_____________________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
查看习题详情和答案>>过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等.某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质.
下面是测定过氧化的含量的方法,请填写下列空白:
(1)移取10.00 mL密度为ρg/mL的过氧化氢溶液至250 mL________(填仪器名称)中,加水稀释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作为被测试样.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里.
![]()
(3)滴定时,将高锰酸钾标准溶液注入________(填“酸式”或“碱式”)滴定管中.滴定到达终点的现象是________.
(4)复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为________.
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果________(填“偏高”或“偏低”或“不变”).
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等.某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,请填写下列空白:
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250 mL________(填仪器名称)中,加水衡释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里.
________MnO4-+________H2O2+________H+=________Mn2++________H2O+________
(3)滴定时,将高锰酸钾标准溶液注入________(填“酸式”或“碱式”)滴定管中.滴定到达终点的现象是________.
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为________.
(5)下列操作能使测定结果偏高的是________
A.滴定前滴定管尖嘴中有气泡,滴定后气泡消失.
B.读取高锰酸钾标准溶液的刻度时,滴定前平视,滴定后俯视.
C.滴定前,在用蒸馏水洗涤滴定管后,未用高锰酸钾标准液润洗.
D.滴定过程中,锥形瓶中部分溶液溅出
(15分)
我国规定:室内甲醛含量不得超过0.08mg·m-3。某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛(HCHO)的含量。
【查阅资料】KMnO4( H+)溶液为强氧化剂,可氧化甲醛和草酸。
4MnO4―+5HCHO+H+=4Mn2++5CO2↑+11H2O
2MnO4―+5H2C2O4+6H+=2Mn2++10CO2 ↑+8H2O
【实验一】
按如图所示装置进行采样
(1)由图可知甲醛的物理性质为
(2)空气中甲醛采样吸收装置中用到的玻璃仪器为:玻璃导管、
(3)为了使通过吸收装置的甲醛尽可能被吸收液吸收,可采取的措施是:(只写出一种即可) 。
设置空气采集器为恒定流量0.5 L/min,采集20min。
【实验二】
量取10.00 mL 的甲醛吸收液转移到锥形瓶中,量取12.00 mL 1.00×10-3 mol·L-1 KMnO4溶液于锥形瓶中,并滴入几滴稀H2SO4备用。
(4)用1.00×10-3 mol·L-1标准草酸溶液进行滴定,当
时,达到滴定终点。
(5)记录滴定所消耗的草酸溶液的体积。重复实验2次,消耗草酸溶液的体积分别为10.90 mL、10.02 mL、9.98mL。计算该居室内空气中甲醛的浓度为 mg·m-3。
(6)若滴定过程中,发现滴定管下端开始有气泡,滴定后气泡消失,则测定结果将
(填“偏大”、“无影响”、“偏小”)
【实验三】
环境监测站工作人员采样后,将5.00 mL 的甲醛吸收液注入比色瓶中,再向比色瓶中注入显色试剂0.5 mL,盖紧瓶塞,摇匀,静置显色。当室内环境温度不同时,记录显色时间见下表。
| 环境温度/℃ | 5 | 10 | 15 | 20 | 25 | 30 | 35 |
| 显色时间/min | 45 | 30 | 15 | 13 | 10 | 7 | 5 |
(7)由该表可以得出的结论是
(8)请用化学反应原理解释
查看习题详情和答案>>
(15分)
我国规定:室内甲醛含量不得超过0.0 8mg·m-3。某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛(HCHO)的含量。
【查阅资料】KMnO4 ( H+)溶液为强氧化剂,可氧化甲醛和草酸。
4MnO4―+5HCHO+H+=4Mn2++5CO2↑+11H2O
2MnO4―+5H2C2O4+6H+=2Mn2++10CO2 ↑+8H2O
【实验一】
按如图所示装置进行采样
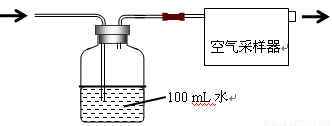
(1)由图可知甲醛的物理性质为
(2)空气中甲醛采样吸收装置中用到的玻璃仪器为:玻璃导管、
(3)为了使通过吸收装置的甲醛尽可能被吸收液吸收,可采取的措施是:(只写出一种即可) 。
设置空气采集器为恒定流量0.5 L/min,采集20min。
【实验二】
量取10.00 mL 的甲醛吸收液转移到锥形瓶中,量取12.00 mL 1.00×10-3 mol·L-1 KMnO4溶液于锥形瓶中,并滴入几滴稀H2SO4备用。
(4)用1.00×10-3 mol·L-1标准草酸溶液进行滴定,当
时,达到滴定终点。
(5)记录滴定所消耗的草酸溶液的体积。重复实验2次,消耗草酸溶液的体积分别为10.90 mL、10.02 mL、9.98 mL。计算该居室内空气中甲醛的浓度为 mg·m-3。
(6)若滴定过程中,发现滴定管下端开始有气泡,滴定后气泡消失,则测定结果将
(填“偏大”、“无影响”、“偏小”)
【实验三】
环境监测站工作人员采样后,将5.00 mL 的甲醛吸收液注入比色瓶中,再向比色瓶中注入显色试剂0.5 mL,盖紧瓶塞,摇匀,静置显色。当室内环境温度不同时,记录显色时间见下表。
|
环境温度/℃ |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
|
显色时间/min |
45 |
30 |
15 |
13 |
10 |
7 |
5 |
(7)由该表可以得出的结论是
(8)请用化学反应原理解释
查看习题详情和答案>>