网址:http://m.1010jiajiao.com/timu_id_179250[举报]
(共11分).某反应中反应物与生成物有: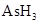 、
、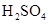 、
、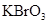 、
、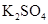 、
、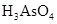 、
、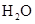 和一种未知物质X。(1)已知
和一种未知物质X。(1)已知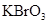 在反应中得到电子,则该反应的还原剂是
。(2)已知0.2mol
在反应中得到电子,则该反应的还原剂是
。(2)已知0.2mol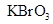 在反应中得到1mol电子生成X,则X的化学式为
。(3)根据上述反应可推知
。
在反应中得到1mol电子生成X,则X的化学式为
。(3)根据上述反应可推知
。
a.氧化性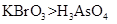 b.氧化性:
b.氧化性: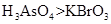
c.还原性: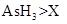 d.还原性:
d.还原性: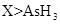
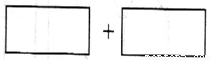
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:
查看习题详情和答案>>
(11分)某课外小组设计的实验室制取乙酸乙酯的装置如图14-2所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。

已知①无水氯化钙可与乙醇形成难溶于水的CaCl2·6 C2H50H ②有关有机物的沸点:
|
试剂 |
乙醚 |
乙醇 |
乙酸 |
乙酸乙酯 |
|
沸点/℃ |
34.7 |
78.5 |
118 |
77.1 |
请回答:
(1)浓硫酸的作用是 ;若用同位素180示踪法确定反应产物水分子中氧原子的提供者,写出能表示180位置的化学方程式: 。
(2)球形干燥管C的作用是 。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示) ;反应结束后D中的现象是 .
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出 (填物质名称);再加入(此空从下列选项中选择,填编号) ,然后进行蒸馏,收集77℃左右的馏分,以得较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
查看习题详情和答案>>
(共11分)某盐X由非金属元素组成,不稳定加热时分解,生成等物质的量的气态氢化物A和B。A、C、E、G、I含有同种元素,C为黄色固体单质。B、D、F、H、J含有同种元素,B可与J反应生成盐。W是前四周期含有4个未成对电子的金属。上述物质转化关系如图,部分产物和条件已略去。请回答下列问题:

(1)X的化学式
(2)写出由E生成G的化学反应方程式
(3)写出反应B+Y →D+Z的化学方程式
(4)由E直接转换成I可以加入 (填写两种属于不同类别的物质)。
(5)标况下,4.48LA与J的浓溶液反应转移1.6mole-,写出此反应的离子方程式 。
(6)将1mol/L200mL I和1mol/L100mL J溶液混合,加入到含有0.5mol的W中,则产生气体的物质的量为
查看习题详情和答案>>