网址:http://m.1010jiajiao.com/timu_id_159096[举报]
1.D 2.D 3.B 4.D 5.D 6.B 7.A 8.C
9.C 10.AB 11.D 12.C 13.C 14.C
15.(1)检验反应中生成的H2 (2分)
(2)Fe Fe3O4溶于盐酸生成的Fe3+ 与Fe反应生成了Fe2+ (2分)
(3)① 2Fe2++2H++H2O2=2Fe3++2H2O (2分)
②取少量最后一次洗涤液,滴加AgNO3溶液,若无沉淀生成,表明沉淀已洗涤干净 (2分)
③固体样品质量和红褐色固体的质量 (2分)
(本题共10分,其它合理答案参照给分)
 (3)相同温度下,K2SO4 的溶解度小于KCl、(NH4)2SO4
及NH4Cl
(3)相同温度下,K2SO4 的溶解度小于KCl、(NH4)2SO4
及NH4Cl
(4)CaO、H2O 或Ca(OH)2
(5) 原子利用率高,没有有害物质排放到环境中 (每空2分,共10分)
19.(1)  (2)酸性KMnO4溶液 (3) 3
(2)酸性KMnO4溶液 (3) 3
(4) 
 |
(5)
(6) 
 (每空2分,共12分)
(每空2分,共12分)
20.(1) (C6H10O5)n+nH2O 3nCH4↑+3nCO2↑ (2分)
(2)9.20 (
(3) 设反应③中消耗O2的物质的量为x,则N2的物质的量为4x
2CH4+O2→4H2+2CO CH4 + H2O → 3H2 + CO
2x x 4x 2x 1×103-2x (1×103-2x)×3 (1×103-2x)
合成二甲醚反应中CO和H2为1∶2,合成氨反应中,N2与H2体积比为1∶3,则
4x+(1×103-2x)×3-[2x+(1×103-2x)]×2=4x×3 (3分,关系式)
x=1000/14 mol
NH3
:4x×2×17=
答略。(本题共10分,其它合理答案参照给分)
21.(1) 1s22s22p63s23p63d54s2 (2分)
Mn2+的3d轨道电子排布为半满状态较稳定 (2分)
(2) 直线型 (2分) CO2 (2分)
(3) 1:2 (1分)  (1分) 30 (2分)
(1分) 30 (2分)
本资料由《七彩教育网》www.7caiedu.cn 提供!

(1)从反应开始到达第一次平衡时的平均速率v(A)为
(2)根据上图数据,写出该反应的化学方程式
(3)在5~7min内,若K值不变,则此处曲线变化的原因是
(4)下图2表示此反应的反应速率v和时间t的关系图,根据上图判断,在t3和t5时刻改变的外界条件分别是
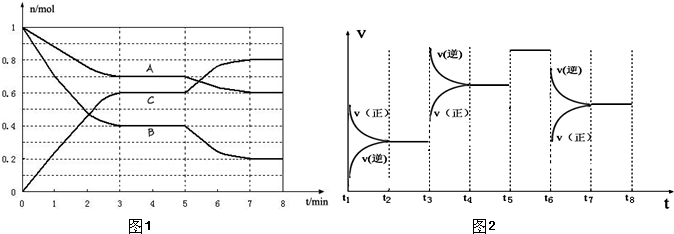
(1)根据图1数据,写出该反应的化学方程式______;此反应的平衡常数表达式K=______.从反应开始到达第一次平衡时的平均速率v(A)为______.
(2)在5~7min内,若K值不变,则此处曲线变化的原因是______.
(3)图2表示此反应的反应速率v和时间t的关系图.
各阶段的平衡常数如下表所示:
| t2~t3 | t4~t5 | t5~t6 | t7~t8 |
| K1 | K2 | K3 | K4 |
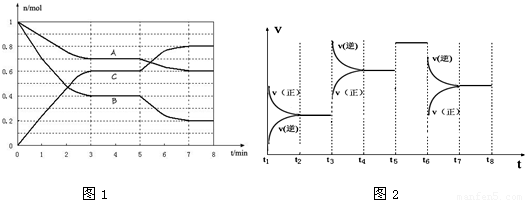
(1)从反应开始到达第一次平衡时的平均速率v(A)为______.
(2)根据上图数据,写出该反应的化学方程式______;求出此反应在25℃的平衡常数K=______(保留2位小数).
(3)在5~7min内,若K值不变,则此处曲线变化的原因是______.
(4)下图2表示此反应的反应速率v和时间t的关系图,根据上图判断,在t3和t5时刻改变的外界条件分别是______和______;A的转化率最大的一段时间是______.
查看习题详情和答案>>

(1)根据图1数据,写出该反应的化学方程式 ;此反应的平衡常数表达式K= .从反应开始到达第一次平衡时的平均速率v(A)为 .
(2)在5~7min内,若K值不变,则此处曲线变化的原因是 .
(3)图2表示此反应的反应速率v和时间t的关系图.
各阶段的平衡常数如下表所示:
| t2~t3 | t4~t5 | t5~t6 | t7~t8 |
| K1 | K2 | K3 | K4 |

(1)根据图1请写出合成氨的热化学方程式
(2)图1中虚线部分是通过改变化学反应条件是
(3)当反应达到平衡位置时不断改变条件(不改变N2、H2和NH3的量),图2表示反应速率随时间的关系,其中表示平衡混合物中NH3的含量最高的时间段是
(4)在一定温度压强下,下列各项能作为判断该反应达到化学平衡状态的依据是
a.单位时间内生成2n molNH3的同时生成n molN2 b.容器内压强不再改变
c.容器内N2、H2、NH3的浓度之比为1:3:2 d.混合气体的密度不再改变
e.混合气体的平均相对分子质量不再改变 f.2v正(H2)=3v正(NH3)
(5)在一定温度下,若将4a mol H2和2amol N2放入2L的密闭容器中,充分反应后测得N2的转化率为50%,则该反应的平衡常数为
| 16 |
| a2 |
| 16 |
| a2 |