网址:http://m.1010jiajiao.com/timu_id_127367[举报]
(15分) 某研究性学习小组为确定某碱式碳酸镁样品的组成,设计出了下图所示的实验装置(图中A至D的部分)。[已知碱式碳酸镁Mgx(OH)y(CO3)z(x、y、z为正整数)加热能分解生成氧化镁、水和二氧化碳]
(1)按上图(夹持仪器未画出)组装好实验装置后,应首先进行的操作是_____________;A处干燥管盛放的药品是_____________,其作用是____________________________。
(2)指导老师在审阅设计方案后指出需要在E处进行改进,请你帮助该小组设计出改进方案:____________________________________。
(3)加热前需要进行的必要操作是__________________________________,其目的是____________________________________;对活塞的操作方法是:关闭活塞 ________,打开活塞________。
(4)通过什么现象能够说明碱式碳酸镁分解完全____________________________。
(5)待B装置中的反应完全后,打开K1,再缓缓鼓入空气数分钟,其目的是________________________。
(6)实验测得数据如下:碱式碳酸镁样品22.6 g;反应前C装置的质量为87.6 g,反应后质量为89.4 g;反应前D装置的质量为74.7 g,反应后质量为83.5 g。请计算推导该碱式碳酸镁的化学式___________________________,该碱式碳酸镁受热分解的化学方程式为 。
查看习题详情和答案>>
(15分) 某研究性学习小组为确定某碱式碳酸镁样品的组成,设计出了下图所示的实验装置(图中A至D的部分)。[已知碱式碳酸镁Mgx(OH)y(CO3)z(x、y、z为正整数)加热能分解生成氧化镁、水和二氧化碳]
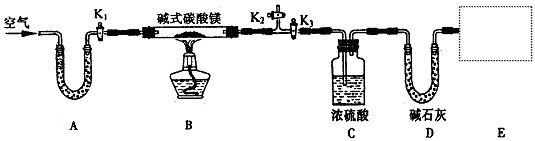
(1)按上图(夹持仪器未画出)组装好实验装置后,应首先进行的操作是_____________;A处干燥管盛放的药品是_____________,其作用是____________________________。
(2)指导老师在审阅设计方案后指出需要在E处进行改进,请你帮助该小组设计出改进方案:____________________________________。
(3)加热前需要进行的必要操作是__________________________________,其目的是____________________________________;对活塞的操作方法是:关闭活塞 ________,打开活塞________。
(4)通过什么现象能够说明碱式碳酸镁分解完全____________________________。
(5)待B装置中的反应完全后,打开K1,再缓缓鼓入空气数分钟,其目的是________________________。
(6)实验测得数据如下:碱式碳酸镁样品22.6 g;反应前C装置的质量为87.6 g,反应后质量为89.4 g;反应前D装置的质量为74.7 g,反应后质量为83.5 g。请计算推导该碱式碳酸镁的化学式___________________________,该碱式碳酸镁受热分解的化学方程式为 。
查看习题详情和答案>>
(1)2KClO3(s)![]() 2KCl(s)+3O2(g) ΔH=-78.03 kJ·mol-1 ΔS=1 110 J·mol-1·K-1
2KCl(s)+3O2(g) ΔH=-78.03 kJ·mol-1 ΔS=1 110 J·mol-1·K-1
(2)CO(g)![]() C(s,石墨)+
C(s,石墨)+![]() O2(g) ΔH=110.5 kJ·mol-1 ΔS=-89.36 J·mol-1·K-1
O2(g) ΔH=110.5 kJ·mol-1 ΔS=-89.36 J·mol-1·K-1
(3)4Fe(OH)2(s)+2H2O(l)+O2(g) ![]() 4Fe(OH)3(s) ΔH=-444.3 kJ·mol-1 ΔS=-280.1 J·mol-1·K-1
4Fe(OH)3(s) ΔH=-444.3 kJ·mol-1 ΔS=-280.1 J·mol-1·K-1
(4)NH4HCO3(s)+CH3COOH(aq)![]() CO2(g)+CH3COONH4(aq)+H2O(l)
CO2(g)+CH3COONH4(aq)+H2O(l)
ΔH=37.301 kJ·mol-1 ΔS=184.05 J·mol-1·K-1
(5)KCl(s) ![]() K+(aq)+Cl-(aq) ΔH=17.1 kJ·mol-1 ΔS=75.9 J·mol-1·K-1
K+(aq)+Cl-(aq) ΔH=17.1 kJ·mol-1 ΔS=75.9 J·mol-1·K-1
(6)2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) ΔH=-113.0 kJ·mol-1 ΔS=-145.3 J·mol-1·K-1
N2(g)+2CO2(g) ΔH=-113.0 kJ·mol-1 ΔS=-145.3 J·mol-1·K-1
(每空格3分,计15分)某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)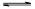 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。
实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度 (×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A.
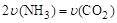 B.密闭容器中总压强不变
B.密闭容器中总压强不变C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,计算25.0℃时的分解平衡常数:__________________________。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量____ __(填“增加”、“减小”或“不变”)。
④氨基甲酸铵分解反应的焓变△H__ __0,熵变△S__ _0(填>、<或=)。 查看习题详情和答案>>
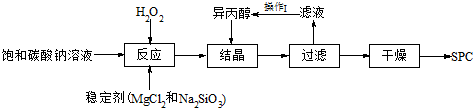
(1)反应的最佳温度控制在15℃~20℃,温度偏高时造成产率低的可能原因有
(2)操作Ⅰ的名称为
(3)加入异丙醇的作用是
(4)过碳酸钠的化学式可表示为aNa2CO3?bH2O2.现将一定质量的过碳酸钠粉末配成稀溶液,再向其中加入适量MnO2粉末,完全反应后生成672mL气体(标准状况).反应后的混合物经过滤、洗涤后,将滤液和洗涤液混合并加水配成100mL溶液A.现向体积为10mL、浓度为cmol?L-1的稀硫酸中逐滴滴入溶液A,边滴边振荡,充分反应后,测得实验数据如下表所示:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ | IV |
| 滴加溶液A的体积/mL | 5.0 | 10.0 | 15.0 | 20.0 |
| 生成气体的体积/mL(标准状况) | 44.8 | 89.6 | 89.6 | 89.6 |