摘要:(或 或 )
网址:http://m.1010jiajiao.com/timu_id_115131[举报]
(2011?上海模拟)烯烃通过臭氧氧化并经锌和水处理得到醛或酮,例如:
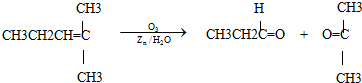
一种链状单烯烃A通过臭氧氧化并经锌和水处理得到B和C.化合物B含碳69.8%,含氢11.6%,B无银镜反应.D在浓硫酸存在下加热,可得到能使溴水褪色且只有一种结构的物质E.G的分子式为C7H14O2C7H14O2.有关转化关系如下;
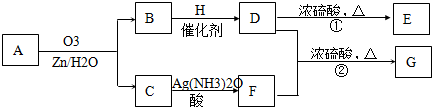
(1)B的相对分子质量是
(2)写出结构简式:A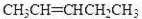
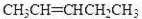 .
.
(3)写出反应①、②的反应类型:①
(4)写出反应②的化学方程式: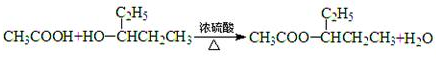
 .
.
(5)F的一种同分异构体能发生酯化反应和银镜反应,其结构简式为
查看习题详情和答案>>
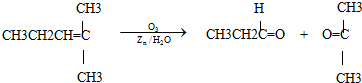
一种链状单烯烃A通过臭氧氧化并经锌和水处理得到B和C.化合物B含碳69.8%,含氢11.6%,B无银镜反应.D在浓硫酸存在下加热,可得到能使溴水褪色且只有一种结构的物质E.G的分子式为C7H14O2C7H14O2.有关转化关系如下;

(1)B的相对分子质量是
86
86
.(2)写出结构简式:A
(CH3CH2)2C=CHCH2CH3
(CH3CH2)2C=CHCH2CH3
、E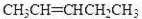
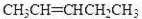
(3)写出反应①、②的反应类型:①
消去反应
消去反应
、②酯化反应
酯化反应
.(4)写出反应②的化学方程式:


(5)F的一种同分异构体能发生酯化反应和银镜反应,其结构简式为
HOCH2CHO
HOCH2CHO
.(一)括号中的物质是杂质,写出除去这些杂质的试剂:
(1)MgO (Al2O3)
(3)FeCl3(FeCl2)
(二)海水中含有大量的氯化镁,从海水中提取镁的生产流程如图1所示:
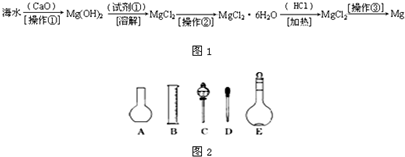
回答下列问题:
写出在海水中加入氧化钙生成氢氧化镁的化学方程式
操作①主要是指
(三)实验室配制480ml 0.1mol?L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体
(2)如图2所示的仪器配制溶液肯定不需要的是
(3)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的
(4)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是
(5)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了
(6)若实验时遇到下列情况,将使溶液的浓度偏低的是
A.配制前设有将容量瓶中的水除尽; B.碳酸钠失去了部分结晶水;
C.碳酸钠晶体不纯,其中混有氯化钠; D.称量碳酸钠晶体时所用砝码生锈; E.定容时仰视刻度线.
查看习题详情和答案>>
(1)MgO (Al2O3)
NaOH溶液
NaOH溶液
(2)Cl2(HCl)饱和NaCl溶液
饱和NaCl溶液
(3)FeCl3(FeCl2)
氯气或氯水
氯气或氯水
(4)NaHCO3溶液(Na2CO3)CO2
CO2
(二)海水中含有大量的氯化镁,从海水中提取镁的生产流程如图1所示:

回答下列问题:
写出在海水中加入氧化钙生成氢氧化镁的化学方程式
CaO+MgCl2+H2O=Mg(OH)2+CaCl2
CaO+MgCl2+H2O=Mg(OH)2+CaCl2
;操作①主要是指
过滤
过滤
;试剂①可选用HCl
HCl
;操作②是指蒸发浓缩,冷却结晶,过滤
蒸发浓缩,冷却结晶,过滤
;经操作③最终可得金属镁.(三)实验室配制480ml 0.1mol?L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体
14.3
14.3
g.(2)如图2所示的仪器配制溶液肯定不需要的是
AC
AC
(填序号),本实验所需玻璃仪器E规格为500
500
mL.(3)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的
①③⑤
①③⑤
.(填数字符号)(4)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是
dbac
dbac
.(填写字母,每种仪器只能选择一次)(5)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了
2
2
种用途.(填写数字)(6)若实验时遇到下列情况,将使溶液的浓度偏低的是
CE
CE
.A.配制前设有将容量瓶中的水除尽; B.碳酸钠失去了部分结晶水;
C.碳酸钠晶体不纯,其中混有氯化钠; D.称量碳酸钠晶体时所用砝码生锈; E.定容时仰视刻度线.
(2008?上海)某反应体系中的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O.
(1)请将Au2O3之外的反应物与生成物分别填入以下空格并配平.
+
(2)反应中1mol还原剂
(3)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂和氧化剂物质的量之比为
查看习题详情和答案>>
(1)请将Au2O3之外的反应物与生成物分别填入以下空格并配平.
+
4Na2S2O3
4Na2S2O3
+2H2O
2H2O
=Au2O
Au2O
+2Na2S4O6
2Na2S4O6
+4NaOH
4NaOH
(2)反应中1mol还原剂
失去
失去
(填“得到”或“失去”)1
1
mol电子.(3)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂和氧化剂物质的量之比为
1:4
1:4
.(2011?淮安二模)过硼酸钠是一种优良的漂白剂,被广泛应用于洗衣粉、漂白粉、洗涤剂中.以硼砂(主要成为Na2B4O7)为原料生产过硼酸钠晶体的主要流程如下:

(1)由Na2B4O7和NaOH反应制NaBO2的离子方程式为
(2)沉淀A中含有酸不溶物和氢氧化镁杂质,为了分离出氢氧化镁,在沉淀中加过量的酸,过滤得到含Mg2+的滤液,再在滤液加入碱使Mg2+形成氢氧化镁.若加碱前溶液中c(Mg2+)=0.056mol?L-1,那么需调节溶液的pH=
(3)已知纯品过硼酸钠晶体中各元素的物质的量比为:n(Na):n(B):n(H):n(O)=1:1:n:7.将制得的纯品样品在
70℃以上加热将逐步失去结晶水,测得纯品质量随温度的变化如右图所示,则T3时所得晶体的化学式为

(4)若反应温度控制不当,所得的过硼酸钠晶体中将混有NaBO2,则产品中钠的质量分数
查看习题详情和答案>>

(1)由Na2B4O7和NaOH反应制NaBO2的离子方程式为
B4O72-+2OH-=4BO2-+H2O
B4O72-+2OH-=4BO2-+H2O
;(2)沉淀A中含有酸不溶物和氢氧化镁杂质,为了分离出氢氧化镁,在沉淀中加过量的酸,过滤得到含Mg2+的滤液,再在滤液加入碱使Mg2+形成氢氧化镁.若加碱前溶液中c(Mg2+)=0.056mol?L-1,那么需调节溶液的pH=
9
9
时,才开始出现沉淀.[已知25℃下Mg(OH)2的Ksp=5.6×10-12](3)已知纯品过硼酸钠晶体中各元素的物质的量比为:n(Na):n(B):n(H):n(O)=1:1:n:7.将制得的纯品样品在
70℃以上加热将逐步失去结晶水,测得纯品质量随温度的变化如右图所示,则T3时所得晶体的化学式为
NaBO3?H2O
NaBO3?H2O
.(书写简单计算过程)
(4)若反应温度控制不当,所得的过硼酸钠晶体中将混有NaBO2,则产品中钠的质量分数
升高
升高
(填“升高”、“降低”或“不变”).