摘要:C.平衡混合气中G的质量分数学科网
网址:http://m.1010jiajiao.com/timu_id_114357[举报]
Ⅰ、CO和H2的混合气体俗称合成气,是一种重要的工业原料气,焦炭、天然气(主要成分为CH4)、重油、煤在高温下均可与水蒸气反应制得合成气.
(1)已知某反应的平衡常数表达式为:K=
,它所对应的化学方程式为:______.
(2)向体积为2L的密闭容器中充入CH4和H2O(g)组成的混合气(共1mol),在一定条件下发生反应,并达到平衡状态,测得温度、压强、投料比X〔
)对该反应的影响如图所示.

①图1中的两条曲线所示投料比的关系X2______X1(填“=”“>”或“<”下同)
②图2中两条曲线所示的压强比的关系:P2______P1
(3)以CH4、O2为原料可设计成燃料电池:
①设装置中盛有150.0mL1.0mol/LKOH溶液,放电时参与反应的氧气在标准状况下的体积为4.48L,放电过程中转移电子的物质的量为______.
②以H2SO4溶液代替KOH溶液为电解质溶液,则燃料电池的负极反应式为:______.
Ⅱ、(1)有一种用CO2生产甲醇燃料的方法:
已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-akJ?mol-1;
CH3OH(g)═CH3OH(l)△H=-bkJ?mol-1;
2H2(g)+O2(g)═2H2O(g)△H=-ckJ?mol-1;
H2O(g)═H2O(l)△H=-dkJ?mol-1,
则表示CH3OH(l)燃烧热的热化学方程式为:______.
(2)已知某温度下Mg(OH)2的Ksp=6.4xl0-12,当溶液中c(Mg2+)≤1.0×10-5mol?L-1可视为沉淀完全,则应保持溶液中c(OH-)≥______mol?L-1.
查看习题详情和答案>>
(1)已知某反应的平衡常数表达式为:K=
| c(H2)?c(CO) |
| c(H2O) |
(2)向体积为2L的密闭容器中充入CH4和H2O(g)组成的混合气(共1mol),在一定条件下发生反应,并达到平衡状态,测得温度、压强、投料比X〔
| n(CH4) |
| n(H2O) |

①图1中的两条曲线所示投料比的关系X2______X1(填“=”“>”或“<”下同)
②图2中两条曲线所示的压强比的关系:P2______P1
(3)以CH4、O2为原料可设计成燃料电池:
①设装置中盛有150.0mL1.0mol/LKOH溶液,放电时参与反应的氧气在标准状况下的体积为4.48L,放电过程中转移电子的物质的量为______.
②以H2SO4溶液代替KOH溶液为电解质溶液,则燃料电池的负极反应式为:______.
Ⅱ、(1)有一种用CO2生产甲醇燃料的方法:
已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-akJ?mol-1;
CH3OH(g)═CH3OH(l)△H=-bkJ?mol-1;
2H2(g)+O2(g)═2H2O(g)△H=-ckJ?mol-1;
H2O(g)═H2O(l)△H=-dkJ?mol-1,
则表示CH3OH(l)燃烧热的热化学方程式为:______.
(2)已知某温度下Mg(OH)2的Ksp=6.4xl0-12,当溶液中c(Mg2+)≤1.0×10-5mol?L-1可视为沉淀完全,则应保持溶液中c(OH-)≥______mol?L-1.
A、B、C、D、E、F、G是原子序数依次增大的短周期元素,其中A与E、D与G同主族,且D与G核内质子数之和是A与E核内质子数之和的2倍,A与B、C、D可分别形成10电子分子,E、F、G元素最高价氧化物对应水化物之间可相互发生反应,请回答下列问题
(1)E、G两种元素的符号:E
(2)Zn与稀硫酸反应需加入少量硫酸铜溶液反应速率会大大加快,其原理是
(3)E在D2中燃烧生成化合物X中阴阳离子个数比为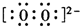
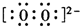 .
.
(4)能够说明可逆反应2CD2(g) C2D4(g)达到平衡状态的标志是
C2D4(g)达到平衡状态的标志是
①单位时间消耗2mol CD2的同时,生成1mol C2D4
②恒温恒压下,混合气体的密度不变
③CD2和C2D4的浓度之比为2:1
④混合气体的颜色不变
⑤单位时间消耗4mol CD2的同时,消耗2mol C2D4
(5)向含E的最高价氧化物的水化物0.5mol的水溶液中通入标况下BD2气体11.2L,其化学反应方程式为
查看习题详情和答案>>
(1)E、G两种元素的符号:E
Na
Na
、GS
S
;F在元素周期表中的位置是第三周期第ⅢA族
第三周期第ⅢA族
.(2)Zn与稀硫酸反应需加入少量硫酸铜溶液反应速率会大大加快,其原理是
发生反应Zn+CuSO4═ZnSO4+Cu,形成铜锌-硫酸原电池,反应速率加快
发生反应Zn+CuSO4═ZnSO4+Cu,形成铜锌-硫酸原电池,反应速率加快
.(3)E在D2中燃烧生成化合物X中阴阳离子个数比为
1:2
1:2
;X中的阴离子电子式为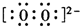
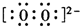
(4)能够说明可逆反应2CD2(g)
 C2D4(g)达到平衡状态的标志是
C2D4(g)达到平衡状态的标志是②④⑤
②④⑤
;①单位时间消耗2mol CD2的同时,生成1mol C2D4
②恒温恒压下,混合气体的密度不变
③CD2和C2D4的浓度之比为2:1
④混合气体的颜色不变
⑤单位时间消耗4mol CD2的同时,消耗2mol C2D4
(5)向含E的最高价氧化物的水化物0.5mol的水溶液中通入标况下BD2气体11.2L,其化学反应方程式为
NaOH+CO2=NaHCO3
NaOH+CO2=NaHCO3
. A、B、C、D、E、F、G是原子序数依次增大的短周期元素,其中A与E、D与G同主族,且D与G核内质子数之和是A与E核内质子数之和的2倍,A与B、C、D可分别形成10电子分子,E、F、G元素最高价氧化物对应水化物之间可相互发生反应,请回答下列问题
(1)E、G两种元素的符号:E 、G ;F在元素周期表中的位置是 .
(2)Zn与稀硫酸反应需加入少量硫酸铜溶液反应速率会大大加快,其原理是 。
(3) E在D2中燃烧生成化合物X中阴阳离子个数比为 ;X中的阴离子电子式为 .
(4)能够说明可逆反应2CD2(g) 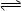 C2D4(g)达到平衡状态的标志是 ;
C2D4(g)达到平衡状态的标志是 ;
①单位时间消耗2mol CD2的同时,生成1 mol C2D4②恒温恒压下,混合气体的密度不变③CD2和C2D4的浓度之比为2∶1 ④混合气体的颜色不变⑤单位时间消耗4mol CD2的同时,消耗2mol C2D4
(5)向含E的最高价氧化物的水化物0.5 mol的水溶液中通入标况下BD2气体11.2L,其化学反应方程式为 。
A、B、C、D、E、F、G是原子序数依次增大的短周期元素,其中A与E、D与G同主族,且D与G核内质子数之和是A与E核内质子数之和的2倍,A与B、C、D可分别形成10电子分子,E、F、G元素最高价氧化物对应水化物之间可相互发生反应,请回答下列问题
(1)E、G两种元素的符号:E______、G______;F在元素周期表中的位置是______.
(2)Zn与稀硫酸反应需加入少量硫酸铜溶液反应速率会大大加快,其原理是______.
(3)E在D2中燃烧生成化合物X中阴阳离子个数比为______;X中的阴离子电子式为______.
(4)能够说明可逆反应2CD2(g)

C2D4(g)达到平衡状态的标志是______;
①单位时间消耗2mol CD2的同时,生成1mol C2D4
②恒温恒压下,混合气体的密度不变
③CD2和C2D4的浓度之比为2:1
④混合气体的颜色不变
⑤单位时间消耗4mol CD2的同时,消耗2mol C2D4
(5)向含E的最高价氧化物的水化物0.5mol的水溶液中通入标况下BD2气体11.2L,其化学反应方程式为______.
查看习题详情和答案>>
(1)E、G两种元素的符号:E______、G______;F在元素周期表中的位置是______.
(2)Zn与稀硫酸反应需加入少量硫酸铜溶液反应速率会大大加快,其原理是______.
(3)E在D2中燃烧生成化合物X中阴阳离子个数比为______;X中的阴离子电子式为______.
(4)能够说明可逆反应2CD2(g)

C2D4(g)达到平衡状态的标志是______;
①单位时间消耗2mol CD2的同时,生成1mol C2D4
②恒温恒压下,混合气体的密度不变
③CD2和C2D4的浓度之比为2:1
④混合气体的颜色不变
⑤单位时间消耗4mol CD2的同时,消耗2mol C2D4
(5)向含E的最高价氧化物的水化物0.5mol的水溶液中通入标况下BD2气体11.2L,其化学反应方程式为______.
A、B、C、D、E、F、G是原子序数依次增大的短周期元素,其中A与E、D与G同主族,且D与G核内质子数之和是A与E核内质子数之和的2倍,A与B、C、D可分别形成10电子分子,E、F、G元素最高价氧化物对应水化物之间可相互发生反应,请回答下列问题
(1)E、G两种元素的符号:E______、G______;F在元素周期表中的位置是______.
(2)Zn与稀硫酸反应需加入少量硫酸铜溶液反应速率会大大加快,其原理是______.
(3)E在D2中燃烧生成化合物X中阴阳离子个数比为______;X中的阴离子电子式为______.
(4)能够说明可逆反应2CD2(g) C2D4(g)达到平衡状态的标志是______;
C2D4(g)达到平衡状态的标志是______;
①单位时间消耗2mol CD2的同时,生成1mol C2D4
②恒温恒压下,混合气体的密度不变
③CD2和C2D4的浓度之比为2:1
④混合气体的颜色不变
⑤单位时间消耗4mol CD2的同时,消耗2mol C2D4
(5)向含E的最高价氧化物的水化物0.5mol的水溶液中通入标况下BD2气体11.2L,其化学反应方程式为______.
查看习题详情和答案>>
(1)E、G两种元素的符号:E______、G______;F在元素周期表中的位置是______.
(2)Zn与稀硫酸反应需加入少量硫酸铜溶液反应速率会大大加快,其原理是______.
(3)E在D2中燃烧生成化合物X中阴阳离子个数比为______;X中的阴离子电子式为______.
(4)能够说明可逆反应2CD2(g)
 C2D4(g)达到平衡状态的标志是______;
C2D4(g)达到平衡状态的标志是______;①单位时间消耗2mol CD2的同时,生成1mol C2D4
②恒温恒压下,混合气体的密度不变
③CD2和C2D4的浓度之比为2:1
④混合气体的颜色不变
⑤单位时间消耗4mol CD2的同时,消耗2mol C2D4
(5)向含E的最高价氧化物的水化物0.5mol的水溶液中通入标况下BD2气体11.2L,其化学反应方程式为______.
查看习题详情和答案>>