网址:http://m.1010jiajiao.com/timu_id_10534[举报]
一、我会选择
1. A 2. B 3. C 4. A 5. B 6. A
7. B 8. A 9. C 10. B 11. C 12. D
13. C 14. B 15. D 16. D
二、我会填空
17. (1)
(2)
(3) 置换反应
置换反应
18. ① ② ②③
19. (1)N
H C (2)
20. ①二氧化硫 ②金刚石 ③烧碱 ④水
21. 红色在液体中慢慢扩散
构成红墨水的微粒不停运动,扩散到液体中 小
构成物质的微粒间有间隔
*22. (1)B (2)26.5%
*23. (1)盐 +3 (2)D (3)D
*24. (1)0 (2)C、H、O (3)
(4)
三、我会实验
25. (1)③ (2)① (3)④ (4)②
26. (1)铜
(2)金属表面由红色变成黑色 
(3)蓝
27. A 反应物为固体,需加热 D 氧气不易溶于水
*28. [查阅资料]:能与水反应;能与 反应
反应
[实验]:
A:检验二氧化硫气体,吸收二氧化硫将其除去,消除对二氧化碳检验的干扰;
B:检验二氧化硫是否除尽。
A:溶液紫色褪去(或溶液褪色,或颜色变浅);
C:澄清的石灰水变浑浊。
[结论与讨论]:将混合气体先通过高锰酸钾溶液检验并吸收二氧化硫气体;再通过高锰酸钾溶液检验二氧化硫气体是否被除尽,最后将气体导入澄清石灰水中检验二氧化碳气体的存在。
[应用]:熟石灰的悬浊液 熟石灰与高锰酸钾相比成本较低,熟石灰的悬浊液比澄清的石灰水含溶质多,吸收效率高。
四、我会计算
29. (1)31 (2)192:12:28:16 (3)11.3%
*30. (1)解:漂白粉中主要成分的质量:
(2)解:设所需 的质量为x
的质量为x

(3)氯
答:略
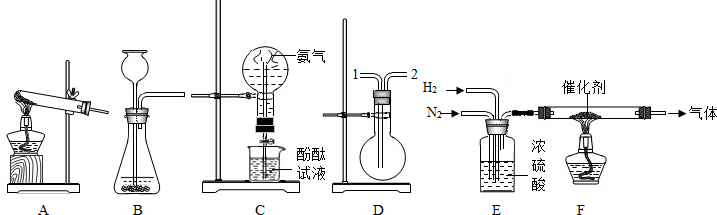
(1)将熟石灰与氯化铵混合加热可以用于制备氨气,请从上图中选择装置
(2)装置C 能够形成红色的喷泉,这说明了氨气具有
(3)实验室模拟合成氨的实验中,先将氮气和氢气通过E装置,E装置的作用除了使氢气和氮气气流稳定以及使气体充分混合外,还有
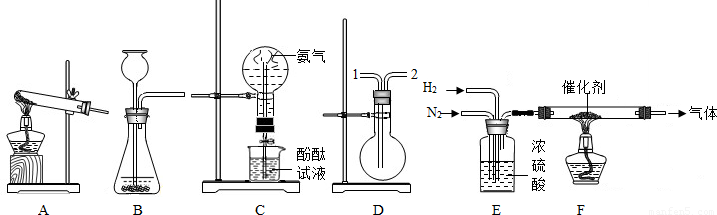
(1)将熟石灰与氯化铵混合加热可以用于制备氨气,请从上图中选择装置______用于制备该气体,试管中的化学反应是(填写化学方程式)______ CaCl2+2H2O+2NH3↑ 查看习题详情和答案>>

(2)装置C 能够形成红色的喷泉,这说明了氨气具有 、 的性质。
(3)实验室模拟合成氨的实验中,先将氮气和氢气通过E装置,E装置的作用除了使氢气和氮气气流稳定以及使气体充分混合外,还有 的作用;装置F用于合成氨,铂丝作为催化剂可反复使用,这是因为 。
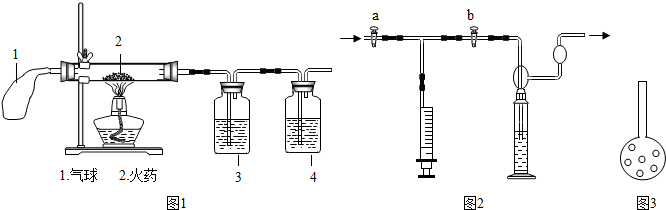
[提出问题]烟花爆竹燃放时会产生什么气体?
[查阅资料]我国传统的黑火药的标准配方为:硝酸钾75%、硫磺l0%、木炭l5%,因为黑火药中的硫磺成分具有着火温度低、燃速快等性质,因而使黑火药容易点火,使得在生产过程中硫的使用量过大.
(2)CO2和SO2均能使石灰水变浑浊;
[猜想]烟花爆竹燃放时会产生CO2和SO2
[实验过程]他们设计的实验探究过程如图1实验开始前应先检查
[实验反思]
(1)装置中气球的作用是
(2)已知 硬质玻璃管中发生的反应有S+2KNO3+3C═3CO2+N2+X,则X的化学式为
| ||
| ||
[查阅资料]可用含有一定量碘的溶液测定空气中的SO2含量,反应方程式是:SO2+I2+2H2O=H2SO4+2HI.
[测定装置]:甲同学设计了如图2所示的实验装置:
[测定步骤]:
(一) 配制一定浓度的稀碘溶液
(二)二氧化硫含量的测定
(1)将一定浓度、一定质量的稀碘溶液放于洗气瓶中,并滴入几滴稀淀粉溶液,此时洗瓶中溶液的颜色为蓝色.(淀粉遇碘单质呈蓝色)
(2)3位同学分别设计好的装置来到燃放点,打开a,关闭b用注射器抽取100mL燃放点空气.再关闭a,打开b,再缓缓推动注射器,将气体全部推入滴有淀粉的碘水溶液中,重复上述操作多次,直到溶液刚好变成无色,记录抽气的次数
(3)3位同学使溶液刚好变成无色时抽气的次数分别为50、60、65次,
(4)最终我们通过计算可以确定燃放点的二氧化硫含量是否超标.
[测定反思]
(1)小明经过思考后认为在测定时可将图3所示的多孔球泡放入洗气瓶中,你认为加此仪器的好处是
(2)小强同学认为:实验方案需要抽气的次数太多,操作麻烦.与小亮讨论后,决定对设计的实验加以调整,以减少抽气的次数,他们调整的方案可能是
(3)三位同学经过对烟花爆竹的研究,明白了国家“禁放”的和“限放”的原因,你认为原因的是
A 减少噪声污染 B 减少固体废弃物污染 C 减少大气污染 D 减少粉尘污染.
【查阅资料】碳酸钙:白色粉末,20℃溶解度为0.0065g,水溶液的pH 值为9.5~10.2,空气饱和碳酸钙水溶液的pH 值为8.0~8.6;
碱式碳酸铜:绿色粉末状固体,俗称铜绿;20℃溶解度为0.0008g,其水溶液pH值约为7;
碳酸氢铵:白色粉状固体,溶解度受温度影响较大,20℃时溶解度为21.7g,溶液pH值约为8.
【猜想一】三种碳酸盐是否都能使酚酞变色,不同温度下变色情况是否不同?
【设计方案】
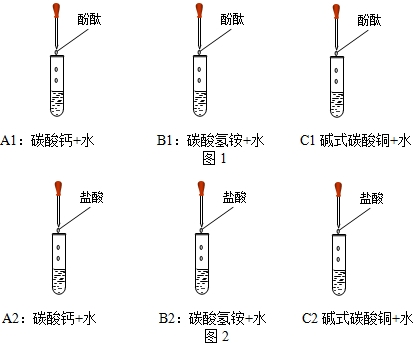
(1)小敏在三个试管中分别加入碳酸钙、碳酸氢铵、碱式碳酸铜,然后分别加入蒸馏水,振荡,滴加酚酞(如图1所示),发现A1试管内变红,B1试管内淡红色,C1试管内不红,说明碳酸钙水溶液的碱性
(2)小芳也做同样的实验,她在试管内加入铜绿,再加蒸馏水,发现试管内马上变红,请你帮她分析原因可能是
(3)小敏继续把上述三个试管放入装有80℃热水的烧杯中,(如图1)发现B1试管内产生密集的气泡,并闻到
| ||
| ||
(4)小芳另取一定量的碳酸氢铵固体,放置在小烧杯中,用开水直接浇注在烧杯中,观察到烧杯中迅速产生大量的气泡并且连液体一起溢出烧杯.碳酸氢铵开水浇注比水浴加热反应更快的原因是:
【猜想二】三种碳酸盐是否都能与盐酸反应?
【设计方案】
(1)小敏另取三个试管,分别加入少量碳酸钙、碳酸氢铵、碱式碳酸铜,用胶头滴管逐滴滴加稀盐酸,(如图2所示)发现三种物质都能和稀盐酸反应.试管C2中现象为
【反思与评价】三种碳酸盐都能与盐酸反应,但并不都能使酚酞变红.