题目内容
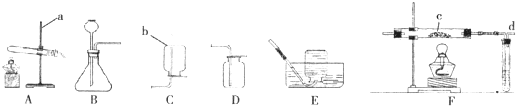
实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并探究氨气性质.查阅资料得到氨气的一些性质:无色、有刺激性气味的气体,比空气轻;易液化得液氨;极易溶于水.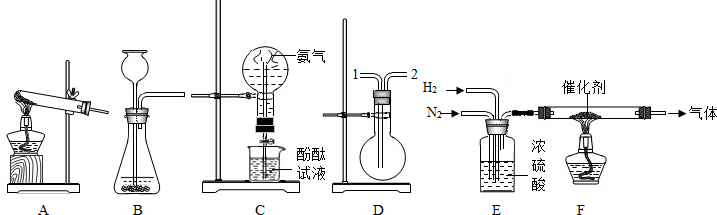
(1)将熟石灰与氯化铵混合加热可以用于制备氨气,请从上图中选择装置
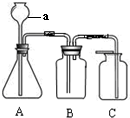
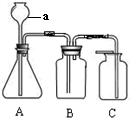
(2)装置C 能够形成红色的喷泉,这说明了氨气具有
(3)实验室模拟合成氨的实验中,先将氮气和氢气通过E装置,E装置的作用除了使氢气和氮气气流稳定以及使气体充分混合外,还有
分析:(1)根据题意:熟石灰与氯化铵混合加热可以用于制备氨气.可知是加热反应.据此选择实验发生装置.然后根据反应物是熟石灰和氯化铵,反应条件是加热,写出化学反应式即可.再根据氨气比空气轻的特点,可知用D装置收集氨气时从2端进入;
(2)C装置中能够形成红色喷泉,是因为氨气溶于水后,在大气压的作用下烧杯中的酚酞试液上升,形成喷泉.又因为酚酞试液遇碱变红,说明氨气溶于水后,水溶液显碱性;我们可以据此填写答案;
(3)根据E装置中有浓硫酸,可知E装置还有干燥气体的作用;根据催化剂的作用可以知道催化剂的铂丝在反应前后的变化.
(2)C装置中能够形成红色喷泉,是因为氨气溶于水后,在大气压的作用下烧杯中的酚酞试液上升,形成喷泉.又因为酚酞试液遇碱变红,说明氨气溶于水后,水溶液显碱性;我们可以据此填写答案;
(3)根据E装置中有浓硫酸,可知E装置还有干燥气体的作用;根据催化剂的作用可以知道催化剂的铂丝在反应前后的变化.
解答:解:(1)熟石灰与氯化铵混合加热可以用于制备氨气,可知是加热反应,所以应选A作为发生装置;根据反应物是熟石灰和氯化铵,反应条件是加热,可知反应方程式是:Ca(OH)2+2NH4Cl
CaCl2+2H2O+2NH3↑;又因为氨气比空气轻,所以用装置D收集氨气时应从2端进.故答案为:A、Ca(OH)2+2NH4Cl
CaCl2+2H2O+2NH3↑、2;
(2)C装置中能够形成红色喷泉,是因为氨气溶于水后,装置中的压强变小,在外界大气压的作用下烧杯中的酚酞试液上升,形成喷泉.又酚酞试液遇碱变红,C装置中的红色喷泉是因为氨气溶于水后,形成碱性溶液的缘故.故答案为:易溶于水、水溶液显碱性;
(3)E装置中有浓硫酸,浓硫酸具有很强的吸水性,所以E装置可以用来干燥气体或吸收水分;催化剂可以增大反应的速率,但本身的化学性质和质量在反应前后都没有发生变化.所以作为催化剂的铂丝,可以反复使用.故答案为:干燥气体或吸收水、反应前后质量和化学性质均不变.
| ||
| ||
(2)C装置中能够形成红色喷泉,是因为氨气溶于水后,装置中的压强变小,在外界大气压的作用下烧杯中的酚酞试液上升,形成喷泉.又酚酞试液遇碱变红,C装置中的红色喷泉是因为氨气溶于水后,形成碱性溶液的缘故.故答案为:易溶于水、水溶液显碱性;
(3)E装置中有浓硫酸,浓硫酸具有很强的吸水性,所以E装置可以用来干燥气体或吸收水分;催化剂可以增大反应的速率,但本身的化学性质和质量在反应前后都没有发生变化.所以作为催化剂的铂丝,可以反复使用.故答案为:干燥气体或吸收水、反应前后质量和化学性质均不变.
点评:本题主要考查实验装置的选取、化学方程式的书写和反应中的现象,需要同学们掌握牢靠的基础知识.同时要同学们了解催化剂的定义.

练习册系列答案
相关题目