0 34486 34494 34500 34504 34510 34512 34516 34522 34524 34530 34536 34540 34542 34546 34552 34554 34560 34564 34566 34570 34572 34576 34578 34580 34581 34582 34584 34585 34586 34588 34590 34594 34596 34600 34602 34606 34612 34614 34620 34624 34626 34630 34636 34642 34644 34650 34654 34656 34662 34666 34672 34680 447348
 1996年诺贝化学奖授予对发现C60有重大贡献的三位科学家.C60分子是形如球状的多面体(如图13),该结构的建立基于以下考虑:
1996年诺贝化学奖授予对发现C60有重大贡献的三位科学家.C60分子是形如球状的多面体(如图13),该结构的建立基于以下考虑: 13
13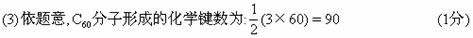

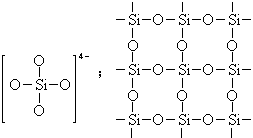
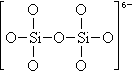 下图是石英晶体平面示意图(如图12),它实际上是立体的网状结构,其中硅、氧原子数之比为____。原硅酸根离子SiO44-的结构可表示为二聚硅酸根离子Si2O76-中,只有硅氧键,它的结构可表示 为__________。(96年 29题4分)
下图是石英晶体平面示意图(如图12),它实际上是立体的网状结构,其中硅、氧原子数之比为____。原硅酸根离子SiO44-的结构可表示为二聚硅酸根离子Si2O76-中,只有硅氧键,它的结构可表示 为__________。(96年 29题4分)