0 31282 31290 31296 31300 31306 31308 31312 31318 31320 31326 31332 31336 31338 31342 31348 31350 31356 31360 31362 31366 31368 31372 31374 31376 31377 31378 31380 31381 31382 31384 31386 31390 31392 31396 31398 31402 31408 31410 31416 31420 31422 31426 31432 31438 31440 31446 31450 31452 31458 31462 31468 31476 447348


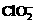 )。饮用水中ClO2、
)。饮用水中ClO2、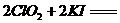
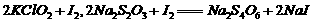 ,则步骤4中加入的指示剂为 ,滴定达到终点时溶液的颜色变化为
,则步骤4中加入的指示剂为 ,滴定达到终点时溶液的颜色变化为
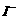 将溶液中的
将溶液中的 还原为
还原为 以测定其含量,该反应的离子方程式为:
以测定其含量,该反应的离子方程式为: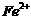 将
将 ③ 用硫酸铜晶体和氢氧化钠溶液制取氧化铜 ④ 测定某溶液的pH
③ 用硫酸铜晶体和氢氧化钠溶液制取氧化铜 ④ 测定某溶液的pH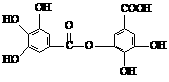 (1)1molA最多可与
mol NaOH反应。
(1)1molA最多可与
mol NaOH反应。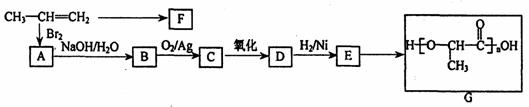 18.(8分)工业上由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。
18.(8分)工业上由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。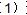
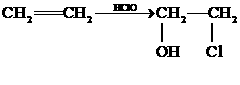
 mol/L B.
mol/L B.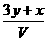 mol/L C.
mol/L C.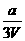 mol/L D.无法计算
mol/L D.无法计算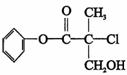 A.有机物A 属于芳香烃
B.有机物A 可以与Br2的CCl4溶液发生加成反应
A.有机物A 属于芳香烃
B.有机物A 可以与Br2的CCl4溶液发生加成反应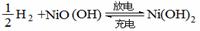 池的总反应为 。据此判断,下列叙述中正确的是
池的总反应为 。据此判断,下列叙述中正确的是  白磷在高压下隔绝空气加热后急速冷却,可得钢灰色固体--黑磷,其转化过程如下:
白磷在高压下隔绝空气加热后急速冷却,可得钢灰色固体--黑磷,其转化过程如下: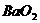 (过氧化钡)固体中的阴离子和阳离子之比为2∶1
(过氧化钡)固体中的阴离子和阳离子之比为2∶1