27、(15分)
⑴用某种方法制得的碳纳米管中常含有杂质 - 碳纳米颗粒。这种碳纳米颗粒可用氧化气化法除去,其反应体系有反应物、生成物共七种:C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3、H2O。
①写出该反应的化学方程式:
②上述反应中生成0.1mol还原产物时,转移电子的物质的量是 mol;
③由单质与氧气反应生成11g上述反应中的氧化产物时,放出热量98.375kJ,写出相应的热化学方程式
⑵控制变量是科学研究中的重要研究方法,其基本思路是,在实验研究中人为只改变一个因素(调节变量),其他因素保持相同,观察温室因调节变量改变的因素(因变量),从而分析得到研究结论。中学化学中应用控制变量的方法研究问题的例子很多。请分析或设计:
①在研究浓度对化学反应的影响时,教材安排了利用Na2S2O3与H2SO4反应的一组对照实验
(Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O)
|
烧杯编号 |
加3%Na2S2O3溶液体积(ml) |
加H2O体积(ml) |
加(体积比为1:20)H2SO4溶液体积(ml) |
所需时间(s) |
|
1 |
5 |
5 |
2 |
|
|
2 |
7 |
3 |
2 |
|
|
3 |
10 |
0 |
2 |
|
在三个烧杯(底部有黑色“+”字标记)内分别加入表中所示体积的三种液体,搅拌并开始计时,到出现混浊使烧杯底部“+”字看不见时停止计时。比较所需时间,得出浓度对化学反应速率影响的结论。实验中,温度和反应体系中硫酸浓度是保持相同的因素,调节变量是 ,因变量是
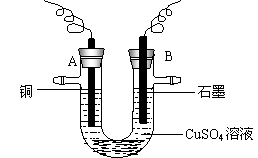 ②运用控制变量原理设计实验,利用纯碱溶液探究温度对盐的水解的影响,简述实验方法:
②运用控制变量原理设计实验,利用纯碱溶液探究温度对盐的水解的影响,简述实验方法:
 如图所示,质量为M=1㎏的平板小车上放置着m1=6㎏,m2=2㎏的物块,两物块与小车间动摩擦因数为μ=0.5。两物块间夹有一压缩轻质弹簧,物块间有张紧的轻绳相连。小车右端有与m2相连的锁定开关,现已锁定。水平地面光滑,物块均可视为质点。现将轻绳烧断,若已知m1相对小车滑过0.4m时从车上脱落,此时小车以速度v0=6m/s抽右运动,当小车第一次与墙壁瞬间锁定开关打开。设小车与墙壁碰撞前后速度大小不变,碰撞时间极短,小车足够长。(g=10m/s2)。求
如图所示,质量为M=1㎏的平板小车上放置着m1=6㎏,m2=2㎏的物块,两物块与小车间动摩擦因数为μ=0.5。两物块间夹有一压缩轻质弹簧,物块间有张紧的轻绳相连。小车右端有与m2相连的锁定开关,现已锁定。水平地面光滑,物块均可视为质点。现将轻绳烧断,若已知m1相对小车滑过0.4m时从车上脱落,此时小车以速度v0=6m/s抽右运动,当小车第一次与墙壁瞬间锁定开关打开。设小车与墙壁碰撞前后速度大小不变,碰撞时间极短,小车足够长。(g=10m/s2)。求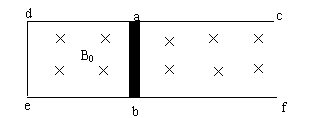
 ⑴滑块到达C点时的速度多大?
⑴滑块到达C点时的速度多大? (17分)
(17分) F、电键
F、电键 如图所示,质量为M,长为L的木排,停在静水中。质量为m1和m2的两个人从木排两端由静止开始同时向对方运动,当质量m1的人到达木排另一端时,另一人恰到达木排中间。不计水的阻力,则关于此过程中木排的位移x的说法正确的是
如图所示,质量为M,长为L的木排,停在静水中。质量为m1和m2的两个人从木排两端由静止开始同时向对方运动,当质量m1的人到达木排另一端时,另一人恰到达木排中间。不计水的阻力,则关于此过程中木排的位移x的说法正确的是
 面积均为S的两个电阻相同的线圈,分别放在如图所示的磁场中,甲图中的是磁感应强度为B0的匀强磁场,线圈在磁场中以周期T绕OOˊ轴匀速转动,乙图中的磁场变化规律为B=B0cos2πt/T,从图示位置开始计时,则
面积均为S的两个电阻相同的线圈,分别放在如图所示的磁场中,甲图中的是磁感应强度为B0的匀强磁场,线圈在磁场中以周期T绕OOˊ轴匀速转动,乙图中的磁场变化规律为B=B0cos2πt/T,从图示位置开始计时,则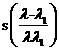 B、
B、  C、
C、 D、
D、