31、(6分)小兵和小东是某校化学研究性学习小组的成员,他们在查阅资料时,发现单质碳能够在高温时与金属氧化物反应得到金属单质。于是,他们用木炭与CuO进行了如下的探究活动。请你参与他们的这次活动,并解决的关问题:
[提出问题]
木碳与氧化铜反应除生成单质铜外,另一种生成物是什么?
[猜想与假设]
(1)可能是CO。(2)可能是CO2。
[设计实验方案]
(1)检验CO2的方法是(用化学方程式表示) 。
(2)为了检验CO,他们设计的方案是:把小动物放在收集的气体中,观察能否存活。后经充分研究后,认为此方案不可行,其不可行的理由是 。
 他们在互联网上用Google收集到这样一条信息:把滤纸浸泡在磷钼酸和氯化钯的黄色混合溶液中制成的试纸遇CO立即变成蓝色,而遇CO2不变色。
他们在互联网上用Google收集到这样一条信息:把滤纸浸泡在磷钼酸和氯化钯的黄色混合溶液中制成的试纸遇CO立即变成蓝色,而遇CO2不变色。
[实验与结论]设计的实验装置图如下:
|
实验现象 |
实验结论 |
|
A中固体由黑色变成红色 |
有
生成 |
|
B中黄色试纸没有变蓝 |
没有
生成 |
|
C中 |
有CO2生成 |
[反思与评价]
如果A装置中的试管口高于试管底部,在实验过程中可能造成的后果是
。

30.(4分)研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探险究,以下是他们探究的主要过程:
[假设]H2O2生成O2的快慢与催化剂的种类有关
[实验方案]常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量的MnO2和红砖粉,测量各成一瓶(相同体积)O2所需要的时间。
|
实验编号 |
1 |
2 |
|
反应物 |
6%
H2O2 |
6%
H2O2 |
|
催化剂 |
1g红砖粉 |
1g MnO2 |
|
时间 |
152s |
35s |
[实验记录]
[结论]该探究过程得出的结论是________________________________。
[反思]H2O2在常温下分角缓慢,别入MnO2或红砖粉后反应明显加快,若要证明MnO2和红砖粉是该反应的催化剂,还需要增加实验证明它们在化学反应前后的________ ________________是否改变。
H2O2生成O2的快慢还与哪些因素有关?请你帮助他们继续探究。(只要求提出假设和实验方案)
[假设]________________________________。
[实验方案]________________________________________________。
 ,相关实验数据如下图所示:
,相关实验数据如下图所示: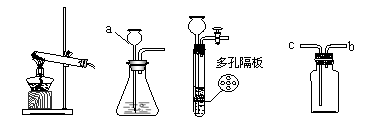

 N2↑+ Cl2↑+ 2O2↑+ aX。请回答下列问题:
N2↑+ Cl2↑+ 2O2↑+ aX。请回答下列问题: (5分)元素周期表是学习化学的重要工具。元素周期表能够反映元素原子结构的许多信息,原子结构与元素的性质和物质的组成有关。请根据元素周期表中钙元素的“身份证”(见右图),填写以下各图中横线上的空白。
(5分)元素周期表是学习化学的重要工具。元素周期表能够反映元素原子结构的许多信息,原子结构与元素的性质和物质的组成有关。请根据元素周期表中钙元素的“身份证”(见右图),填写以下各图中横线上的空白。 