摘要:向某NaOH溶液中逐滴加入稀H2SO4.则溶液的pH与所加的稀H2SO4的体积图像正确的是: A. B. C. D. pH pH pH pH 7 7 7 7 V V V V
网址:http://m.1010jiajiao.com/timu3_id_98737[举报]
(2012?建邺区一模)某化学兴趣小组的同学对“硫酸、硝酸钡、氢氧化钠、碳酸钠”四种物质之间的反应进行了定性和定量的研究.
根据复分解反应发生的条件,初步判断上述四种溶液两两之间能发生
(1)
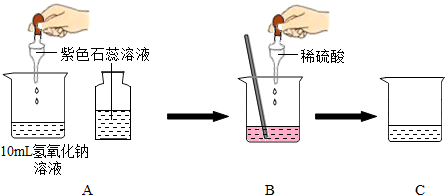
实验一:证明氢氧化钠溶液和稀硫酸混合后确实发生了化学反应王同学按如图方法进行了实验.请回答:在A的实验中,滴入紫色石蕊溶液的目的是
B装置中发生的化学反应方程式为
实验二:定量分析稀硫酸与两种混合物反应后溶液的成分刘同学称取38.2g氢氧化钠和碳酸钠的混合溶液于烧杯中,向其中逐滴滴加质量分数为15.3%的稀硫酸,同时记录实验数据,
测得加入稀硫酸的质量与生成气体的质量关系如图所示.
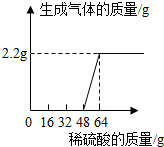
①当加入16g稀硫酸时,溶液中的溶质为
②求混合物与稀硫酸恰好完全反应时所得溶液的溶质质量分数.(请写出计算过程,结果保留到0.1%)
实验三:实验分析四种化合物溶液混合后的成分洪同学按以下流程进行了实验:
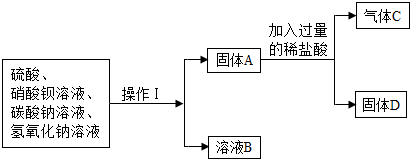
操作Ⅰ的名称是
查看习题详情和答案>>

根据复分解反应发生的条件,初步判断上述四种溶液两两之间能发生
4
4
个反应;其中有气体、沉淀生成的化学方程式为:(请各写出一个)(1)
Na2CO3+H2SO4═Na2SO4+CO2↑+H2O
Na2CO3+H2SO4═Na2SO4+CO2↑+H2O
;(2)H2SO4+Ba(NO3)2═BaSO4↓+2HNO3
H2SO4+Ba(NO3)2═BaSO4↓+2HNO3
.实验一:证明氢氧化钠溶液和稀硫酸混合后确实发生了化学反应王同学按如图方法进行了实验.请回答:在A的实验中,滴入紫色石蕊溶液的目的是
指示反应的进行
指示反应的进行
;B装置中发生的化学反应方程式为
2NaOH+H2SO4═Na2SO4+2H2O
2NaOH+H2SO4═Na2SO4+2H2O
;实验二:定量分析稀硫酸与两种混合物反应后溶液的成分刘同学称取38.2g氢氧化钠和碳酸钠的混合溶液于烧杯中,向其中逐滴滴加质量分数为15.3%的稀硫酸,同时记录实验数据,
测得加入稀硫酸的质量与生成气体的质量关系如图所示.

①当加入16g稀硫酸时,溶液中的溶质为
NaOH,Na2SO4,Na2CO3
NaOH,Na2SO4,Na2CO3
(写化学式)②求混合物与稀硫酸恰好完全反应时所得溶液的溶质质量分数.(请写出计算过程,结果保留到0.1%)
实验三:实验分析四种化合物溶液混合后的成分洪同学按以下流程进行了实验:

操作Ⅰ的名称是
过滤
过滤
,固体D的化学式是BaSO4
BaSO4
;如溶液B中滴入酚酞,呈无色,则B中一定没有OH- CO32-
OH- CO32-
离子;一定含有Na+ NO3-
Na+ NO3-
离子. (2005?绵阳)(1)硫酸亚铁是一种重要的化工原料,可用作杀虫剂、净水剂和木材防腐剂,还可用来治疗缺铁性贫血.工业上用废铁屑与稀硫酸反应制硫酸亚铁,主要反应的化学方程式为
(2005?绵阳)(1)硫酸亚铁是一种重要的化工原料,可用作杀虫剂、净水剂和木材防腐剂,还可用来治疗缺铁性贫血.工业上用废铁屑与稀硫酸反应制硫酸亚铁,主要反应的化学方程式为Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
.废铁屑与硫酸反应产生的气体中含有有毒气体H2S,用CuSO4溶液可以吸收这种气体并产生黑色沉淀,该反应的化学方程式为
H2S+CuSO4═CuS↓+H2SO4
H2S+CuSO4═CuS↓+H2SO4
.(2)为了探究CO的还原性,某同学将绕成螺旋状的铜丝放在酒精灯上加热至铜丝变黑后,立即将铜丝伸入盛满CO的集气瓶中(内装适量澄清石灰水),铜丝又恢复光亮的红色,振荡集气瓶,还可以看到集气瓶中
石灰水变浑浊
石灰水变浑浊
.上述实验过程中,能表明CO具有还原性的反应的化学方程式是
CuO+CO
Cu+CO2
| ||
CuO+CO
Cu+CO2
.将上述表面变黑的铜丝冷却后放入稀硫酸中,可以看到的现象是
| ||
黑色固体逐渐消失
黑色固体逐渐消失
溶液由无色变成蓝色
溶液由无色变成蓝色
,CuO+H2SO4=CuSO4+H2O
CuO+H2SO4=CuSO4+H2O
.(3)一包白色固体可能含有NaCl、CuSO4、NH4NO3、BaC12、K2 C O3中的一种或几种.有同学进行下列实验来确定该固体的成分:
(a)取少许固体放入试管,加入NaOH浓溶液并微热,把湿润的红色石蕊试纸放在试管口,试纸变为蓝色.
(b)取一些白色固体放入试管加水溶解,得无色透明溶液.
(c)向实验b所得溶液中滴2滴酚酞试液,溶液变为红色,再向其中加入过量CaC12溶液,红色褪去,产生白色沉淀.
(d)将实验c所得溶液中的沉淀滤去,向滤液中加入AgNO3溶液,又产生白色沉淀.
①根据以上实验现象判断:这包白色固体中一定有
NH4NO3、K2CO3
NH4NO3、K2CO3
,肯定没有CuSO4、BaC12
CuSO4、BaC12
.②若用这包白色固体配成稀溶液来浇花,可产生的作用是
AC
AC
(填下列选项的字母序号).A.促进花草的茎、叶生长茂盛,叶色浓绿
B.促进花草的根系发达,增强抗寒抗旱能力
C.促进花草生长健壮,茎杆粗硬,增强对病虫害和倒伏的抵抗能力
(4)实验室需用20%的稀硫酸(密度为1.14g?cm-3)460mL,若用如图标签所示的硫酸来配制,则至少需用这种硫酸
58.2
58.2
mL.
(2011?静安区二模)在研究酸和碱化学性质时,某小组同学想证明:稀硫酸与氢氧化钠溶液混合后,虽然仍为无色溶液,但确实发生了化学反应.请与他们一起完成实验方案的设计、实施和评价.
[演示实验]向装有一定量氢氧化钠溶液的试管中滴加几滴酚酞溶液,再滴加稀硫酸,并不断振荡溶液,若观察到
[交流评价]请你评价上述两组由实验现象获得的结论是否正确,并说明理由.
方案①:
方案②:
[拓展实验]取一定量的稀硫酸,逐滴匀速滴加氢氧化钠溶液,测得反应过程中pH变化(
20℃)如图所示:从0→t1时,溶液的酸碱性变化情况是
查看习题详情和答案>>
[演示实验]向装有一定量氢氧化钠溶液的试管中滴加几滴酚酞溶液,再滴加稀硫酸,并不断振荡溶液,若观察到
红色消失
红色消失
(实验现象),则证明氢氧化钠溶液与稀硫酸发生了化学反应,反应的化学方程式为H2SO4+2NaOH=Na2SO4+2H2O;
H2SO4+2NaOH=Na2SO4+2H2O;
.[提出问题]是否可以用其他实验方法证明稀硫酸与氢氧化钠溶液能发生反应呢?| 学生探究 | 实验过程 | 实验现象 | 结论 |
| 方案① |  |
加入氢氧化钠溶液后,温度明显上升. | 测量温度变化可以证明稀硫酸与氢氧化钠溶液能发生反应 |
| 方案② |  |
出现白色沉淀 | 用氯化钡溶液可以证明稀硫酸与氢氧化钠溶液能发生反应 |

方案①:
正确,中和反应放热,如果温度升高,则可证明稀硫酸与氢氧化钠溶液能发生反应
正确,中和反应放热,如果温度升高,则可证明稀硫酸与氢氧化钠溶液能发生反应
.方案②:
错误,因为氢氧化钠与硫酸反应与否都不影响硫酸钡白色沉淀的生成
错误,因为氢氧化钠与硫酸反应与否都不影响硫酸钡白色沉淀的生成
.[拓展实验]取一定量的稀硫酸,逐滴匀速滴加氢氧化钠溶液,测得反应过程中pH变化(
20℃)如图所示:从0→t1时,溶液的酸碱性变化情况是
溶液酸性不断减弱,t1时变为中性
溶液酸性不断减弱,t1时变为中性
.由图示分析,稀硫酸与氢氧化钠溶液发生反应的依据是溶液PH增大,t1时PH=7
溶液PH增大,t1时PH=7
.当加入氢氧化钠溶液到t2时,所得溶液中的溶质为(写化学式)Na2SO4和NaOH
Na2SO4和NaOH
.