网址:http://m.1010jiajiao.com/timu3_id_97611[举报]
 碱式碳酸镁密度小,是橡胶制品的优良填料.其组成一般以xMgCO3?yMg(OH)2?zH2O表示.
碱式碳酸镁密度小,是橡胶制品的优良填料.其组成一般以xMgCO3?yMg(OH)2?zH2O表示.【探究一】碱式碳酸镁的制备
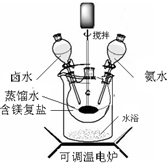
碱式碳酸镁可用复盐MgCO3?(NH4)2CO3?H2O作原料制备.取一定量的该复盐放入三颈烧瓶中,并将三颈烧瓶放在恒温水浴锅中加热(如图所示),按一定的液固比加入蒸馏水,开启搅拌器同时加入预定的氨水,待温度到达 40℃时开始分解,此时滴加卤水(氯化镁溶液)并继续滴入氨水,保持10分钟,一段时间后过滤洗涤,滤出的固体在120℃干燥得到碱式碳酸镁产品.
回答下列问题:
(1)①搅拌的目的是
(2)所得碱式碳酸镁产品中常检出有少量Cl-,其原因是混有
(3)设计实验检验碱式碳酸镁中含有Cl-
| 实验操作 | 实验现象 | 实验结论 |
| ①取样溶解,向样品溶液中滴加过量稀硝酸. ②再向上述所得溶液加 硝酸银或AgNO3 硝酸银或AgNO3 溶液 |
现象① 产生气泡 产生气泡 ;现象② 产生白色沉淀 产生白色沉淀 ; |
含有 Cl- |
300℃
已知:碱式碳酸镁分解反应方程式为:xMgCO3?yMg(OH)2?zH2O
| ||
探究小组利用下图测定xMgCO3?yMg(OH)2?zH2O组成.
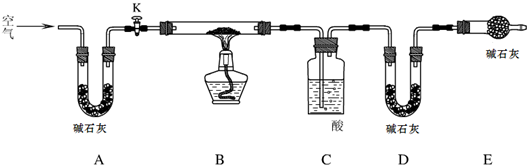
实验步骤:
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中.
步骤2:打开活塞K,鼓入空气,一段时间后关闭,称量相关装置的质量.
步骤3:加热装置B直至装置C中无气泡产生.
步骤4:
步骤5:称量相关装置的质量.
某同学在实验过程中采集了如下数据:
A.反应前玻璃管的质量100.0g
B.反应后玻璃管与残留固体总质量120.0g
C.装置C实验后增重9.0g
D.装置D实验后增重17.6g
回答下列问题:
(1)检查整套实验装置气密性的方法如下:将装置A的左端、装置E的右端分别接上导管,放入盛有水的烧杯中,
(2)如果没有装置A,则测定得到的Z值
装置C中的酸为
(3)根据实验测定的数据,求出碱式碳酸铜(xMgCO3?yMg(OH)2?zH2O)
中x:y:z=
【交流反思】
(4)如果不称量装置C实验前后的增重,要根据实验数据,求出x:y:z的值,还可测量的实验数据是
乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属.乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体.
[提出问题]白色固体是什么物质?
[做出猜想]小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二:________;猜想三:Ca(OH)2.
他的依据是________.
[交流反思]经过同学们交流讨论,认为猜想一不成立.否定猜想一的理由是:________.
[进行实验]
(一)取少量白色固体放入试管中,滴加稀盐酸,没有观察到________,证明猜想二不成立.
(二)取少量白色固体加入到水中,取上层清液,________,有白色沉淀出现,证明猜想三成立.该反应的化学方程式为:________.
结论:白色固体是Ca(OH)2.
[拓展应用]已知碳化钙与水反应非常剧烈,乙炔的密度比空气略小.实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置是________(选填图中装置序号).

乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体。
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二: ;猜想三:Ca(OH)2。
他的依据是 。
【交流反思】经过同学们交流讨论,认为猜想一不成立。否定猜想一的理由是:
。
【进行实验】(一)取少量白色固体放入试管中,滴加稀盐酸,没有观察到 ,证明猜想二不成立。
(二)取少量白色固体加入到水中,取上层清液, ,有白色沉淀出现,证明猜想三成立。该反应的化学方程式为: 。结论:白色固体是Ca(OH)2。
【拓展应用】1、已知碳化钙与水反应非常剧烈,乙炔的密度比空气略小。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置是 (选填图中装置序号)。
A B C D E F
2、写出乙炔在空气中燃烧的化学方程式 。
乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体。
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二: ;猜想三:Ca(OH)2。
他的依据是 。
【交流反思】经过同学们交流讨论,认为猜想一不成立。否定猜想一的理由是:
。
【进行实验】
(一)取少量白色固体放入试管中,滴加稀盐酸,没有观察到 ,证明猜想二不成立。
(二)取少量白色固体加入到水中,取上层清液, ,有白色沉淀出现,证明猜想三成立。该反应的化学方程式为:
。
结论:白色固体是Ca(OH)2。
【拓展应用】已知碳化钙与水反应非常剧烈,乙炔的密度比空气略小。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置是 (选填图中装置序号)。
A B C D E F
乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体。
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二: ;猜想三:Ca(OH)2。
他的依据是 。
【交流反思】经过同学们交流讨论,认为猜想一不成立。否定猜想一的理由是:
。
【进行实验】
(一)取少量白色固体放入试管中,滴加稀盐酸,没有观察到 ,证明猜想二不成立。
(二)取少量白色固体加入到水中,取上层清液, ,有白色沉淀出现,证明猜想三成立。该反应的化学方程式为:
。
结论:白色固体是Ca(OH)2。
【拓展应用】已知碳化钙与水反应非常剧烈,乙炔的密度比空气略小。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置是 (选填图15中装置序号)。

|
查看习题详情和答案>>