摘要:42.甲化工厂排放的酸性污水和乙化工厂排放的污水.共含有以下6种离子中的各3种:K+. OH-.C03 2-.Ba2+.H+.NO3-.则乙化工厂排放的污水中所含有的3种离子是 A.K+.OH-.H+ B.K+.OH-.C03 2- C.Ba2+.OH-.NO- D.O2-.K+.Ba2+
网址:http://m.1010jiajiao.com/timu3_id_97175[举报]
甲化工厂排放的酸性污水和乙化工厂排放的污水,共含有以下6种离子中的各3种:K+OH-、CO32-、Ba2+、H+、NO3-,则乙化工厂排放的污水中所含有的3种离子是( )
A. K+、OH-、H+ B. K+、OH-、CO32-
C. Ba2+、OH-、NO3- D. OH-、K+、Ba2+
查看习题详情和答案>>
 A.某镇有座硫酸厂,设备简陋,技术陈旧,该厂每天排放大量含SO2的废气和含H2SO4的酸性废水.当地的其他工厂和居民均用煤炭作燃料.只要下雨就下酸雨,对该镇环境造成极大破坏.
A.某镇有座硫酸厂,设备简陋,技术陈旧,该厂每天排放大量含SO2的废气和含H2SO4的酸性废水.当地的其他工厂和居民均用煤炭作燃料.只要下雨就下酸雨,对该镇环境造成极大破坏.(1)分析该镇下酸雨的原因:
(2)举一例说明酸雨对环境造成的危害:
(3)二氧化硫是大气污染物,溶于水所得溶液的pH
(4)该镇某中学环保小组提出了治理酸雨的下列措施,你认为其中不妥的是
A.将硫酸厂搬离该镇
B.建议环保部门下令整改
C.将硫酸厂排出的废气中的SO2处理后排放
D.工厂和居民改用较清洁的燃料
(5)可用熟石灰来处理硫酸厂排出的酸性废水,处理原理的化学方程式是
(6)浓硫酸弄到手上后应立即用水冲洗,然后涂上碳酸氢钠.若是稀硫酸弄到手上,
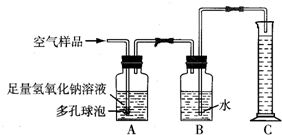
B.据报道,从2005年1月1日起,贵州省各地环保部门将对实验室类污染实施严格的环境监管.由于学校化学实验室要排放成分复杂的污染物,所以也被列为环境监管范围.某校化学兴趣小组的同学在甲实验室中进行了氧气分别与碳、硫、铁反应的实验后,为了解该实验产生的气体对空气成分造成的影响,接着设计了如下实验装置进行实验(图中多孔球泡的作用是:增大气体与溶液的接触面积,使反应充分进行).请回答下列问题:
(1)实验在没有受污染的乙实验室中进行,取出适量甲实验室中空气样品的方法是
(2)将取得的空气样品按如图所示的装置进行实验测定:装置A的作用是
(3)若通入空气样品100mL,实验结束后,量筒中液体的体积为99mL(导管内液体忽略不计),说明装置
(4)请写出你在做化学实验时,减少实验对环境污染的一种做法:
 2003年6月5日世界环境日的主题是:“水--二十亿人生命之所系”.请你回答下列问题:
2003年6月5日世界环境日的主题是:“水--二十亿人生命之所系”.请你回答下列问题:(1)自来水常用二氧化氯(ClO2)来杀菌消毒,它能转化为可溶解性氯化物.为检验自来水中是否含有氯离子,应选用的化学试剂是
AgNO3和稀硝酸
AgNO3和稀硝酸
.(2)节约用水,防治水污染具有十分重要的意义.某工厂有甲、乙、丙三个车间,各自排放的污水中均无沉淀物.各车间的污水分别含有以下六种物质中的各两种:KOH、K2SO4、AgNO3、Ba(NO3)2、KCl、HNO3.为防止污染水源,某中学化学兴趣小组配合工厂进行污水检测,结果如下表.
试剂 现象 车间 |
石蕊试液 | 氯化钡溶液 |
甲 |
蓝色 | 白色沉淀 |
| 乙 | 紫色 | 无明显现象 |
| 丙 | 红色 | 白色沉淀 |
HNO3
HNO3
和AgNO3
AgNO3
.为变害为利,化学兴趣小组与工厂研究设计如下图污水处理方案.请回答:沉淀A是BaSO4
BaSO4
,若各步处理均完全反应,最终排放液C的溶质是KNO3
KNO3
,在农业上它可用作复合肥料. 机动车排放的尾气是空气的重要污染源,其成分之一是NO.某化学兴趣小组的同学在查阅资料后得知:
机动车排放的尾气是空气的重要污染源,其成分之一是NO.某化学兴趣小组的同学在查阅资料后得知:
A.NO的部分性质(已知:空气在20℃时的密度是1.293g/L).
| 物理性质 | 化学性质 | |||
| 颜色 | 沸点 | 密度(20℃)[来 | 溶解性 | |
| 无色 | -151.76℃ | 1.249 g/L | 不易溶于水 | 2NO+O2=2NO2 |
请根据上面信息回答下列问题:
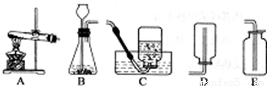
(1)若选择合适的装置来制取并收集NO气体,发生装置选择______,
收集装置选择______.
(2)用装置C收集气体前,将集气瓶内的空气排尽的操作方法是:______.
(3)该小组的同学通过查阅资料还得知:①NO容易和血红蛋白结合而使人中毒;②NO能抗击侵入人体的微生物,并能阻止癌细胞的繁殖和肿瘤细胞的扩散.综合分析①和②的信息,你得到的启示是______.
(4)某化工厂准备生产Cu(NO3)2,以铜和稀硝酸为主要原料设计了两种方案:
方案甲:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑十4X;
方案乙:2Cu+O2═2CuO CuO+2HNO3═Cu(NO3)2+H2O
从环境保护的角度考虑,你认为较合理的方案是______.从经济效益的角度考虑,选择此方案的另一条理由是______. 查看习题详情和答案>>
机动车排放的尾气是空气的重要污染源,其成分之一是NO.某化学兴趣小组的同学在查阅资料后得知:
A.NO的部分性质(已知:空气在20℃时的密度是1.293g/L).
B.NO的实验室制法:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑十4H2O
请根据上面信息回答下列问题:
(1)若选择合适的装置来制取并收集NO气体,发生装置选择______,
收集装置选择______.
(2)用装置C收集气体前,将集气瓶内的空气排尽的操作方法是:______.
(3)该小组的同学通过查阅资料还得知:①NO容易和血红蛋白结合而使人中毒;②NO能抗击侵入人体的微生物,并能阻止癌细胞的繁殖和肿瘤细胞的扩散.综合分析①和②的信息,你得到的启示是______.
(4)某化工厂准备生产Cu(NO3)2,以铜和稀硝酸为主要原料设计了两种方案:
方案甲:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑十4X;
方案乙:2Cu+O2═2CuO CuO+2HNO3═Cu(NO3)2+H2O
从环境保护的角度考虑,你认为较合理的方案是______.从经济效益的角度考虑,选择此方案的另一条理由是______.
 查看习题详情和答案>>
查看习题详情和答案>>
A.NO的部分性质(已知:空气在20℃时的密度是1.293g/L).
| 物理性质 | 化学性质 | |||
| 颜色 | 沸点 | 密度(20℃)[来 | 溶解性 | |
| 无色 | -151.76℃ | 1.249 g/L | 不易溶于水 | 2NO+O2=2NO2 |
请根据上面信息回答下列问题:
(1)若选择合适的装置来制取并收集NO气体,发生装置选择______,
收集装置选择______.
(2)用装置C收集气体前,将集气瓶内的空气排尽的操作方法是:______.
(3)该小组的同学通过查阅资料还得知:①NO容易和血红蛋白结合而使人中毒;②NO能抗击侵入人体的微生物,并能阻止癌细胞的繁殖和肿瘤细胞的扩散.综合分析①和②的信息,你得到的启示是______.
(4)某化工厂准备生产Cu(NO3)2,以铜和稀硝酸为主要原料设计了两种方案:
方案甲:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑十4X;
方案乙:2Cu+O2═2CuO CuO+2HNO3═Cu(NO3)2+H2O
从环境保护的角度考虑,你认为较合理的方案是______.从经济效益的角度考虑,选择此方案的另一条理由是______.
 查看习题详情和答案>>
查看习题详情和答案>>