摘要:(1)离子的写法 方法:先写出元素符号.再在右上角标明该离子带的电荷数.注意“+.- 于数字后面 例:3个硫酸根离子:3SO42-,两个镁离子:2Mg2+ (2)分子的写法 方法:写某物质的一个分子符号时.就用该物质的化学式表示其分子符号. 例:3个二氧化硫分子:3SO2,一个氨气分子:NH3 (3)结构示意图 原子结构示意图:先确定圆圈内数值然后再依次排出其电子数来.原子时有:电子决数==圆圈内的质子数. 例:画出钠原子的结构示意图 离子结构示意图:先确定圆圈内的数值然后再排电子数时.电子数总和等于质子数加上或减去所带的电荷数. 例:画出AI3+的结构示意图
网址:http://m.1010jiajiao.com/timu3_id_94689[举报]
氯碱厂电解饱和食盐水溶液制取NaOH的工艺流程示意图如图:
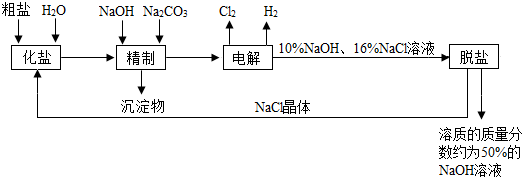
依据图,完成下列填空:
(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和 ,请用适当的数字和符号填空
②2个氯分子 ③粗盐中含有的一种阳离子
④零价的氢元素 ⑤硫酸钠
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是 .
(3)在电解过程中,发生反应的化学方程式为 ,
电解后溶液的pH .(填“升高”、“不变”、“降低”)
(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是 .
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(5)为了有效地除去氯化镁、氯化钙、硫酸钠,加入试剂的合理顺序为 .
A.先加入NaOH,后加入Na2CO3,再加入钡试剂
B.先加入NaOH,后加入钡试剂,再加入Na2CO3
C.先加入钡试剂,后加入NaOH,再加入Na2CO3
D.先加入钡试剂,后加入Na2CO3,再加入NaOH
(6)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过 (填写操作名称)、冷却、过滤除去NaCl.
(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式 .
查看习题详情和答案>>

依据图,完成下列填空:
(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和
②2个氯分子
④零价的氢元素
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是
(3)在电解过程中,发生反应的化学方程式为
电解后溶液的pH
(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(5)为了有效地除去氯化镁、氯化钙、硫酸钠,加入试剂的合理顺序为
A.先加入NaOH,后加入Na2CO3,再加入钡试剂
B.先加入NaOH,后加入钡试剂,再加入Na2CO3
C.先加入钡试剂,后加入NaOH,再加入Na2CO3
D.先加入钡试剂,后加入Na2CO3,再加入NaOH
(6)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式
氯碱厂电解饱和食盐水溶液制取NaOH的工艺流程示意图如图:
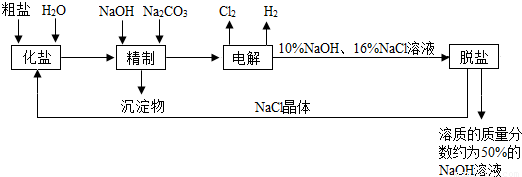
依据图,完成下列填空:
(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和 ,请用适当的数字和符号填空
②2个氯分子 ③粗盐中含有的一种阳离子
④零价的氢元素 ⑤硫酸钠
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是 .
(3)在电解过程中,发生反应的化学方程式为 ,
电解后溶液的pH .(填“升高”、“不变”、“降低”)
(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是 .
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(5)为了有效地除去氯化镁、氯化钙、硫酸钠,加入试剂的合理顺序为 .
A.先加入NaOH,后加入Na2CO3,再加入钡试剂
B.先加入NaOH,后加入钡试剂,再加入Na2CO3
C.先加入钡试剂,后加入NaOH,再加入Na2CO3
D.先加入钡试剂,后加入Na2CO3,再加入NaOH
(6)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过 (填写操作名称)、冷却、过滤除去NaCl.
(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式 . 查看习题详情和答案>>

依据图,完成下列填空:
(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和 ,请用适当的数字和符号填空
②2个氯分子 ③粗盐中含有的一种阳离子
④零价的氢元素 ⑤硫酸钠
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是 .
(3)在电解过程中,发生反应的化学方程式为 ,
电解后溶液的pH .(填“升高”、“不变”、“降低”)
(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是 .
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(5)为了有效地除去氯化镁、氯化钙、硫酸钠,加入试剂的合理顺序为 .
A.先加入NaOH,后加入Na2CO3,再加入钡试剂
B.先加入NaOH,后加入钡试剂,再加入Na2CO3
C.先加入钡试剂,后加入NaOH,再加入Na2CO3
D.先加入钡试剂,后加入Na2CO3,再加入NaOH
(6)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过 (填写操作名称)、冷却、过滤除去NaCl.
(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式 . 查看习题详情和答案>>
信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,将得到的红色金属M和金属E进行如下框图所示转化,获得高效净水剂K2EO4.(答题时,化学式及化学方程式中的M、E均用所对应的元素符号表示):

(1)写出M溶于稀H2SO4和H2O2混合液的离子方程式 。
(2)检验X中阳离子的方法和现象是 。
(3)某同学取X的溶液在空气中放置后,酸化并加入KI和淀粉溶液,溶液变为蓝色。试用离子方程式表示溶液变为蓝色的原因: 。
(4)由MSO4的蓝色溶液经一系列操作可以获得蓝色晶体,这些操作中用到的实验仪器除了酒精灯、烧杯、玻璃棒、漏斗、铁架台外,还需要用到的硅酸盐仪器有 (填写仪器名称)。
(5)某同学利用H2还原MO来测定M的相对原子质量,下图是测定装置示意图。A中试剂是盐酸。

①装置D的作用 ;
②连接好装置并检验装置的气密性后,应首先“加热反应管E”还是“从A瓶中逐滴加入液体”? 在这两步之间还应进行的操作是 。
③该实验设计是否还有不足之处?若有请指出并改进,如没有本问可不答。
(6)试说明K2EO4可用作高效净水剂的原因 。
查看习题详情和答案>>