摘要:某一氧化碳和二氧化碳组成的混合气体.先通过灼热的氧化铜粉末充分反应.消耗了7.95g氧化铜.再将剩余气体通过足量的澄清石灰水.充分反应后.生成沉淀20g.则原混合气体中二氧化碳气体的质量为多少克? 第二学期大庆油田教育中心期末检测
网址:http://m.1010jiajiao.com/timu3_id_93655[举报]
某一氧化碳和二氧化碳组成的混合气体,先通过灼热的氧化铜粉末充分反应,消耗了7.95g氧化铜,再将剩余气体通过足量的澄清石灰水,充分反应后,生成沉淀20g,则原混合气体中二氧化碳气体的质量为多少克? .
查看习题详情和答案>>
某一氧化碳和二氧化碳组成的混合气体,先通过灼热的氧化铜粉末充分反应,消耗了7.95g氧化铜,再将剩余气体通过足量的澄清石灰水,充分反应后,生成沉淀20g,则原混合气体中二氧化碳气体的质量为多少克?________.
查看习题详情和答案>>某一氧化碳和二氧化碳组成的混合气体,先通过灼热的氧化铜粉末充分反应,消耗了7.95g氧化铜,再将剩余气体通过足量的澄清石灰水,充分反应后,生成沉淀20g,则原混合气体中二氧化碳气体的质量为多少克?
查看习题详情和答案>>
某一氧化碳和二氧化碳组成的混合气体,先通过灼热的氧化铜粉末充分反应,消耗了7.95g氧化铜,再将剩余气体通过足量的澄清石灰水,充分反应后,生成沉淀20g,则原混合气体中二氧化碳气体的质量为多少克?______ Cu+CO2
79.5 44
7.95g y
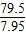 =
=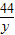
y=4.4克,
所以原混合气中二氧化碳为:8.8-4.4=4.4克,
答:原混合气中二氧化碳为8.8-4.4=4.4克. 查看习题详情和答案>>
79.5 44
7.95g y
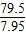 =
=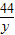
y=4.4克,
所以原混合气中二氧化碳为:8.8-4.4=4.4克,
答:原混合气中二氧化碳为8.8-4.4=4.4克. 查看习题详情和答案>>
 某一定量的乙醇燃烧时由于氧气不足,燃烧的产物为二氧化碳、一氧化碳和水蒸气的混合物.现实验室提供下列盛有药品的仪器(假设各装置中的反应或吸收都是完全的),有两名同学各自证明上述混合气体中的各成分.请用A、B、C、D填空.
某一定量的乙醇燃烧时由于氧气不足,燃烧的产物为二氧化碳、一氧化碳和水蒸气的混合物.现实验室提供下列盛有药品的仪器(假设各装置中的反应或吸收都是完全的),有两名同学各自证明上述混合气体中的各成分.请用A、B、C、D填空.(1)甲同学分别证明混合气体中含有某一种气体:
①证明其中含有水蒸气,选用
B
B
②证明其中含有CO2,选用
D
D
③选取必要的仪器(每种只能用一次)证明其中含有CO,按气体通过的先后顺序依次是
C、A、D
C、A、D
(2)乙同学用上述仪器(每种只用一次)组装一套装置,通过一次实验证明混合气体中含有CO2、CO和水蒸气,则应该将
C
C
中药品换成Ba(OH)2溶液,按气体通过的先后顺序,连接的仪器依次是B、C、A、D
B、C、A、D
.