网址:http://m.1010jiajiao.com/timu3_id_93172[举报]
请你仔细分析后回答下列问题:
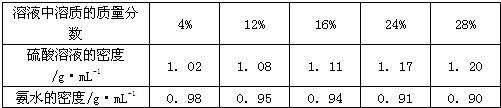
(1)根据上表可总结出的规律是:对于硫酸溶液
对于氨水
(2)某同学多次、随机抽取表中数据来探究浓、稀溶液等体积混合后,溶质质量分数与浓、稀溶液等质量混合后溶质质量分数之间的关系.
已知:将12%的硫酸溶液与28%的硫酸溶液等质量混合,所的溶液中溶质的质量分数等于a%,此a值为
而将12%的硫酸溶液与28%的硫酸溶液等体积混合,所得溶液中溶质的质量分数
将12%的氨水与28%的氨水等体积混合,所得溶液中溶质的质量分数
(3)根据以上计算或推理的结果,总结出的规律是
甲生认为:可用溶液的颜色深浅判断;
乙生认为:溶液的密度大小判断;
丙生认为:溶液与其他物质发生化学反应的速率大小判断.
请你判断甲、乙、丙三位学生的观点是否正确,并举例说明理由.
【小题1】下列各类食物中蛋白质含量最丰富的是 (填序号,下同)。




①草莓 ②西红柿 ③米饭 ④鸡蛋
【小题2】人体缺乏碘元素易引起甲状腺肿大,碘元素在周期表中的信息如下图所示。

则下列说法正确的是 。
①加碘食盐中的碘是指碘单质 ②碘的原子序数是53
③新鲜蔬菜、瓜果中含丰富的碘元素 ④碘的相对原子质量是126.9
【小题3】下列生活中的物品,属于有机合成材料的是 。

①橡胶轮胎 ②不锈钢锅 ③棉布围裙 ④塑料保鲜盒
【小题4】我们穿的衣服通常是由纤维织成的,常见的纤维有棉花、羊毛、涤纶等,用灼烧法可初步鉴定这三种纤维,其中灼烧后产生烧焦羽毛气味的纤维是 。
①棉花 ②羊毛 ③涤纶
【小题5】科学家预测“氢能”将是21世纪最理想的新能源。氢气燃烧的化学方程式为 。
【小题6】餐具上的油污可以用加入洗涤剂的水洗掉,说明洗涤剂具有 功能。
【小题7】 味精是烹制菜肴的调味品,味精的鲜味与溶液的酸碱度有关,当pH为6-7时鲜味最强;味精的鲜味还与温度有关,其水溶液经120℃以上长时间加热,不仅鲜味消失,而且生成对人体有害的焦谷氨酸钠。据此,下列认识正确的是 。
A.味精应避免在酸性或碱性较强的条件下使用
B.谷氨酸钠在加热条件下生成焦谷氨酸钠是物理变化
C.菜烧熟起锅后再放味精比炒菜过程中加入味精更有利于人体健康 查看习题详情和答案>>
(7分)化学与人类生活的关系越来越密切。
【小题1】下列各类食物中蛋白质含量最丰富的是 (填序号,下同)。



①草莓 ②西红柿 ③米饭 ④鸡蛋
【小题2】人体缺乏碘元素易引起甲状腺肿大,碘元素在周期表中的信息如下图所示。
则下列说法正确的是 。
①加碘食盐中的碘是指碘单质 ②碘的原子序数是53
③新鲜蔬菜、瓜果中含丰富的碘元素 ④碘的相对原子质量是126.9
【小题3】下列生活中的物品,属于有机合成材料的是 。
①橡胶轮胎 ②不锈钢锅 ③棉布围裙 ④塑料保鲜盒
【小题4】我们穿的衣服通常是由纤维织成的,常见的纤维有棉花、羊毛、涤纶等,用灼烧法可初步鉴定这三种纤维,其中灼烧后产生烧焦羽毛气味的纤维是 。
①棉花 ②羊毛 ③涤纶
【小题5】科学家预测“氢能”将是21世纪最理想的新能源。氢气燃烧的化学方程式为 。
【小题6】餐具上的油污可以用加入洗涤剂的水洗掉,说明洗涤剂具有 功能。
【小题7】 味精是烹制菜肴的调味品,味精的鲜味与溶液的酸碱度有关,当pH为6-7时鲜味最强;味精的鲜味还与温度有关,其水溶液经120℃以上长时间加热,不仅鲜味消失,而且生成对人体有害的焦谷氨酸钠。据此,下列认识正确的是 。
A.味精应避免在酸性或碱性较强的条件下使用
B.谷氨酸钠在加热条件下生成焦谷氨酸钠是物理变化
C.菜烧熟起锅后再放味精比炒菜过程中加入味精更有利于人体健康
(1)(文字表达式2分,共16分)实验室制取气体是初中非常重要的一组实验,结合下列实验装置图回答有关问题:


①(9分)仪器a的名称是 。小强想用氯酸钾与二氧化锰加热制氧气,应选用的气体发生装置是 (填字母),发生反应的文字表达式是 。小红想用过氧化氢溶液和二氧化锰来制取氧气,应选择的气体发生装置是_________(填装置序号),在加试剂之前的操作是___________________________;发生反应的文字表达式是 。请你比较小红与小强的方法,其中小红选择的方法的优点有____________________________________(答一条)。
②(7分)小刘同学善于动脑筋,在复习 “铁在氧气里燃烧”实验后,他进行了一系列思考和探究:实验时在集气瓶里加少量水,其目的是______________________________________,发生反应的文字表达式是 。该反应属于 反应(填反应类型”);在复习“硫粉在氧气中燃烧”的实验后,他认为若收集一瓶氧气供硫粉在氧气中燃烧时使用,最好选择气体收集装置中的___________(填装置序号),理由是________________________________________。通过查阅资料得知:①氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水,显碱性;小刘同学想收集一瓶氨气,他应选择的收集装置是 (填字母编号);
(2)(最后一空2分,共5分)实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气, 小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除Mn02、CuO外,Fe203也可以作KCl03分解的催化剂。
【完成实验】按下表进行实验,并测定分解温度(分解温度越低,催化效果越好)。
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | KCl03 | 580 |
| ② | KCl03、Mn02质量比1:1) | 350 |
| ③ | KCl03、CuO(质量比l:1) | 370 |
| ④ | KCl03、Fe203(质量比1:1) | 390 |
【分析数据、得出结论】:由实验____________与实验④对比,证明猜想合理;实验所用的三种金属氧化物,催化效果最好的是_____________________。
【反思】:若要证明Fe203是该反应的催化剂,还要验证它在化学反应前后的质量和__________不变;质量相同的同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证:__ ___ ___。
查看习题详情和答案>>