摘要:1.实验室里常用分解过氧化氢溶液或加热高锰酸钾的方法来制取氧气. a.2H2O2 MnO2 2H2O+ O2↑ 请指出该反应中的反应物是: .反应条件是: .生成物是 MnO2在该反应中作 .它的特点是.虽然参加了化学反应.但其 和 不变.其作用是改变化学反应的 . b.2KMnO4 加热 K2MnO4 + MnO2 + O2↑ 画出该制取氧气的装置图.并标明仪器名称:
网址:http://m.1010jiajiao.com/timu3_id_92904[举报]
在实验室里可用
查看习题详情和答案>>
分解过氧化氢溶液
分解过氧化氢溶液
或加热氯酸钾
加热氯酸钾
来制取氧气.当用过氧化氢溶液
过氧化氢溶液
制取氧气时,通常加入二氧化锰,这时,二氧化锰起催化
催化
作用,反应完毕后,当把二氧化锰分离出来,发现此时的二氧化锰的质量
质量
和化学性质
化学性质
没有发生变化.在实验室里,常用分解过氧化氢溶液或加热高锰酸钾的方法制取氧气。两个反应均属于 反应类型。在两个反应中,都接触到二氧化锰,在前一个反应中,它是该反应的 ,在后一个反应中,它是该反应的____。
查看习题详情和答案>>
在实验室里,常用分解过氧化氢溶液(二氧化锰作催化剂)的方法制取氧气(如图所示).

(1)该制取反应的文字表达式为 .
(2)如果锥形瓶中的反应过于剧烈,应该采取的措施是: .
(3)过氧化氢在常温下分解缓慢,加入二氧化锰或红砖粉后反应明显加快,若要证明二氧化锰或红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的 和 是否改变.
查看习题详情和答案>>

(1)该制取反应的文字表达式为
(2)如果锥形瓶中的反应过于剧烈,应该采取的措施是:
(3)过氧化氢在常温下分解缓慢,加入二氧化锰或红砖粉后反应明显加快,若要证明二氧化锰或红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的
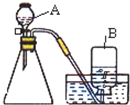 在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.(1)小明同学选用如图所示的装置制取氧气.制取过程中所发生的化学反应表达式为:
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.实验过程中,证明集气瓶收集满氧气的现象是
| ||
集气瓶口有气泡溢出
集气瓶口有气泡溢出
.(2)小红同学通过互联网得知:CuSO4溶液、动物某些脏器中含有的物质等能催化过氧化氢的分解.实验证明,在过氧化氢溶液中滴加CuSO4溶液能显著加快过氧化氢的分解.CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42-),为了进一步探究CuSO4溶液中哪种粒子能起催化作用.小红同学作了以下分析和设计.
①小红同学认为最不可能的是H2O,他的理由是
过氧化氢的溶液中中的溶剂是水,因此H2O不能起催化作用
过氧化氢的溶液中中的溶剂是水,因此H2O不能起催化作用
.②要说明另外的两种粒子是否起到催化作用,小红同学设计了如下实验,完成了这次探究活动.
| 实验步骤 | 实验现象 | 结论 |
| a.取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴稀硫酸(含SO42-) | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是 Cu2+ Cu2+ . |
| b.另取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴 硫酸铜 硫酸铜 溶液 |
溶液中有大量气泡放出 |
质量和化学性质不发生改变
质量和化学性质不发生改变
. 在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.(1)小明同学选用如图所示的装置制取氧气.制取过程中所发生的化学反应表达式为:
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
实验前小明同学先向仪器A中加入水,然后将导气管放入水槽中,并打开仪器A的活塞,观察导气管口是否有连续的气泡出现.该实验操作的目的是
检查装置的气密性
检查装置的气密性
.(2)小红同学通过互联网得知:CuSO4溶液、动物某些脏器中含有的物质等能催化过氧化氢的分解.
实验证明,在过氧化氢溶液中滴加CuSO4溶液能显著加快过氧化氢的分解.CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42-),为了进一步探究CuSO4溶液中哪种粒子能起催化作用.小红同学作了以下分析和设计.
①小红同学认为最不可能的是H2O,他的理由是
过氧化氢溶液中的溶剂是水,因此H2O不能起催化作用
过氧化氢溶液中的溶剂是水,因此H2O不能起催化作用
.②要说明另外的两种粒子是否起到催化作用,小红同学设计了如下实验,完成了这次探究活动.
| 实验步骤 | 实验现象 | 结论 |
| a.取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴稀硫酸(含SO42-) | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是 铜离子 铜离子 . |
| b.另取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴 硫酸铜 硫酸铜 溶液 |
溶液中有大量气泡放出 |
化学性质和质量都不变
化学性质和质量都不变
.