摘要:16.有一包黑色粉末.在试管里加强热后有红色固体出现.放出使澄清石灰水变浑浊的气体.可知这包黑色粉末是 ( ) A.Fe3O4.MnO2 B.CuO.C C.CuO.MnO2. D.MnO2.C
网址:http://m.1010jiajiao.com/timu3_id_91467[举报]
为了防止食品腐败,在许多食品包装盒中都有一包黑色粉末,这种粉末是一种除氧剂,该粉末没有失效时呈黑色,失败后带有红棕色,为了确定该粉末的成分,小明做出了以下的猜想.
猜想1 该粉末是炭粉;
猜想2 该粉末是铁粉
猜想3 该粉末是木炭粉和铁粉的混合物
如下实验,填写表中空格
交流与反思
(1)根据失效后的颜色判断,该粉末失效的原因是
(2)采用什么实验方法可以使失效的粉末“再生”?
查看习题详情和答案>>
猜想1 该粉末是炭粉;
猜想2 该粉末是铁粉
猜想3 该粉末是木炭粉和铁粉的混合物
如下实验,填写表中空格
| 实验操作 | 实验现象 | 猜想是否成立 | |
| 实验1 | 加入足量的硫酸铜溶液 | 黑色粉末变成红色 黑色粉末变成红色 |
猜想1:不成立 |
| 实验2 | 加入足量 稀盐酸 稀盐酸 |
黑色粉末逐渐溶解,有大量的气泡产生 黑色粉末逐渐溶解,有大量的气泡产生 |
猜想2:成立 |
| 实验3 | 用磁铁吸引 | 粉末被全部吸引 | 猜想3: 不成立 不成立 |
(1)根据失效后的颜色判断,该粉末失效的原因是
铁与空气中的氧气和水反应生成了铁锈
铁与空气中的氧气和水反应生成了铁锈
.变质后得到的红棕色粉末的主要成分是Fe2O3
Fe2O3
(化学式)(2)采用什么实验方法可以使失效的粉末“再生”?
可在高温条件下,使用CO还原氧化铁而等到铁粉
可在高温条件下,使用CO还原氧化铁而等到铁粉
化学方程式为3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
.
| ||
(2011?巴中)有一包黑色粉末,可能是铁粉、木炭粉、氧化铜中的一种或几种,为了证明它的组成,进行如下探究实验
(1)验证并分离铁粉的最简单的物理方法是
(2)通过实验已证明该包黑色粉末没有铁粉,再取黑色粉末少许于试管中,加入足量的稀硫酸微热,现象
写出上述反应中的化学方程式:
查看习题详情和答案>>
(1)验证并分离铁粉的最简单的物理方法是
用磁铁吸引
用磁铁吸引
.(2)通过实验已证明该包黑色粉末没有铁粉,再取黑色粉末少许于试管中,加入足量的稀硫酸微热,现象
黑色固体全部溶解,溶液变蓝
黑色固体全部溶解,溶液变蓝
,结论是黑色粉末只含有氧化铜.写出上述反应中的化学方程式:
CuO+H2SO4═CuSO4+H2O
CuO+H2SO4═CuSO4+H2O
.(1)实验是进行科学探究的重要方式,请根据图回答问题:
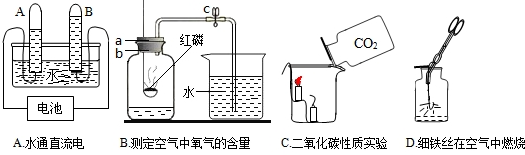
①用A图所示装置进行电解水实验时,A管的导线连接的是直流电的 极.
②用B图所示装置测定空气中氧气的含量时,得到的结论是: .
③利用C图所示方法,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛的火焰先熄灭.二氧化碳这种性质在实际生活中的应用为 .
④利用D图所示方法,对细铁丝在氧气中燃烧为什么会火星四射进行探究.下表不同含碳量的铁丝(所用铁丝直径均相同)放入氧气中燃烧时的实验现象:
由上表可分析出,“火星”可能是 与氧气反应所导致的.
(2)为了防止食品腐败,在许多食品包装盒中都有一包黑色粉末.这种粉末是一种除氧剂.该粉末没有失效时呈黑色,失效后带有红棕色.为了确定该粉末的成分,小明做出了以下的猜想:
猜想1:该粉末是木炭粉
猜想2:该粉末是铁粉
猜想3:该粉末是木炭粉和铁粉的混合物
小明取没有失效的该粉末,分别用不同的方法进行如下实验,填写表中空格.
交流与反思:
①根据失效后的颜色判断,该粉末失效的原因是
变质后得到的红棕色粉末的主要成分是 (填物质的化学式).
②采用什么实验方法可以使失效的粉末“再生”?(用化学方程式表示) .
查看习题详情和答案>>

①用A图所示装置进行电解水实验时,A管的导线连接的是直流电的
②用B图所示装置测定空气中氧气的含量时,得到的结论是:
③利用C图所示方法,把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛的火焰先熄灭.二氧化碳这种性质在实际生活中的应用为
④利用D图所示方法,对细铁丝在氧气中燃烧为什么会火星四射进行探究.下表不同含碳量的铁丝(所用铁丝直径均相同)放入氧气中燃烧时的实验现象:
| 铁丝中含碳量 | 0.05% | 0.2% | 0.6% |
| 燃烧时的现象 | 剧烈燃烧,极少火星 | 剧烈燃烧,少量火星 | 剧烈燃烧,大量火星 |
(2)为了防止食品腐败,在许多食品包装盒中都有一包黑色粉末.这种粉末是一种除氧剂.该粉末没有失效时呈黑色,失效后带有红棕色.为了确定该粉末的成分,小明做出了以下的猜想:
猜想1:该粉末是木炭粉
猜想2:该粉末是铁粉
猜想3:该粉末是木炭粉和铁粉的混合物
小明取没有失效的该粉末,分别用不同的方法进行如下实验,填写表中空格.
| 实验操作 | 实验现象 | 猜想是否成立 | |
| 实验1 | 加入足量的硫酸铜溶液 | 猜想1:不成立 | |
| 实验2 | 加入足量的 |
猜想2:成立 | |
| 实验3 | 用磁铁吸引 | 粉末被全部吸引 | 猜想3: |
①根据失效后的颜色判断,该粉末失效的原因是
变质后得到的红棕色粉末的主要成分是
②采用什么实验方法可以使失效的粉末“再生”?(用化学方程式表示)
28、有一包黑色粉末,可能由C、CuO、Fe三种物质中的一种或几种组成,为探究其成份,进行如下探究:取少量粉末于烧杯中,加入过量稀H2SO4,微热.
(1)对可能出现的现象和结论分析如下,请完成下列表格:
(2)通过具体实验分析,确认该粉末一定含C和CuO,甲同学为进一步确认其中不含Fe,做了一个简单的实验,其方法为
(3)为进一步探究C和CuO的性质,乙同学经过查阅资料得知C在高温下能和金属氧化物发生反应,使金属氧化物还原,他利用该混合物做如下实验:
Ⅰ.取少量粉末放在敞口容器中充分灼烧,冷却到室温,将固体放入烧杯中,加入过量稀H2SO4,烧杯中
Ⅱ.另取少量粉末在隔绝空气情况下加热(假设碳完全反应),待冷却后,取剩余固体于烧杯中,再加入过量稀H2SO4,充分反应后静置,则烧杯中不溶物的存在情况是
查看习题详情和答案>>
(1)对可能出现的现象和结论分析如下,请完成下列表格:
| 烧杯中可能出现的现象 | 结 论 |
| 黑色粉末完全不溶 | |
| 黑色粉末为C和CuO混合物 | |
| 黑色粉末部分溶解,溶液变为浅绿色且有气泡产生 |
将粉末用磁铁吸引,无明显现象(或加盐酸看是否有气泡冒出)
.(3)为进一步探究C和CuO的性质,乙同学经过查阅资料得知C在高温下能和金属氧化物发生反应,使金属氧化物还原,他利用该混合物做如下实验:
Ⅰ.取少量粉末放在敞口容器中充分灼烧,冷却到室温,将固体放入烧杯中,加入过量稀H2SO4,烧杯中
无
不溶物(填“有”、“无”),溶液呈蓝
色.Ⅱ.另取少量粉末在隔绝空气情况下加热(假设碳完全反应),待冷却后,取剩余固体于烧杯中,再加入过量稀H2SO4,充分反应后静置,则烧杯中不溶物的存在情况是
一定有
(填“一定有”、“一定没有”、“可能有”),若溶液为蓝色,则溶液中的溶质为H2SO4,CuSO4
.