摘要:1.有一白色粉末A.到少量进行以下的实验: 试推判: 蓝色沉淀B是 .发生反应的化学方程式是 .白色沉淀C是 .发生反应的化学方程式是 .由此推断白色粉末A是 .
网址:http://m.1010jiajiao.com/timu3_id_89691[举报]
一包白色粉末,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成。为探究其组成,进行如下实验:
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液。
(2)取(1)中滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体。根据上述实验可推断:
| A.原固体混合物中一定不含有CuSO4、、Na2SO4 |
| B.原固体混合物中一定不含有CuSO4、Na2SO4、BaCl2 |
| C.原固体混合物中一定含有CaCO3、NaOH |
| D.为进一步探究原白色粉末的组成,取(1)中得到的滤液,向其中通入二氧化碳,产生白色沉淀,则可推断原白色粉末中一定还含有BaCl2 、NaOH |
(2005
年长沙)有一包白色粉末,可能由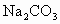 、
、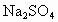 、
、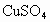 、NaCl等物质中的一种或几种组成.现进行下列实验:①取一定量的白色粉末于烧杯中,加足量的蒸馏水使其充分溶解,只得到无色澄清溶液.
、NaCl等物质中的一种或几种组成.现进行下列实验:①取一定量的白色粉末于烧杯中,加足量的蒸馏水使其充分溶解,只得到无色澄清溶液.
②取①中溶液少许于试管中,滴入
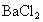 溶液,产生白色沉淀.
溶液,产生白色沉淀.
③向生成的白色沉淀中,加入足量稀硝酸,该白色沉淀部分溶解,并有气体
(A)产生,此气体能使澄清石灰水变浑浊.请根据以上实验推断:
(1)
该包白色粉末中一定会有________,一定不含________,可能含有________.(2)
写出气体(A)与澄清石灰水反应的化学方程式________. 查看习题详情和答案>>
食品添加剂碳酸钙为极细白色粉末,该产品可作面粉处理剂、膨松剂、稳定剂和食品工业用加工助剂.某实验探究小组利用石灰石为原料,设计了如下两个流程得到碳酸钙粉末.
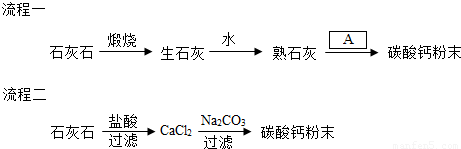
①生石灰的化学式是 ,流程一中加入的“A”可以是CO2,这样做的优点是 ;
②写出石灰石与盐酸发生的主要化学方程式 ;写出以上流程中属于化合反应的化学方程式 ;
③若石灰石中所含碳酸钙的纯度为90%,取用100g该石灰石则所含碳酸钙的物质的量为多少摩尔?用盐酸溶解上述石灰石,理论上所用盐酸含HCl的物质的量至少为多少摩尔?
请列式计算,写出计算过程:计算碳酸钙物质的量 计算HCl的物质的量
④“流程一”中生石灰加一定量的水得到熟石灰乳,而不是得到澄清石灰水,这样做的理由是 ;
为判断熟石灰是否完全转化,实验的方法可以是取反应过程中少量样品进行如下实验:
⑤“流程二”中有两次过滤,第一次过滤的目的是 ,
过滤后发现滤液仍有一些浑浊,而过滤器经检查发现完好,此时应该进行的操作是 .
⑥若要得到食品级碳酸钙,上述两个流程中,应该倾向利用 (填“流程一”“流程二”)进行生产. 查看习题详情和答案>>

①生石灰的化学式是 ,流程一中加入的“A”可以是CO2,这样做的优点是 ;
②写出石灰石与盐酸发生的主要化学方程式 ;写出以上流程中属于化合反应的化学方程式 ;
③若石灰石中所含碳酸钙的纯度为90%,取用100g该石灰石则所含碳酸钙的物质的量为多少摩尔?用盐酸溶解上述石灰石,理论上所用盐酸含HCl的物质的量至少为多少摩尔?
请列式计算,写出计算过程:计算碳酸钙物质的量 计算HCl的物质的量
④“流程一”中生石灰加一定量的水得到熟石灰乳,而不是得到澄清石灰水,这样做的理由是 ;
为判断熟石灰是否完全转化,实验的方法可以是取反应过程中少量样品进行如下实验:
| 实验药品及操作 | 实验现象 | 结论 |
| 熟石灰已完全转化 |
过滤后发现滤液仍有一些浑浊,而过滤器经检查发现完好,此时应该进行的操作是 .
⑥若要得到食品级碳酸钙,上述两个流程中,应该倾向利用 (填“流程一”“流程二”)进行生产. 查看习题详情和答案>>
夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”,宣称“含天然活性氧,能在瞬间去除洗衣粉难以除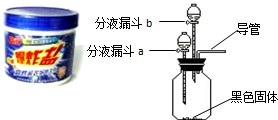 去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:
去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:
【提出问题】:“污渍爆炸盐”的主要化学成分是什么?
【查阅相关资料】:过碳酸钠俗称固体双氧水,白色结晶颗粒.过碳酸钠溶于水时,分解生成碳酸钠和过氧化氢,目前已成为世界上广泛应用的主要洗涤助剂之一.
【猜想】:“污渍爆炸盐”的主要化学成分可能是过碳酸钠.
【设计与实验】小强同学设计的主要实验装置如图所示.请你运用初中所学知识,帮助小强同学完成下列实验报告.
【实验的初步结论】:小强认为“污渍爆炸盐”溶于水生成碳酸钠和过氧化氢,所以“污渍爆炸盐”的主要化学成分是过碳酸钠.
【反思与评价】:根据探究经历,我知道还可以用红砖粉末等代替,同样可以达到实验效果;操作③中加入b中液体能产生所验证的气体,除碳酸钠等碳酸盐外,另一种俗名为小苏打的碳酸氢盐也有如此特性,化学方程式为
查看习题详情和答案>>
 去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:
去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:【提出问题】:“污渍爆炸盐”的主要化学成分是什么?
【查阅相关资料】:过碳酸钠俗称固体双氧水,白色结晶颗粒.过碳酸钠溶于水时,分解生成碳酸钠和过氧化氢,目前已成为世界上广泛应用的主要洗涤助剂之一.
【猜想】:“污渍爆炸盐”的主要化学成分可能是过碳酸钠.
【设计与实验】小强同学设计的主要实验装置如图所示.请你运用初中所学知识,帮助小强同学完成下列实验报告.
| 序号 | 主要操作步骤 | 主要实验现象 | 操作目的 |
| ① | 在广口瓶中加入少量 二氧化锰 二氧化锰 (黑色固体);在分液漏斗a中加入新配制的“污渍爆炸盐”的饱和水溶液;在分液漏斗b中加入稀盐酸 稀盐酸 . |
无 无 |
检验溶液中是否含有过氧化氢 检验溶液中是否含有过氧化氢 |
| ② | 打开分液漏斗a的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | 检验过氧化氢分解 检验过氧化氢分解 |
| 然后 用带火星的木条接近导管口 用带火星的木条接近导管口 . |
带火星的木条复燃 带火星的木条复燃 |
验证生成气体的成分 | |
| 第②步操作得到的结论:“污渍爆炸盐”溶于水生成过氧化氢. | |||
| ③ | 待②步反应停止后,打开分液漏斗b的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | 检验碳酸钠和盐酸反应 检验碳酸钠和盐酸反应 |
| 将生成的气体通入 澄清石灰水 澄清石灰水 . |
澄清石灰水变浑浊 澄清石灰水变浑浊 . |
验证生成气体的成分 | |
| 第③步操作得到的结论:“污渍爆炸盐”溶于水生成碳酸钠. | |||
【反思与评价】:根据探究经历,我知道还可以用红砖粉末等代替,同样可以达到实验效果;操作③中加入b中液体能产生所验证的气体,除碳酸钠等碳酸盐外,另一种俗名为小苏打的碳酸氢盐也有如此特性,化学方程式为
NaHCO3+HCl=NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
.夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”,宣称“含天然活性氧,能在瞬间去除洗衣粉难以除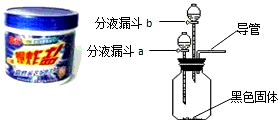 去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:
去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:
【提出问题】:“污渍爆炸盐”的主要化学成分是什么?
【查阅相关资料】:过碳酸钠俗称固体双氧水,白色结晶颗粒.过碳酸钠溶于水时,分解生成碳酸钠和过氧化氢,目前已成为世界上广泛应用的主要洗涤助剂之一.
【猜想】:“污渍爆炸盐”的主要化学成分可能是过碳酸钠.
【设计与实验】小强同学设计的主要实验装置如图所示.请你运用初中所学知识,帮助小强同学完成下列实验报告.
| 序号 | 主要操作步骤 | 主要实验现象 | 操作目的 |
| ① | 在广口瓶中加入少量________(黑色固体);在分液漏斗a中加入新配制的“污渍爆炸盐”的饱和水溶液;在分液漏斗b中加入________. | ________ | ________ |
| ② | 打开分液漏斗a的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | ________ |
| 然后________. | ________ | 验证生成气体的成分 | |
| 第②步操作得到的结论:“污渍爆炸盐”溶于水生成过氧化氢. | |||
| ③ | 待②步反应停止后,打开分液漏斗b的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | ________ |
| 将生成的气体通入________. | ________. | 验证生成气体的成分 | |
| 第③步操作得到的结论:“污渍爆炸盐”溶于水生成碳酸钠. | |||
【反思与评价】:根据探究经历,我知道还可以用红砖粉末等代替,同样可以达到实验效果;操作③中加入b中液体能产生所验证的气体,除碳酸钠等碳酸盐外,另一种俗名为小苏打的碳酸氢盐也有如此特性,化学方程式为________. 查看习题详情和答案>>