题目内容
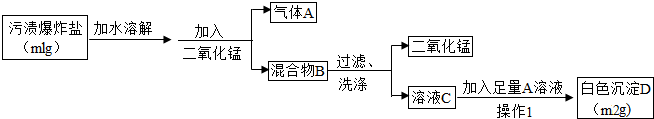
夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”,宣称“含天然活性氧,能在瞬间去除洗衣粉难以除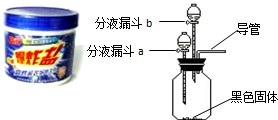 去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:
去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:
【提出问题】:“污渍爆炸盐”的主要化学成分是什么?
【查阅相关资料】:过碳酸钠俗称固体双氧水,白色结晶颗粒.过碳酸钠溶于水时,分解生成碳酸钠和过氧化氢,目前已成为世界上广泛应用的主要洗涤助剂之一.
【猜想】:“污渍爆炸盐”的主要化学成分可能是过碳酸钠.
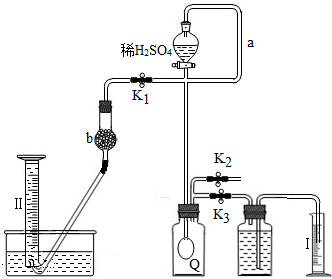
【设计与实验】小强同学设计的主要实验装置如图所示.请你运用初中所学知识,帮助小强同学完成下列实验报告.
【实验的初步结论】:小强认为“污渍爆炸盐”溶于水生成碳酸钠和过氧化氢,所以“污渍爆炸盐”的主要化学成分是过碳酸钠.
【反思与评价】:根据探究经历,我知道还可以用红砖粉末等代替,同样可以达到实验效果;操作③中加入b中液体能产生所验证的气体,除碳酸钠等碳酸盐外,另一种俗名为小苏打的碳酸氢盐也有如此特性,化学方程式为
 去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:
去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:【提出问题】:“污渍爆炸盐”的主要化学成分是什么?
【查阅相关资料】:过碳酸钠俗称固体双氧水,白色结晶颗粒.过碳酸钠溶于水时,分解生成碳酸钠和过氧化氢,目前已成为世界上广泛应用的主要洗涤助剂之一.
【猜想】:“污渍爆炸盐”的主要化学成分可能是过碳酸钠.
【设计与实验】小强同学设计的主要实验装置如图所示.请你运用初中所学知识,帮助小强同学完成下列实验报告.
| 序号 | 主要操作步骤 | 主要实验现象 | 操作目的 |
| ① | 在广口瓶中加入少量 二氧化锰 二氧化锰 (黑色固体);在分液漏斗a中加入新配制的“污渍爆炸盐”的饱和水溶液;在分液漏斗b中加入稀盐酸 稀盐酸 . |
无 无 |
检验溶液中是否含有过氧化氢 检验溶液中是否含有过氧化氢 |
| ② | 打开分液漏斗a的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | 检验过氧化氢分解 检验过氧化氢分解 |
| 然后 用带火星的木条接近导管口 用带火星的木条接近导管口 . |
带火星的木条复燃 带火星的木条复燃 |
验证生成气体的成分 | |
| 第②步操作得到的结论:“污渍爆炸盐”溶于水生成过氧化氢. | |||
| ③ | 待②步反应停止后,打开分液漏斗b的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | 检验碳酸钠和盐酸反应 检验碳酸钠和盐酸反应 |
| 将生成的气体通入 澄清石灰水 澄清石灰水 . |
澄清石灰水变浑浊 澄清石灰水变浑浊 . |
验证生成气体的成分 | |
| 第③步操作得到的结论:“污渍爆炸盐”溶于水生成碳酸钠. | |||
【反思与评价】:根据探究经历,我知道还可以用红砖粉末等代替,同样可以达到实验效果;操作③中加入b中液体能产生所验证的气体,除碳酸钠等碳酸盐外,另一种俗名为小苏打的碳酸氢盐也有如此特性,化学方程式为
NaHCO3+HCl=NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
.分析:①过碳酸钠溶于水时,分解生成碳酸钠和过氧化氢,碳酸钠能和盐酸反应生成二氧化碳气体,广口瓶中加入二氧化锰来催化过氧化氢分解,分液漏斗b中要加入稀盐酸来证明溶液中含有碳酸钠;
②过氧化氢遇二氧化锰能分解生成氧气,所以可以用带火星的木条来检验打开分液漏斗a后产生的气体是不是氧气,来判断分液漏斗A中是否含有过氧化氢溶液;
③在验证了过氧化氢的存在之后,为了更充分的说明含有碳酸钠,所以要滴加稀盐酸来观察现象然后得出是否含有碳酸钠;最后得出结论.
【反思与评价】:根据质量守恒定律和碳酸盐与盐酸反应的规律书写化学方程式.
②过氧化氢遇二氧化锰能分解生成氧气,所以可以用带火星的木条来检验打开分液漏斗a后产生的气体是不是氧气,来判断分液漏斗A中是否含有过氧化氢溶液;
③在验证了过氧化氢的存在之后,为了更充分的说明含有碳酸钠,所以要滴加稀盐酸来观察现象然后得出是否含有碳酸钠;最后得出结论.
【反思与评价】:根据质量守恒定律和碳酸盐与盐酸反应的规律书写化学方程式.
解答:解:①根据题给条件可知,过碳酸钠溶于水时,分解生成碳酸钠和过氧化氢,碳酸钠能和盐酸反应生成二氧化碳气体,由于在广口瓶中已经加入了黑色固体,该黑色固体很明显就是二氧化锰,所以分液漏斗b中要加入稀盐酸来证明溶液中含有碳酸钠;
②打开分液漏斗a后,产生了大量的气体,猜想可能是氧气,所以可以用带火星的木条来进行检验,结果带火星的木条复燃,说明该气体是氧气,进一步说明了分液漏斗a中含有过氧化氢溶液;
③等反应完全后打开分液漏斗b,此时将产生的气体通入澄清石灰水中,如果澄清石灰水变浑浊,则说明生成了碳酸钠,进而说明在分液漏斗a的溶液中含有碳酸钠;
结合实验②③可以判断出该污渍爆炸盐的主要成分为过氧化钠.
【反思与评价】:小苏打是碳酸氢钠,它能和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑.
故答案为:
【反思与评价】:NaHCO3+HCl=NaCl+H2O+CO2↑.
②打开分液漏斗a后,产生了大量的气体,猜想可能是氧气,所以可以用带火星的木条来进行检验,结果带火星的木条复燃,说明该气体是氧气,进一步说明了分液漏斗a中含有过氧化氢溶液;
③等反应完全后打开分液漏斗b,此时将产生的气体通入澄清石灰水中,如果澄清石灰水变浑浊,则说明生成了碳酸钠,进而说明在分液漏斗a的溶液中含有碳酸钠;
结合实验②③可以判断出该污渍爆炸盐的主要成分为过氧化钠.
【反思与评价】:小苏打是碳酸氢钠,它能和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑.
故答案为:
| 序号 | 主要操作步骤 | 主要实验现象 | 操作目的 |
| ① | 在广口瓶中加入少量 二氧化锰(黑色固体);在分液漏斗a中加入新配制的“污渍爆炸盐”的饱和水溶液;在分液漏斗b中加入 稀盐酸. | 无 | 检验溶液中是否含有过氧化氢 |
| ② | 打开分液漏斗a的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | 检验过氧化氢分解 |
| 然后 用带火星的木条接近导管口. | 带火星的木条复燃 | 验证生成气体的成分 | |
| 第②步操作得到的结论:“污渍爆炸盐”溶于水生成过氧化氢. | |||
| ③ | 待②步反应停止后,打开分液漏斗b的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | 检验碳酸钠和盐酸反应 |
| 将生成的气体通入 澄清石灰水. | 澄清石灰水变浑浊. | 验证生成气体的成分 | |
点评:记住氧气和二氧化碳的检验方法,掌握过氧化氢和碳酸钠的性质,能够根据物质的性质来选择合适的方法来对物质加以验证,其中检验碳酸盐常用的方法是用稀盐酸和澄清石灰水.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
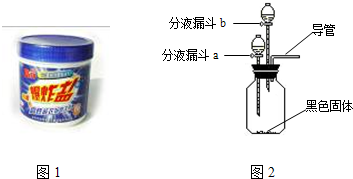
夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”(图1),宣称“含天然活性氧,能在瞬间去除洗衣粉难以除去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:
(1)提出问题
“污渍爆炸盐”的主要化学成分是什么?
(2)查阅相关资料
资料主要信息如下:过碳酸钠俗称固体双氧水,白色结晶颗粒.过碳酸钠溶于水时,分解生成碳酸钠和过氧化氢,目前已成为世界上广泛应用的主要洗涤助剂之一.
(3)猜想
“污渍爆炸盐”的主要化学成分可能是过碳酸钠.
(4)设计与实验
小强同学设计的主要实验装置如图2所示.
请你运用初中所学知识,帮助小强同学完成下列实验报告.
(5)实验的初步结论
小强认为:“污渍爆炸盐”溶于水生成碳酸钠和过氧化氢,“污渍爆炸盐”的主要化学成分是过碳酸钠.
(6)我还想探究的问题过碳酸钠的化学式是怎样的呢?
根据化学反应方程式:X+H2O═Na2CO3+H2O2,推出X的化学式为 .

(1)提出问题
“污渍爆炸盐”的主要化学成分是什么?
(2)查阅相关资料
资料主要信息如下:过碳酸钠俗称固体双氧水,白色结晶颗粒.过碳酸钠溶于水时,分解生成碳酸钠和过氧化氢,目前已成为世界上广泛应用的主要洗涤助剂之一.
(3)猜想
“污渍爆炸盐”的主要化学成分可能是过碳酸钠.
(4)设计与实验
小强同学设计的主要实验装置如图2所示.
请你运用初中所学知识,帮助小强同学完成下列实验报告.
| 序号 | 主要操作步骤 | 主要实验现象 | 化学反应方程式 | |
| ① | 在集气瓶中加入少量 |
|||
| ② | 打开分液漏斗a的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | ||
| 然后 |
||||
| 第②步操作得到的结论:“污渍爆炸盐”溶于水生成过氧化氢 | ||||
| ③ | 待②步反应停止后,打开分液漏斗b的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | ||
| 将生成的气体通入 |
验证生成气体的成分. | |||
| 第③步操作得到的结论:“污渍爆炸盐”溶于水生成碳酸钠 | ||||
小强认为:“污渍爆炸盐”溶于水生成碳酸钠和过氧化氢,“污渍爆炸盐”的主要化学成分是过碳酸钠.
(6)我还想探究的问题过碳酸钠的化学式是怎样的呢?
根据化学反应方程式:X+H2O═Na2CO3+H2O2,推出X的化学式为
 30、夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”,宣称“含天然活性氧,能在瞬间去除洗衣粉难以除去的多种顽固污渍”.小健同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.
30、夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”,宣称“含天然活性氧,能在瞬间去除洗衣粉难以除去的多种顽固污渍”.小健同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究. 28、夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种
28、夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种

 31、夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”,宣称“含天然活性氧,能瞬间去除洗衣粉难以除去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下:
31、夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”,宣称“含天然活性氧,能瞬间去除洗衣粉难以除去的多种顽固污渍”.小强同学对这种“污渍爆炸盐”的化学成分非常感兴趣,对其化学成分进行探究.主要探究过程如下: