摘要:11.氢气的性质(1)物理性质:密度最小的气体.难溶于水 (2)化学性质 ①可燃性:氢气在空气中燃烧 2H2 + O22H2 O 现象:纯净的氢气在空气里安静地燃烧.发出淡蓝色火焰.放出热量 不纯的氢气点燃很可能会爆炸.所以点燃氢气前一定要先检验氢气的纯度. ②还原性:氢气还原氧化铜 H2 +CuO Cu+H2 O 现象:黑色固体逐渐变为光亮的红色固体.管壁有水珠产生 氢气还原氧化铜实验注意事项:“酒精灯迟到早退 .即 开始时要先通入氢气后加热(目的是排净管内空气.防止氢气与管内空气混合受热发生爆炸), 实验结束时要先停止加热.继续通入氢气至试管冷却(防止生成的铜受热被氧化成CuO)现象? (3)氢气的用途:充气球.冶炼金属.高能燃料.化工原料
网址:http://m.1010jiajiao.com/timu3_id_89566[举报]
 碳是组成物质最多的一种元素,碳的化合物是自然界中重要的物质.
碳是组成物质最多的一种元素,碳的化合物是自然界中重要的物质.
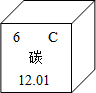
(1)在元素周期表中,碳元素的信息如图所示,碳元素的相对原子质量为________.
(2)过多的CO2排放会造成温室效应,为了减缓大气中CO2含量的增加,目前以下建议可行的是________(填字母序号).
A.电解水生产清洁燃料氢气
B.开发燃煤新技术充分利用燃料
C.禁止使用煤、石油、天然气等燃料
D.开发太阳能、风能、地热能等新能源
(3)甲醇(CH3OH)是一种生物质能燃料,它是无色、略带酒精味的液体,易燃,有毒,密度比水小,能与水相混溶.其中属于甲醇物理性质的是________.
(4)海底埋藏着大量的“可燃冰”,将成为未来的新能源,其主要成分是甲烷水合物,甲烷燃烧的化学方程式为________.
(5)石灰石用途非常广泛.可用来吸收火力发电厂煤燃烧时产生的二氧化硫废气,请将反应的化学方程式补充完整:2CaCO3+2SO2+O2 2CaSO4+________.
2CaSO4+________.
查看习题详情和答案>>
碳是组成物质最多的一种元素,碳的化合物是自然界中重要的物质.
(1)在元素周期表中,碳元素的信息如图所示,碳元素的相对原子质量为______.
(2)过多的CO2排放会造成温室效应,为了减缓大气中CO2含量的增加,目前以下建议可行的是______(填字母序号).
A.电解水生产清洁燃料氢气
B.开发燃煤新技术充分利用燃料
C.禁止使用煤、石油、天然气等燃料
D.开发太阳能、风能、地热能等新能源
(3)甲醇(CH3OH)是一种生物质能燃料,它是无色、略带酒精味的液体,易燃,有毒,密度比水小,能与水相混溶.其中属于甲醇物理性质的是______.
(4)海底埋藏着大量的“可燃冰”,将成为未来的新能源,其主要成分是甲烷水合物,甲烷燃烧的化学方程式为______.
(5)石灰石用途非常广泛.可用来吸收火力发电厂煤燃烧时产生的二氧化硫废气,请将反应的化学方程式补充完整:2CaCO3+2SO2+O2
2CaSO4+______.
查看习题详情和答案>>
(1)在元素周期表中,碳元素的信息如图所示,碳元素的相对原子质量为______.
(2)过多的CO2排放会造成温室效应,为了减缓大气中CO2含量的增加,目前以下建议可行的是______(填字母序号).
A.电解水生产清洁燃料氢气
B.开发燃煤新技术充分利用燃料
C.禁止使用煤、石油、天然气等燃料
D.开发太阳能、风能、地热能等新能源
(3)甲醇(CH3OH)是一种生物质能燃料,它是无色、略带酒精味的液体,易燃,有毒,密度比水小,能与水相混溶.其中属于甲醇物理性质的是______.
(4)海底埋藏着大量的“可燃冰”,将成为未来的新能源,其主要成分是甲烷水合物,甲烷燃烧的化学方程式为______.
(5)石灰石用途非常广泛.可用来吸收火力发电厂煤燃烧时产生的二氧化硫废气,请将反应的化学方程式补充完整:2CaCO3+2SO2+O2
| ||

碳是组成物质最多的一种元素,碳的化合物是自然界中重要的物质.
(1)在元素周期表中,碳元素的信息如图所示,碳元素的相对原子质量为 .
(2)过多的CO2排放会造成温室效应,为了减缓大气中CO2含量的增加,目前以下建议可行的是 (填字母序号).
A.电解水生产清洁燃料氢气
B.开发燃煤新技术充分利用燃料
C.禁止使用煤、石油、天然气等燃料
D.开发太阳能、风能、地热能等新能源
(3)甲醇(CH3OH)是一种生物质能燃料,它是无色、略带酒精味的液体,易燃,有毒,密度比水小,能与水相混溶.其中属于甲醇物理性质的是 .
(4)海底埋藏着大量的“可燃冰”,将成为未来的新能源,其主要成分是甲烷水合物,甲烷燃烧的化学方程式为 .
(5)石灰石用途非常广泛.可用来吸收火力发电厂煤燃烧时产生的二氧化硫废气,请将反应的化学方程式补充完整:2CaCO3+2SO2+O2 2CaSO4+ .
2CaSO4+ .
 查看习题详情和答案>>
查看习题详情和答案>>
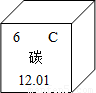
(1)在元素周期表中,碳元素的信息如图所示,碳元素的相对原子质量为 .
(2)过多的CO2排放会造成温室效应,为了减缓大气中CO2含量的增加,目前以下建议可行的是 (填字母序号).
A.电解水生产清洁燃料氢气
B.开发燃煤新技术充分利用燃料
C.禁止使用煤、石油、天然气等燃料
D.开发太阳能、风能、地热能等新能源
(3)甲醇(CH3OH)是一种生物质能燃料,它是无色、略带酒精味的液体,易燃,有毒,密度比水小,能与水相混溶.其中属于甲醇物理性质的是 .
(4)海底埋藏着大量的“可燃冰”,将成为未来的新能源,其主要成分是甲烷水合物,甲烷燃烧的化学方程式为 .
(5)石灰石用途非常广泛.可用来吸收火力发电厂煤燃烧时产生的二氧化硫废气,请将反应的化学方程式补充完整:2CaCO3+2SO2+O2
 2CaSO4+ .
2CaSO4+ . 查看习题详情和答案>>
查看习题详情和答案>>
23、物质的用途与物质的性质密切相关.某同学根据此规律进行归纳、整理,请你帮助他补充填空:
查看习题详情和答案>>
| 物质 | 性质→用途 | 物质 | 性质→用途 |
| 石墨 | 导电性→ 电极 |
氢气 | 密度最小 →填充升空气球 |
| 盐酸 | 酸性→ 除铁锈 |
一氧化碳 | 还原性→ 冶炼金属 |
课本“分解过氧化氢制氧气的反应中二氧化锰的催化作用”以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
| 实验步骤 | 实验现象 |
| Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。 | |
| Ⅳ.分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 | |
(1)A中产生的气体是 。
(2)实验Ⅱ、Ⅲ证明:氧化铁的 和 在反应前后均没有发生变化,可以作过氧化氢溶液分解的催化剂。
(3)写出氧化铁催化过氧化氢溶液分解的符号表达式 。
【实验评价】
(1)实验设计Ⅳ的目的是 。
(2)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是 。
【实验拓展】
(1)查阅资料得知:CuO、CuSO4、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是 (填序号)。
A.MnO2只能作过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其他反应的反应物或生成物
(2)实验创新是中学生最为重要的科学素养。下图是某学校的师生对“MnO2催化H2O2溶液分解实验装置的创新设计”,实验过程如下:
①将一支球形干燥管水平放置,用滴管吸取3ml(密度为1g/ml)质量分数为5%的H2O2加入干燥管的球泡内,再用药匙取0.2gMnO2粉末,加在干燥管的进气管的管壁上。
②点燃橡胶塞上棒香后,塞紧干燥管并将其竖立,观察到带火星的棒香立即复燃。

对该创新实验的评价,你认为不合理的是 (填序号)。
A.实验中所用的仪器、材料及药品均易得到
B.实验使用的药品用量太大
C.反应速度太慢,耽误时间
D.实验现象明显,整个装置好似点燃的灯塔,趣味性强 查看习题详情和答案>>