摘要:12.下列各组物质中.发生化学反应能生成不同产物的是 ( ) ①CO2与NaOH溶液 ②P与Cl2 ③Fe与Cl2 ④Na与O2 ⑤AgNO3溶液与氨水 ⑥C与O2 ⑦CH4与Cl2 ⑧Cu与硝酸 A.除③外 B.除③⑧外 C.除③⑦外 D.除⑥⑦⑧外 [解析] 本题考查了常见物质间的化学反应及反应物相对用量.反应条件对反应产物的影响.CO2与NaOH反应的产物可以是Na2CO3或NaHCO3(CO2过量),P与Cl2反应的产物可以是PCl3或PCl5,Na与O2反应的产物可以是Na2O或Na2O2,AgNO3与NH3·H2O反应的产物可以是AgOH或Ag(NH3)2OH,C与O2反应的产物可以是CO或CO2,CH4与Cl2反应的产物可以是CHCl3.CH2Cl2.CH3Cl及CCl4,Cu与HNO3反应的还原产物可以是NO2.NO. [答案] A
网址:http://m.1010jiajiao.com/timu3_id_88967[举报]
下列各组物质中,发生化学反应能生成不同产物的是
①CO2与NaOH溶液 ②P与Cl2 ③Fe与Cl2 ④Na与O2 ⑤AgNO3溶液与氨水 ⑥C与O2 ⑦CH4与Cl2 ⑧Cu与硝酸
A.除③外 B.除③⑧外 C.除③⑦外 D.除⑥⑦⑧外
查看习题详情和答案>>某化学课外活动小组探究铁粉与水蒸气反应的产物,并用生成的气体来还原氧化铜,最后测定水的组成,拟用如图所示的部分仪器来完成该探究实验(铁架台及酒精灯等仪器可自由选择).

请回答下列问题:
(1)B中所盛的试剂是
(2)请将各接口连接好:k→a,h→
(3)A中发生反应的化学方程式为
(4)实验中需要加热的装置有
(5)用图中所给仪器组装成的装置的不足之处是
查看习题详情和答案>>

请回答下列问题:
(1)B中所盛的试剂是
水
水
,F中所盛的试剂是碱石灰
碱石灰
,E的作用是除去氢气中的水蒸气
除去氢气中的水蒸气
.(2)请将各接口连接好:k→a,h→
i,j→g,f→b,c→d
i,j→g,f→b,c→d
.(3)A中发生反应的化学方程式为
3Fe(g)+4H2O
Fe3O4+4H2↑
| ||
3Fe(g)+4H2O
Fe3O4+4H2↑
.
| ||
(4)实验中需要加热的装置有
A、B、D
A、B、D
(填装置下面的字母,下同),需要称量质量的装置有D、F
D、F
,测定水的组成的步骤为实验前后分别称量D装置和F装置的质量,D装置的两次称量之差即是生成的水中氧元素的质量,F装置的两次称量之差即生成水的质量,用水的质量减去氧元素的质量的氢元素的质量,从而计算出水中氢、氧元素的质量之比
实验前后分别称量D装置和F装置的质量,D装置的两次称量之差即是生成的水中氧元素的质量,F装置的两次称量之差即生成水的质量,用水的质量减去氧元素的质量的氢元素的质量,从而计算出水中氢、氧元素的质量之比
.(5)用图中所给仪器组装成的装置的不足之处是
装置尾部缺少一个能吸收空气中水蒸气和二氧化碳的装置,球星干燥管直接与空气相连,会因吸收了空气中的水蒸气和二氧化碳,而使测定结果不准确,使氢、氧两元素的质量比偏大.
装置尾部缺少一个能吸收空气中水蒸气和二氧化碳的装置,球星干燥管直接与空气相连,会因吸收了空气中的水蒸气和二氧化碳,而使测定结果不准确,使氢、氧两元素的质量比偏大.
.I 化学兴趣小组对用铜制取硫酸铜晶体的试验方案作研究。甲组同学将铜粉投入盛有稀硫酸的容器中,不发生反应。他们向容器底部缓缓鼓入氧气,溶液慢慢变蓝色,若在溶液中放置有些铂丝,反应速率明显加快。此时,其 他组的同学提出方案如下:

(1)甲组试验可用一个化学反应方程式表示为_______________________;使反应变快的可能原因是_______________________;从该反应器溶液(含有少量H2SO4以抑制水解)中取得产品的试验操作步骤应为_____________、_____________、______________,取得产品后的残留物质可循环使用。
(2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染。则在五组方案中,有科学性错误的是______组方案,有污染的是________组方案,无污染但能量消耗较高的是______组方案,因此选择_______组方案最好。
II.另一化学兴趣小组从化学手册上查得硫酸铜500℃在以上按照下式分解:
(2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染。则在五组方案中,有科学性错误的是______组方案,有污染的是________组方案,无污染但能量消耗较高的是______组方案,因此选择_______组方案最好。
II.另一化学兴趣小组从化学手册上查得硫酸铜500℃在以上按照下式分解:
 ,便决定设计试验测定反应生成的SO2、SO3和O2的物质的量,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数。试验可能用到的仪器如下图所示
,便决定设计试验测定反应生成的SO2、SO3和O2的物质的量,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数。试验可能用到的仪器如下图所示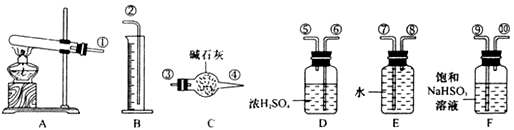
试验测得数据及有关结果如下;
①准确称取6.0g无水CuSO4;
②在试验结束时干燥管总质量增加2.4g;
③测得量筒中水的体积,得出气体在标准状况下的体积为280.mL;
试验结束时,装置F中的溶液只含NaHSO4和NaHSO3
按装置从左到右的方向,各仪器接口连结顺序为:①⑨⑩⑥⑤③④⑧⑦②
试回答下列问题:
(3)装置F的作用是_______________________。
(4)装置D的作用是_______________________。
(5)为减少测量气体体积引起的误差,应注意的事项有:
①装置内气体的温度应恢复到室温。
②_______________________,
③_______________________。
(6)通过 计算,推断出该条件下反应的化学方程式________________。
查看习题详情和答案>>
①准确称取6.0g无水CuSO4;
②在试验结束时干燥管总质量增加2.4g;
③测得量筒中水的体积,得出气体在标准状况下的体积为280.mL;
试验结束时,装置F中的溶液只含NaHSO4和NaHSO3
按装置从左到右的方向,各仪器接口连结顺序为:①⑨⑩⑥⑤③④⑧⑦②
试回答下列问题:
(3)装置F的作用是_______________________。
(4)装置D的作用是_______________________。
(5)为减少测量气体体积引起的误差,应注意的事项有:
①装置内气体的温度应恢复到室温。
②_______________________,
③_______________________。
(6)通过 计算,推断出该条件下反应的化学方程式________________。
Ⅰ.化学兴趣小组对用铜制取硫酸铜晶体的试验方案作研究.甲组同学将铜粉投入盛有稀硫酸的容器中,不发生反应.他们向容器底部缓缓鼓入氧气,溶液慢慢变蓝色,若在溶液中放置有些铂丝,反应速率明显加快.此时,其他组的同学提出方案如下:
乙组:Cu
CuO
CuSO4
丙组:Cu
CuSO4
丁组:Cu
Cu(NO3)2
Cu(OH)2
CuSO4
戊组:Cu
CuSO4
(1)甲组试验可用一个化学反应方程式表示为______;使反应变快的可能原因是______;从该反应器溶液(含有少量H2SO4以抑制水解)中取得产品的试验操作步骤应为______、______、______,取得产品后的残留物质可循环使用.
(2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染.则在五组方案中,有科学性错误的是______ 组方案,有污染的是______组方案,无污染但能量消耗较高的是______组方案,因此选择______组方案最好.
Ⅱ.另一化学兴趣小组从化学手册上查得硫酸铜500℃在以上按照下式分
CuSO4
CuO+SO2↑+SO3↑+O2↑,便决定设计试验测定反应生成的SO2、SO3和O2的物质的量,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数.试验可能用到的仪器如下图所示:
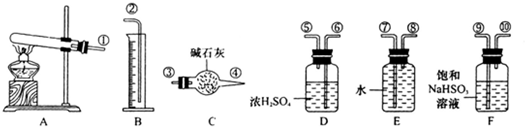
试验测得数据及有关结果如下;
①准确称取6.0g无水CuSO4;②在试验结束时干燥管总质量增加2.4g;③测得量筒中水的体积,得出气体在标准状况下的体积为280mL;试验结束时,装置F中的溶液只含NaHSO4和NaHSO3.按装置从左到右的方向,各仪器接口连结顺序为:①⑨⑩⑥⑤③④⑧⑦②
试回答下列问题:
(1)装置F的作用是______.
(2)装置D的作用是______.
(3)为减少测量气体体积引起的误差,应注意的事项有:
①装置内气体的温度应恢复到室温.
②______,
③______.
(4)通过计算,推断出该条件下反应的化学方程式______.
查看习题详情和答案>>
乙组:Cu
| 氧气 |
| △ |
| 稀H2SO4 |
丙组:Cu
| 硫酸亚铁 |
丁组:Cu
| 硝酸银 |
| 氢氧化钠 |
| 稀硫酸 |
戊组:Cu
| 浓H2SO4 |
| △ |
(1)甲组试验可用一个化学反应方程式表示为______;使反应变快的可能原因是______;从该反应器溶液(含有少量H2SO4以抑制水解)中取得产品的试验操作步骤应为______、______、______,取得产品后的残留物质可循环使用.
(2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染.则在五组方案中,有科学性错误的是______ 组方案,有污染的是______组方案,无污染但能量消耗较高的是______组方案,因此选择______组方案最好.
Ⅱ.另一化学兴趣小组从化学手册上查得硫酸铜500℃在以上按照下式分
CuSO4
| △ |

试验测得数据及有关结果如下;
①准确称取6.0g无水CuSO4;②在试验结束时干燥管总质量增加2.4g;③测得量筒中水的体积,得出气体在标准状况下的体积为280mL;试验结束时,装置F中的溶液只含NaHSO4和NaHSO3.按装置从左到右的方向,各仪器接口连结顺序为:①⑨⑩⑥⑤③④⑧⑦②
试回答下列问题:
(1)装置F的作用是______.
(2)装置D的作用是______.
(3)为减少测量气体体积引起的误差,应注意的事项有:
①装置内气体的温度应恢复到室温.
②______,
③______.
(4)通过计算,推断出该条件下反应的化学方程式______.
Ⅰ.化学兴趣小组对用铜制取硫酸铜晶体的试验方案作研究.甲组同学将铜粉投入盛有稀硫酸的容器中,不发生反应.他们向容器底部缓缓鼓入氧气,溶液慢慢变蓝色,若在溶液中放置有些铂丝,反应速率明显加快.此时,其他组的同学提出方案如下:
乙组:Cu CuO
CuO CuSO4
CuSO4
丙组:Cu CuSO4
CuSO4
丁组:Cu Cu(NO3)2
Cu(NO3)2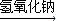 Cu(OH)2
Cu(OH)2 CuSO4
CuSO4
戊组:Cu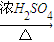 CuSO4
CuSO4
(1)甲组试验可用一个化学反应方程式表示为______;使反应变快的可能原因是______;从该反应器溶液(含有少量H2SO4以抑制水解)中取得产品的试验操作步骤应为______、______、______,取得产品后的残留物质可循环使用.
(2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染.则在五组方案中,有科学性错误的是______ 组方案,有污染的是______组方案,无污染但能量消耗较高的是______组方案,因此选择______组方案最好.
Ⅱ.另一化学兴趣小组从化学手册上查得硫酸铜500℃在以上按照下式分解:
CuSO4 CuO+SO2↑+SO3↑+O2↑,便决定设计试验测定反应生成的SO2、SO3和O2的物质的量,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数.试验可能用到的仪器如下图所示:
CuO+SO2↑+SO3↑+O2↑,便决定设计试验测定反应生成的SO2、SO3和O2的物质的量,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数.试验可能用到的仪器如下图所示:
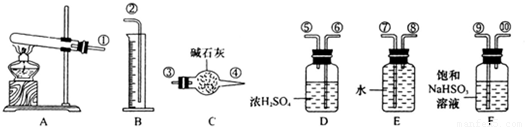
试验测得数据及有关结果如下;
①准确称取6.0g无水CuSO4;②在试验结束时干燥管总质量增加2.4g;③测得量筒中水的体积,得出气体在标准状况下的体积为280mL;试验结束时,装置F中的溶液只含NaHSO4和NaHSO3.按装置从左到右的方向,各仪器接口连结顺序为:①⑨⑩⑥⑤③④⑧⑦②
试回答下列问题:
(1)装置F的作用是______.
(2)装置D的作用是______.
(3)为减少测量气体体积引起的误差,应注意的事项有:
①装置内气体的温度应恢复到室温.
②______,
③______.
(4)通过计算,推断出该条件下反应的化学方程式______ 3CuO+2SO2↑+SO3↑+O2↑ 查看习题详情和答案>>
乙组:Cu
 CuO
CuO CuSO4
CuSO4 丙组:Cu
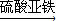 CuSO4
CuSO4丁组:Cu
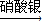 Cu(NO3)2
Cu(NO3)2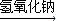 Cu(OH)2
Cu(OH)2 CuSO4
CuSO4戊组:Cu
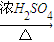 CuSO4
CuSO4(1)甲组试验可用一个化学反应方程式表示为______;使反应变快的可能原因是______;从该反应器溶液(含有少量H2SO4以抑制水解)中取得产品的试验操作步骤应为______、______、______,取得产品后的残留物质可循环使用.
(2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染.则在五组方案中,有科学性错误的是______ 组方案,有污染的是______组方案,无污染但能量消耗较高的是______组方案,因此选择______组方案最好.
Ⅱ.另一化学兴趣小组从化学手册上查得硫酸铜500℃在以上按照下式分解:
CuSO4
 CuO+SO2↑+SO3↑+O2↑,便决定设计试验测定反应生成的SO2、SO3和O2的物质的量,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数.试验可能用到的仪器如下图所示:
CuO+SO2↑+SO3↑+O2↑,便决定设计试验测定反应生成的SO2、SO3和O2的物质的量,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数.试验可能用到的仪器如下图所示:
试验测得数据及有关结果如下;
①准确称取6.0g无水CuSO4;②在试验结束时干燥管总质量增加2.4g;③测得量筒中水的体积,得出气体在标准状况下的体积为280mL;试验结束时,装置F中的溶液只含NaHSO4和NaHSO3.按装置从左到右的方向,各仪器接口连结顺序为:①⑨⑩⑥⑤③④⑧⑦②
试回答下列问题:
(1)装置F的作用是______.
(2)装置D的作用是______.
(3)为减少测量气体体积引起的误差,应注意的事项有:
①装置内气体的温度应恢复到室温.
②______,
③______.
(4)通过计算,推断出该条件下反应的化学方程式______ 3CuO+2SO2↑+SO3↑+O2↑ 查看习题详情和答案>>