网址:http://m.1010jiajiao.com/timu3_id_88508[举报]
(15分)
下图中的A、B、C、D、E、F、G均为有机物
据上图回答问题:
(1)D的化学名称是 。
(2)反应③的化学方程式是: (有机物须用结构简式表示)
(3)B的分子式是:
A的结构简式是 反应的反应类型是
(4)符合下列3个条件的B的同分异构体的数目有 个
ⅰ)含有邻二取代苯环结构、 ⅱ)与B有相同官能团、ⅲ)不与FeCl3溶液发生显色反应。
写出其中任意一个同分异构体的结构简式
(5)G是的工业原料,用化学方程式表示G的一种的工业用途
(14分)下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知:①反应C+G B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中E元素的质量分数为60%。
2F+D,F中E元素的质量分数为60%。
回答问题:
⑴①中反应的化学方程式为 ;
⑵化合物I的电子式为 ,它的空间结构是 ;
⑶将G溶于盐酸,得到的溶液加入一定量的铜粉,写出离子方程式:
⑷C与过量NaOH溶液反应的离子方程式为 ,反应后溶于与过量化合物I反应的离子方程式为 ;
⑸E在I中燃烧观察到的现象是 。
(14分)下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知:①反应C+G B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I
B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是一种常见的温室气体,它和E可以发生反应:2E+I 2F+D,F中E元素的质量分数为60%。
2F+D,F中E元素的质量分数为60%。
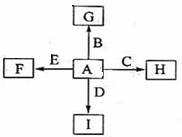
回答问题:
⑴①中反应的化学方程式为 ;
⑵化合物I的电子式为 ,它的空间结构是 ;
⑶将G溶于盐酸,得到的溶液加入一定量的铜粉,写出离子方程式:
⑷C与过量NaOH溶液反应的离子方程式为 ,反应后溶于与过量化合物I反应的离子方程式为 ;
⑸E在I中燃烧观察到的现象是 。
查看习题详情和答案>>
下图中的A、B、C、D、E、F、G均为有机物

据上图回答问题:
(1)D的化学名称是 。
(2)反应③的化学方程式是: (有机物须用结构简式表示)
(3)B的分子式是:
A的结构简式是 反应的反应类型是
(4)符合下列3个条件的B的同分异构体的数目有 个
ⅰ)含有邻二取代苯环结构、 ⅱ)与B有相同官能团、ⅲ)不与FeCl3溶液发生显色反应。
写出其中任意一个同分异构体的结构简式
(5)G是的工业原料,用化学方程式表示G的一种的工业用途
查看习题详情和答案>>根据化学实验仪器的特征和用途回答下列问题:
(1)下列仪器中,根据物质的沸点不同分离物质时需要的是(填编号)________.
①容量瓶 ②普通漏斗 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥滴定管 ⑦燃烧匙 ⑧温度计 ⑨干燥管
(2)实验室里不同化学试剂的保存方法不尽相同.下图中的A、B、C、D、E是常见的一些保存药品的试剂瓶.请把下列常见试剂的序号填写在各试剂瓶下面的括号内.
①NaOH溶液 ②浓硫酸 ③Na2CO3溶液 ④白磷 ⑤大理石 ⑥酒精 ⑦氯水 ⑧浓硝酸

(3)对于下列仪器,用序号回答有关问题:
①容量瓶 ②蒸馏烧瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥蒸发皿 ⑦分液漏斗
对允许加热的仪器,加热时必须垫石棉网的是________;使用时必须检查是否漏水的是________;标有“0”刻度的有________.