网址:http://m.1010jiajiao.com/timu3_id_87997[举报]
 (2008?海南)如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
(2008?海南)如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.(1)写出A在加热条件下与H2反应的化学方程式
| ||
| ||
(2)写出E与A的氢化物反应生成A的化学方程式
(3)写出一个由D生成B的化学方程式
| ||
| ||
| ||
| ||
(4)将5mL 0.10mol?L-1的E溶液与10mL 0.10mol?L-1的NaOH溶液混合.
①写出反应的离子方程式
②反应后溶液的pH
③加热反应后的溶液,其pH
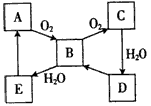
(2)写出一个由D转化成B的化学方程式:_____________。
(3)室温下,将5 mL 0.10 mol·L-1E溶液与10 mL 0.10 mol·L-1 NaOH溶液混合。
①反应后溶液的pH____(填“>”、“<”或“=”)7,理由是________(用离子方程式表 示)。
②将反应后的溶液露置于空气中足够长的时间,其pH将______(填“增大”、“减小”或“不变”),理由是 ______________________。
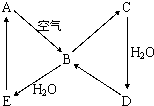 如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
(1)写出A在加热条件下与H2反应的化学方程式______;
(2)写出E与A的氢化物反应生成A的化学方程式______;
(3)写出一个由D生成B的化学方程式______;
(4)将5mL 0.10mol?L-1的E溶液与10mL 0.10mol?L-1的NaOH溶液混合.
①写出反应的离子方程式______;
②反应后溶液的pH______7(填“大于”、“小于”或“等于”),理由是______;
③加热反应后的溶液,其pH______(填“增大”、“不变”或“减小”),理由是______.
查看习题详情和答案>>
(11分)下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。单质A能与某气态单质化合生成化合物B。
(1)若化合物B是造成酸雨的主要污染物,化合物D是组成单质A元素的最高价氧化物对应水化物,则单质A是 (物质名称),将化合物B通入溴水中观察到的现象是 ,该现象说明化合物B具有
性,写出一个由化合物D生成B的化学方程式 ;
(2)若化合物B可用于生产印刷电路板,化合物B和E的组成元素相同,化合物C是组成单质A元素的最高价氧化物对应水化物,则化合物B能用作净水剂的原因是 (用离子方程式表示,下同),印刷电路板生产中发生的主要反应是 ,检验生产废液中是否含有化合物B的实验操作步骤是 。
![]()
![]()

![]() 下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料。
下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料。
![]() (1)写出A在加热条件下与H2反应的化学方程式
(1)写出A在加热条件下与H2反应的化学方程式
![]() _________________________________________________。
_________________________________________________。
![]() (2)写出E与A的氢化物反应生成A的化学方程式 。
(2)写出E与A的氢化物反应生成A的化学方程式 。
![]() (3)写出一个由D生成B的化学方程式 ______________________。
(3)写出一个由D生成B的化学方程式 ______________________。
![]() (4)将5mL0.10mol·L-1的E溶液与10mL0.10 mol·L-1的NaOH溶液混合。
(4)将5mL0.10mol·L-1的E溶液与10mL0.10 mol·L-1的NaOH溶液混合。
![]() ①写出反应的离子方程式________________________;
①写出反应的离子方程式________________________;
![]() ②反应后溶液的pH ______7(填“大于”、“小于”或“等于”),理由是________;
②反应后溶液的pH ______7(填“大于”、“小于”或“等于”),理由是________;
![]() ③加热反应后的溶液,其pH________(填“增大”、“不变”或“减小”),理由是________________________________。
③加热反应后的溶液,其pH________(填“增大”、“不变”或“减小”),理由是________________________________。