摘要:10.诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂.工业上冶炼金属钼的化学原理为: ①2MoS2+7O22MoO3+4SO2,②MoO3+2NH3·H2O===(NH4)2MoO4+H2O,③(NH4)2MoO4+2HCl===H2MoO4↓+2NH4Cl,④H2MoO4MoO3+H2O,⑤用还原剂将MoO3还原成金属钼. 则下列说法正确的是 ( ) A.MoS2煅烧的尾气可以直接排入空气中 B.MoO3既是金属氧化物.也是碱性氧化物 C.H2MoO4是一种强酸 D.利用H2.CO和Al还原等质量的MoO3.所消耗的还原剂的物质的量之比为3∶3∶2 [解析] SO2是大气污染物.不能直接排入空气中.A选项错误,由反应④知MoO3是H2MoO4的酸酐.B选项错误,由反应③和复分解反应制酸的原理知H2MoO4是弱酸.C选项错误,22O.O2. O3.还原等质量的MoO3即失去电子数相等.所以D选项正确. [答案] D
网址:http://m.1010jiajiao.com/timu3_id_87359[举报]
诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为:
 ①2MoS2+7O2====2MoO3+4SO2; ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O;
①2MoS2+7O2====2MoO3+4SO2; ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O;
③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl;④ H2MoO4====MoO3+H2O;
⑤用还原剂将MoO3,还原成金属钼。则下列说法正确的是
A.MoS2煅烧产生的尾气可直接排空
B.MoO3是金属氧化物,也是碱性氧化物
C.H2MoO4是一釉强酸
D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3:3:2
查看习题详情和答案>>
诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为:
①2MoS2 + 7O2=== 2MoO3 + 4SO2; ②MoO3 + 2NH3·H2O === (NH4)2MoO4 + H2O; ③(NH4)2MoO4 + 2HCl ===== H2MoO4↓ + 2NH4Cl;④ H2MoO4==== MoO3 + H2O;
⑤用还原剂将MoO3,还原成金属钼。则下列说法正确的是
A.MoS2煅烧产生的尾气可直接排空
B.MoO3是金属氧化物,也是碱性氧化物
C.H2MoO4是一釉强酸
D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3:3:2
|
⑤用还原剂将MoO3,还原成金属钼。则下列说法正确的是
A.MoS2煅烧产生的尾气可直接排空
B.MoO3是金属氧化物,也是碱性氧化物
C.H2MoO4是一釉强酸
D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3:3:2
诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学反应过程为
①2MoS2+7O2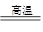 2MoO3+4SO2 ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O ③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl ④H2MoO4
2MoO3+4SO2 ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O ③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl ④H2MoO4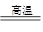 MoO3+H2O
MoO3+H2O
⑤用还原剂将MoO3还原成金属钼。则下列说法正确的是( )。
①2MoS2+7O2
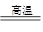 2MoO3+4SO2 ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O ③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl ④H2MoO4
2MoO3+4SO2 ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O ③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl ④H2MoO4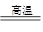 MoO3+H2O
MoO3+H2O⑤用还原剂将MoO3还原成金属钼。则下列说法正确的是( )。
| A.MoS2煅烧产生的尾气可直接排放 |
| B.MoO3是金属氧化物,也是碱性氧化物 |
| C.H2MoO4是一种强酸 |
| D.利用H2、CO和Al分别还原等量的MoO3,所消耗还原剂的物质的量之比为3∶3∶2 |
诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为:
![]() ①2MoS2+7O2====2MoO3+4SO2; ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O;
①2MoS2+7O2====2MoO3+4SO2; ②MoO3+2NH3·H2O=(NH4)2MoO4+H2O;
③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl;④H2MoO4====MoO3+H2O;
⑤用还原剂将MoO3,还原成金属钼。则下列说法正确的是
A.MoS2煅烧产生的尾气可直接排空
B.MoO3是金属氧化物,也是碱性氧化物
C.H2MoO4是一釉强酸
D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3:3:2
查看习题详情和答案>>
诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工业上冶炼钼的化学原理为:
|
③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl;④ H2MoO4====MoO3+H2O;
⑤用还原剂将MoO3,还原成金属钼。则下列说法正确的是
| A.MoS2煅烧产生的尾气可直接排空 |
| B.MoO3是金属氧化物,也是碱性氧化物 |
| C.H2MoO4是一釉强酸 |
| D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3:3:2 |