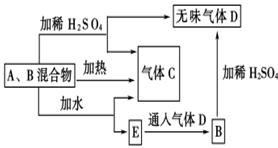
摘要:13.有A.B两种常见化合物组成混合物.其焰色反应均为黄色.其相互转化关系如图. 根据以上关系.回答下列问题: (1)写出A.B.C.D的化学式:A .B .C . D . (2)写出混合物中加水反应的化学方程式: . (3)加热后.若只得到一种固体化合物.则A与B的物质的量之比的最大值为 . [解析] A.B均为钠的化合物.加热.加水.加酸均能产生气体.加热产生气体C.猜测可能含有碳酸钠或碳酸氢钠.加H2SO4产生气体C.D.猜测有Na2O2.C为O2.D为CO2.加水后通入CO2生成B.可推测B为NaHCO3.A为Na2O2.加热NaHCO3分解产生的CO2.H2O(g)都能与Na2O2反应.但可认为CO2优先反应: 2NaHCO3Na2CO3+H2O+CO2↑ 2CO2+2Na2O2===2Na2CO3+O2 要只生成Na2CO3.≤. [答案] (1)Na2O2 NaHCO3 O2 CO2 (2)2Na2O2+2H2O===4NaOH+O2↑ NaOH+NaHCO3===Na2CO3+H2O (3)
网址:http://m.1010jiajiao.com/timu3_id_87033[举报]
有A、B两种常见化合物组成混合物,其焰色反应均为黄色,其相互转化关系如图(其他物质均略去)。
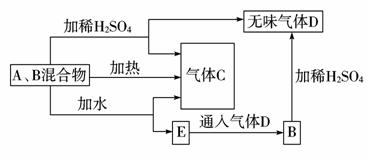
根据以上关系,回答下列问题:
(1)写出A、B、C、D的化学式:A____________,B____________,
C____________,D____________。
(2)写出混合物中加水反应的化学方程式:____________
____________ 。
(3)加热后,若只得到一种固体化合物,则A与B的物质的量之比的最大值为____________。(填数字)
查看习题详情和答案>>(12分)有A、B两种常见化合物组成混合物,其焰色反应均为黄色,其相互转化关系如图(其他物质均略去)。
根据以上关系,回答下列问题:
(1)写出A、B、C、D的化学式:A_______, B__________,C________,D________。
(2)写出混合物中加水反应的化学方程式:
_________________________________________________________________。
查看习题详情和答案>>
(12分)有A、B两种常见化合物组成混合物,其焰色反应均为黄色,其相互转化关系如图(其他物质均略去)。
根据以上关系,回答下列问题:
(1)写出A、B、C、D的化学式:A_______, B__________,C________,D________。
(2)写出混合物中加水反应的化学方程式:
_________________________________________________________________。