摘要:14.金属镁和铝在工农业生产以及人们日常生活中有着十分广泛的用途.某化学兴趣小组的同学们决定对镁.铝及其化合物的性质比较展开探究活动.探究过程中发现了一些“异常 现象. (1)镁条在空气中点燃.发出耀眼的白光,用铝箔在酒精灯上加热.铝箔不能燃烧.铝箔卷缩悬垂却不脱落.将已“卷缩 的铝箔冷却后投入氢氧化钠溶液中.有气体生成.写出“卷缩 铝箔冷却后投入氢氧化钠溶液中发生的离子反应方程式: ① , ② . (2)常温下.在经过砂纸打磨的铝片中取两片质量相等.表面积相同的铝片.分别加入到盛有体积相同.c(H+)相同的稀硫酸和稀盐酸溶液的两支试管中.发现铝片在稀盐酸中产生氢气的速率比在稀硫酸中快. Ⅰ.写出以上反应的离子方程式: . Ⅱ.你认为出现以上现象的可能原因是: 假设① ,假设② . Ⅲ.请设计实验对以上的假设进行验证: ① , ② . [答案] (1)①Al2O3+2OH-+3H2O===2[Al(OH)4]- ②2Al+2OH-+6H2O===2[Al(OH)4]-+3H2↑ (2)Ⅰ.2Al+6H+===2Al3++3H2↑ Ⅱ.假设①:Cl-对铝和酸的反应有促进作用 假设②:SO42-对铝和酸的反应有抑制作用 Ⅲ.①在铝和硫酸反应的容器中加固体氯化钠.看是否加快放出氢气的速率 ②在铝和盐酸反应的容器中加入固体硫酸钠.看是否减慢放出氢气的速率
网址:http://m.1010jiajiao.com/timu3_id_86935[举报]
(1)用酒精灯火焰点燃金属镁条(已除氧化膜)产生的实验现象是 .
(2)用酒精灯火焰加热金属铝箔(已除氧化膜)产生的实验现象是 .
(3)某实验探究小组在进行了上述两个实验后,为了探究两者实验现象的不同,提出了如下假设:
①金属镁和铝的着火点不同;
②金属镁和铝的熔点不同;
③金属镁和铝的沸点不同;
④金属镁和铝在空气或氧气中燃烧的燃烧热不同.
随后他们进行了如下的探究:
【查阅资料】
Ⅰ.几种物质的熔沸点和镁铝的燃烧热
*铝粉在空气中或铝箔在纯氧中均可燃烧
Ⅱ.可燃性固体没有固定的着火点(燃点),其着火点的高低与固体颗粒的大小有关,固体颗粒越小, .例如:面粉分散在空气中遇火可发生爆炸.
【原因探析】
A.镁和铝的熔点很接近且实验所用的是镁条和铝箔,加热它们产生的实验现象不同不可能是由 (填上述4种假设的编号)所引起的.
B.若只从反应生成氧化物放出的热量来分析,应该是 燃烧.
C.若只从镁、铝及其氧化物的熔点和燃烧热来分析,用酒精灯火焰加热镁条(已除氧化膜)的实验现象应是 .
D.用酒精灯火焰加热铝箔(已除氧化膜)产生实验现象的主要原因是 .
E.镁条能燃烧,铝箔不能燃烧的主要原因是由 (填上述4种假设的编号)所引起的.加热和反应产生的热量使温度超过 的沸点, 而被燃烧并产生火焰.
查看习题详情和答案>>
(2)用酒精灯火焰加热金属铝箔(已除氧化膜)产生的实验现象是
(3)某实验探究小组在进行了上述两个实验后,为了探究两者实验现象的不同,提出了如下假设:
①金属镁和铝的着火点不同;
②金属镁和铝的熔点不同;
③金属镁和铝的沸点不同;
④金属镁和铝在空气或氧气中燃烧的燃烧热不同.
随后他们进行了如下的探究:
【查阅资料】
Ⅰ.几种物质的熔沸点和镁铝的燃烧热
| Mg | Al | MgO | Al2O3 | |
| 熔点/℃ | 648.8 | 660.4 | 2852 | 2072 |
| 沸点/℃ | 1107 | 2467 | 3600 | 2980 |
| 燃烧热*/kJ?mol-1 | 601.8 | 833.6 |
Ⅱ.可燃性固体没有固定的着火点(燃点),其着火点的高低与固体颗粒的大小有关,固体颗粒越小,
【原因探析】
A.镁和铝的熔点很接近且实验所用的是镁条和铝箔,加热它们产生的实验现象不同不可能是由
B.若只从反应生成氧化物放出的热量来分析,应该是
C.若只从镁、铝及其氧化物的熔点和燃烧热来分析,用酒精灯火焰加热镁条(已除氧化膜)的实验现象应是
D.用酒精灯火焰加热铝箔(已除氧化膜)产生实验现象的主要原因是
E.镁条能燃烧,铝箔不能燃烧的主要原因是由
(1)用酒精灯火焰点燃金属镁条(已除氧化膜)产生的实验现象是______.
(2)用酒精灯火焰加热金属铝箔(已除氧化膜)产生的实验现象是______.
(3)某实验探究小组在进行了上述两个实验后,为了探究两者实验现象的不同,提出了如下假设:
①金属镁和铝的着火点不同;
②金属镁和铝的熔点不同;
③金属镁和铝的沸点不同;
④金属镁和铝在空气或氧气中燃烧的燃烧热不同.
随后他们进行了如下的探究:
【查阅资料】
Ⅰ.几种物质的熔沸点和镁铝的燃烧热
| Mg | Al | MgO | Al2O3 | |
| 熔点/℃ | 648.8 | 660.4 | 2852 | 2072 |
| 沸点/℃ | 1107 | 2467 | 3600 | 2980 |
| 燃烧热*/kJ?mol-1 | 601.8 | 833.6 |
Ⅱ.可燃性固体没有固定的着火点(燃点),其着火点的高低与固体颗粒的大小有关,固体颗粒越小,______.例如:面粉分散在空气中遇火可发生爆炸.
【原因探析】
A.镁和铝的熔点很接近且实验所用的是镁条和铝箔,加热它们产生的实验现象不同不可能是由______(填上述4种假设的编号)所引起的.
B.若只从反应生成氧化物放出的热量来分析,应该是______燃烧.
C.若只从镁、铝及其氧化物的熔点和燃烧热来分析,用酒精灯火焰加热镁条(已除氧化膜)的实验现象应是______.
D.用酒精灯火焰加热铝箔(已除氧化膜)产生实验现象的主要原因是______.
E.镁条能燃烧,铝箔不能燃烧的主要原因是由______(填上述4种假设的编号)所引起的.加热和反应产生的热量使温度超过______的沸点,______而被燃烧并产生火焰. 查看习题详情和答案>>
(I)多项选择题
下列有关化工生产的说法中不正确的是
A.工业上用电解熔融的氯化物的方法制备金属镁和铝
B.适当提高合成氨原料气中N2的含量,可提高H2的转化率
C.从安全运输上看,硫酸厂靠近硫酸消费中心比靠近原料产地更为有利
D.利用反应NaCl(饱和)+CO2+NH3+H2O=NH4Cl+NaHCO3↓制取NaHCO3时,应在NaCl饱和溶液中先通入过量CO2再通入过量的NH3
E.硫酸厂生产时常采有高压条件提高SO2的转化率
(II)
过碳酸钠(2Na2CO3?3H2O2)俗称固体双氧水,被大量用于洗涤、印染、纺织、造纸、医药卫生等领域中.它的制备原理和路线如下:
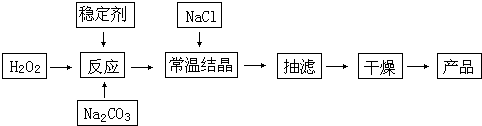
试回答下列问题:
(1)与过碳酸钠的用途相关的化学性质是
A.MnO2 B. H2S C.稀硫酸 D. NaHCO3
(2)加入NaCl的作用是
(3)工业纯碱中含有Fe3+等杂质,加入稳定剂的作用是与生成稳定的配合物.Fe3+的不良影响是
(4)反应的最佳温度控制在15~25℃,温度偏高时造成产率偏低的可能原因是
(5)有人想用过碳酸钠测定氢溴酸的浓度.若一定量的过碳酸钠与100mL氢溴酸溶液恰好完全反应,在标准状况下产生448mL气体,则所用氢溴酸的浓度为
查看习题详情和答案>>
下列有关化工生产的说法中不正确的是
ADE
ADE
A.工业上用电解熔融的氯化物的方法制备金属镁和铝
B.适当提高合成氨原料气中N2的含量,可提高H2的转化率
C.从安全运输上看,硫酸厂靠近硫酸消费中心比靠近原料产地更为有利
D.利用反应NaCl(饱和)+CO2+NH3+H2O=NH4Cl+NaHCO3↓制取NaHCO3时,应在NaCl饱和溶液中先通入过量CO2再通入过量的NH3
E.硫酸厂生产时常采有高压条件提高SO2的转化率
(II)
过碳酸钠(2Na2CO3?3H2O2)俗称固体双氧水,被大量用于洗涤、印染、纺织、造纸、医药卫生等领域中.它的制备原理和路线如下:

试回答下列问题:
(1)与过碳酸钠的用途相关的化学性质是
强氧化性
强氧化性
,下列四种物质可使过碳酸钠较快失效的是ABC
ABC
A.MnO2 B. H2S C.稀硫酸 D. NaHCO3
(2)加入NaCl的作用是
降低2Na2CO3?3H2O2溶解度,析出更多晶体
降低2Na2CO3?3H2O2溶解度,析出更多晶体
(3)工业纯碱中含有Fe3+等杂质,加入稳定剂的作用是与生成稳定的配合物.Fe3+的不良影响是
催化双氧水的分解
催化双氧水的分解
,反应方程式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
(4)反应的最佳温度控制在15~25℃,温度偏高时造成产率偏低的可能原因是
温度高时双氧水易分解
温度高时双氧水易分解
,温度偏低时造成产率偏低的可能原因是温度低时反应慢
温度低时反应慢
,而该流程中还是遗漏了一步操作,造成产品产率偏低,这步操作名称是洗涤
洗涤
.(5)有人想用过碳酸钠测定氢溴酸的浓度.若一定量的过碳酸钠与100mL氢溴酸溶液恰好完全反应,在标准状况下产生448mL气体,则所用氢溴酸的浓度为
1
1
mol/L.(已知:H2O2+2HBr=Br2+2H2O)