摘要:28.已知在Rt△OAB中.∠OAB=900.∠BOA=300.OA=4.现以O为坐标原点.OA所在直线为轴.建立如图所示的平面直角坐标系.点B在第一象限内.将Rt△OAB沿OB折叠后.点A落在第一象限内的点C处. (1)求点C的坐标, (2)若抛物线(≠0)经过C.A两点.求此抛物线的解析式, (3)若⊙的半径为.圆心在(2)的抛物线上运动.问:是否存在这样的点P.使得⊙与两坐标轴都相切?若存在.请求出此时⊙半径的值,若不存在.请说明理由.
网址:http://m.1010jiajiao.com/timu3_id_8679[举报]
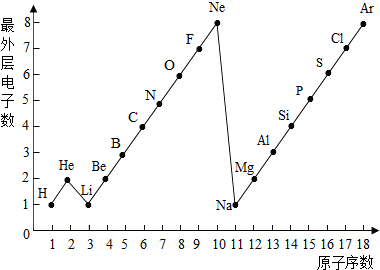 图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如右图.试回答:
图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如右图.试回答:(1)图中与N元素原子最外层电子数相同的元素是
P
P
;在3一10号元素原子最外层电子数变化的趋势是由1增加到8
由1增加到8
;(2)图中He与Ne、Ar原子最外层电子数不一样,但都处在每周期的结尾处,从原子结构上分析其原因
He排2个电子,最外层也达到相对稳定结构
He排2个电子,最外层也达到相对稳定结构
;(3)原子的核外电子排布,特别是最外层的电子数目,与元素的化学性质有密切关系.
钠原子核内有11个质子,原子核外有
11
11
电子钠原子在化学反应中易失
失
(填“得”或“失”)电子钠元素和氯元素所组成化合物的化学式为NaCl
NaCl
(4)已知在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低.现探究钾元素(原子序数为19)单质与水反应的生成物.甲同学猜想生成物为KOH和H2;乙同学猜想生成物为KOH和O2,你认为
乙
乙
同学的猜想不合理.(2007?广东)某小组同学对废干电池筒内的黑色固体(内含有MnO2、NH4Cl、ZnCl2等)进行了如图所示的实验:

(1)操作②的名称是
(2)操作③灼烧滤渣黑色固体时,会产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中除含有MnO2外,还存在的物质是
(3)操作④的试管中产生的气体使带火星的木条复燃,则该气体为
(4)请你写出用pH试纸检测滤液酸碱性的具体操作:
(5)已知在氯化锌溶液中逐滴滴入稀氨水,先生成Zn(OH)2白色沉淀,然后溶解生成可溶
于水的Zn(NH3)4Cl2.同学们对操作②的滤液中的成分进行探究.
查看习题详情和答案>>

(1)操作②的名称是
过滤
过滤
,该操作中玻璃棒的作用是引流
引流
.(2)操作③灼烧滤渣黑色固体时,会产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中除含有MnO2外,还存在的物质是
炭(或碳、或C)
炭(或碳、或C)
.(3)操作④的试管中产生的气体使带火星的木条复燃,则该气体为
氧气或O2
氧气或O2
.(4)请你写出用pH试纸检测滤液酸碱性的具体操作:
剪取小段pH试纸放在洁净表面皿(或点滴板、玻璃片)上,用玻璃棒蘸取(或用胶头滴管取)少许滤液(或溶液、待测液)点(或滴)在pH试纸上,试纸变色后再与比色卡比较读出相应数值
剪取小段pH试纸放在洁净表面皿(或点滴板、玻璃片)上,用玻璃棒蘸取(或用胶头滴管取)少许滤液(或溶液、待测液)点(或滴)在pH试纸上,试纸变色后再与比色卡比较读出相应数值
.(5)已知在氯化锌溶液中逐滴滴入稀氨水,先生成Zn(OH)2白色沉淀,然后溶解生成可溶
于水的Zn(NH3)4Cl2.同学们对操作②的滤液中的成分进行探究.
| 验证方法 | 现象 | 判断 | |
| 猜想I:主要成分 为氯化铵 |
取少量滤液加入NaOH固体,并加热 | 未闻到明显的氨的刺激性气味 | 猜想I不成立 猜想I不成立 |
| 猜想Ⅱ:主要成分 为氯化锌 |
取少量滤液逐滴滴入稀氨水 取少量滤液逐滴滴入稀氨水 |
先有白色沉淀、后溶解 先有白色沉淀、后溶解 |
猜想Ⅱ成立 |
| 由上述实验得出的结论是:滤液中 主要为氯化锌,其中可能含少量的氯化铵 主要为氯化锌,其中可能含少量的氯化铵 | |||