题目内容
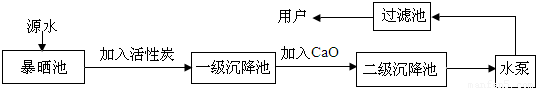
(2007?广东)某小组同学对废干电池筒内的黑色固体(内含有MnO2、NH4Cl、ZnCl2等)进行了如图所示的实验:

(1)操作②的名称是
(2)操作③灼烧滤渣黑色固体时,会产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中除含有MnO2外,还存在的物质是
(3)操作④的试管中产生的气体使带火星的木条复燃,则该气体为
(4)请你写出用pH试纸检测滤液酸碱性的具体操作:
(5)已知在氯化锌溶液中逐滴滴入稀氨水,先生成Zn(OH)2白色沉淀,然后溶解生成可溶
于水的Zn(NH3)4Cl2.同学们对操作②的滤液中的成分进行探究.

(1)操作②的名称是
过滤
过滤
,该操作中玻璃棒的作用是引流
引流
.(2)操作③灼烧滤渣黑色固体时,会产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中除含有MnO2外,还存在的物质是
炭(或碳、或C)
炭(或碳、或C)
.(3)操作④的试管中产生的气体使带火星的木条复燃,则该气体为
氧气或O2
氧气或O2
.(4)请你写出用pH试纸检测滤液酸碱性的具体操作:
剪取小段pH试纸放在洁净表面皿(或点滴板、玻璃片)上,用玻璃棒蘸取(或用胶头滴管取)少许滤液(或溶液、待测液)点(或滴)在pH试纸上,试纸变色后再与比色卡比较读出相应数值
剪取小段pH试纸放在洁净表面皿(或点滴板、玻璃片)上,用玻璃棒蘸取(或用胶头滴管取)少许滤液(或溶液、待测液)点(或滴)在pH试纸上,试纸变色后再与比色卡比较读出相应数值
.(5)已知在氯化锌溶液中逐滴滴入稀氨水,先生成Zn(OH)2白色沉淀,然后溶解生成可溶
于水的Zn(NH3)4Cl2.同学们对操作②的滤液中的成分进行探究.
| 验证方法 | 现象 | 判断 | |
| 猜想I:主要成分 为氯化铵 |
取少量滤液加入NaOH固体,并加热 | 未闻到明显的氨的刺激性气味 | 猜想I不成立 猜想I不成立 |
| 猜想Ⅱ:主要成分 为氯化锌 |
取少量滤液逐滴滴入稀氨水 取少量滤液逐滴滴入稀氨水 |
先有白色沉淀、后溶解 先有白色沉淀、后溶解 |
猜想Ⅱ成立 |
| 由上述实验得出的结论是:滤液中 主要为氯化锌,其中可能含少量的氯化铵 主要为氯化锌,其中可能含少量的氯化铵 | |||
分析:(1)依据图示判断操作的名称,依据玻璃棒在该项操作中的作用分析解答.
(2)根据固体的颜色和化学性质分析该物质.
(3)依据常见的能支持燃烧的气体是氧气分析解答;
(4)依据pH试纸的检测方法分析解答;
(5)依据铵根离子的检验方法以及题干中的氯化锌与氨水的反应分析解答即可;
(2)根据固体的颜色和化学性质分析该物质.
(3)依据常见的能支持燃烧的气体是氧气分析解答;
(4)依据pH试纸的检测方法分析解答;
(5)依据铵根离子的检验方法以及题干中的氯化锌与氨水的反应分析解答即可;
解答:解:(1)由图示可知该操作是过滤操作,过滤操作中,玻璃棒的作用是引流.
(2)使澄清石灰水变浑浊的气体有二氧化碳和二氧化硫,二氧化碳可由黑色的碳单质灼烧制得,二氧化硫可由淡黄色的硫单质灼烧制得,所以该黑色物质是碳单质.
(3)有所学可知能使带火星的木条复燃的气体是氧气.
(4)pH试纸的使用方法是:取一小块试纸在表面皿或玻璃片上,用洁净干燥的玻璃棒蘸取待测液点滴于试纸的中部,观察变化稳定后的颜色,与标准比色卡对比,判断溶液的性质.
(5)铵根离子的检验:铵根离子能和强碱在加热条件下反应生成氨气,氨气具有刺激性气味,未闻到明显的氨的刺激性气味,就说明有铵根离子不是大量存在.
氯化锌的测量则是利用题干中的信息:氯化锌溶液中逐滴滴入稀氨水,先生成Zn(OH)2白色沉淀,然后溶解生成可溶于水的Zn(NH3)4Cl2.从而依据反应的现象待测液中加入氨水,先有白色沉淀、后溶解,则证明氯化锌的存在;
故答案为:
(1)过滤; 引流;(2)炭(或碳、或C);
(3)氧气或O2;
(4)剪取小段pH试纸放在洁净表面皿(或点滴板、玻璃片)上,用玻璃棒蘸取(或用胶头滴管取)少许滤液(或溶液、待测液)点(或滴)在pH试纸上,试纸变色后再与比色卡比较读出相应数值.
(5)
(2)使澄清石灰水变浑浊的气体有二氧化碳和二氧化硫,二氧化碳可由黑色的碳单质灼烧制得,二氧化硫可由淡黄色的硫单质灼烧制得,所以该黑色物质是碳单质.
(3)有所学可知能使带火星的木条复燃的气体是氧气.
(4)pH试纸的使用方法是:取一小块试纸在表面皿或玻璃片上,用洁净干燥的玻璃棒蘸取待测液点滴于试纸的中部,观察变化稳定后的颜色,与标准比色卡对比,判断溶液的性质.
(5)铵根离子的检验:铵根离子能和强碱在加热条件下反应生成氨气,氨气具有刺激性气味,未闻到明显的氨的刺激性气味,就说明有铵根离子不是大量存在.
氯化锌的测量则是利用题干中的信息:氯化锌溶液中逐滴滴入稀氨水,先生成Zn(OH)2白色沉淀,然后溶解生成可溶于水的Zn(NH3)4Cl2.从而依据反应的现象待测液中加入氨水,先有白色沉淀、后溶解,则证明氯化锌的存在;
故答案为:
(1)过滤; 引流;(2)炭(或碳、或C);
(3)氧气或O2;
(4)剪取小段pH试纸放在洁净表面皿(或点滴板、玻璃片)上,用玻璃棒蘸取(或用胶头滴管取)少许滤液(或溶液、待测液)点(或滴)在pH试纸上,试纸变色后再与比色卡比较读出相应数值.
(5)
猜想I不成立 | |||
| 取少量滤液逐滴滴入稀氨水 | 先有白色沉淀、后溶解 | ||
| 主要为氯化锌,其中含少量的氯化铵 | |||
点评:此题涉及到的知识点较多,主要是围绕电池展开的,是对干电池物质成分的探究,充分利用题干中的信息和所学的有关知识是解题的关键,此题对培养学生分析问题的能力有一定帮助.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
(2007?广东)某化学兴趣小组用化学方法测定一种钢样品中铁的含量.同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中.在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如下表:
(1)反应中产生氢气______克,这种钢样品中铁的含量是多少?(精确到0.1%)______
(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;0.6%~2%为高碳钢.假设残留在烧杯中的黑色固体全部是炭,则这种钢属于______.
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻.可是他们将一定量的钢样品灼烧后,发现质量反而增加了很多.原因是______.
| 反应时间 | t | t1 | t2 | t3 |
| 烧杯和药品质量/g | 25.7 | 25.6 | 25.5 | 25.5 |
(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;0.6%~2%为高碳钢.假设残留在烧杯中的黑色固体全部是炭,则这种钢属于______.
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻.可是他们将一定量的钢样品灼烧后,发现质量反而增加了很多.原因是______.