摘要: 甲.乙两位同学分别用下图装置测定空气中氧气的体积分数: (1)甲同学的实验中.当红磷和木炭充分燃烧并冷却到室温后.打开止水夹.看到的主要现象是: , (2)乙同学的实验中.当红磷和木炭充分燃烧并冷却到室温后.打开止水夹.看到的主要现象是: , (3)如果甲.乙两位同学看到的主要现象有所不同.请简单解释其原因: 甲 ,乙 .
网址:http://m.1010jiajiao.com/timu3_id_8538[举报]
甲、乙两位同学分别用下图装置测定空气中氧气的体积分数:
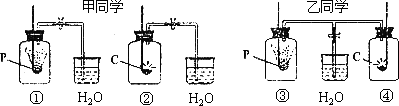
(1)甲同学的实验中,当红磷和木炭充分燃烧并冷却到室温后,打开止水夹,看到的主要现象是:________;
(2)乙同学的实验中,当红磷和木炭充分燃烧并冷却到室温后,打开止水夹,看到的主要现象是:________;
(3)如果甲、乙两位同学看到的主要现象有所不同,请简单解释其原因:甲________;乙________.
 甲、乙两位同学查阅资料知:CH4和CO两种气体均具有可燃性和还原性,他们想对CH4的还原性进行研究,设计了如图所示的装置(假设药品都是足量的)
甲、乙两位同学查阅资料知:CH4和CO两种气体均具有可燃性和还原性,他们想对CH4的还原性进行研究,设计了如图所示的装置(假设药品都是足量的)(1)甲同学对CH4还原CuO的产物提出了以下假设:
假设1:Cu、CO、CO2;
假设2:Cu、CO、H2O;
假设3:Cu、CO2、H2O;
假设4:Cu、CO、CO2、H2O
其中假设
假设1
假设1
明显不合理.(2)为了判断上述哪种假设是正确的,甲同学设计了以下几个实验步骤:
①通入CH4;②停止通CH4;③点燃酒精灯加热;④停止加热;⑤连接并检验装置的质量;⑥分别称量装置A、B、C在反应前的质量;⑦分别称量装置A、B、C在反应后的质量.
该实验合理的操作顺序是
⑥⑤①③④②⑦
⑥⑤①③④②⑦
(填序号).乙同学在对上述方案进行分析后认为该方案还增加一步操作才更加完善,该操作步骤是
将尾气用塑料袋收集起来
将尾气用塑料袋收集起来
.若将合理操作顺序中的第3步和第4步交换顺序,造成的后果是引起爆炸
引起爆炸
,实验过程中能观察到的现象是玻璃管中黑色固体变红
玻璃管中黑色固体变红
.(3)实验过程中记录的实验数据如下:
| A | B | C | |
| 实验前装置的质量 | 150 | 156.6 | 256.8 |
| 实验后装置的质量 | 147.2 | 158.4 | 257.9 |
4
4
合理,相应的化学方程式为:2CH4+7CuO
7Cu+CO+CO2+4H2O
| ||
2CH4+7CuO
7Cu+CO+CO2+4H2O
.
| ||
(4)有同学认为只需要记录B和C两装置在实验前后的质量变化也可以判断哪种假设是合理的,你认为对吗?说明理由:
对,因为甲烷中的碳、氢的质量比是一定的
对,因为甲烷中的碳、氢的质量比是一定的
.甲、乙两个研究性学习小组分别制备氨气,并利用氨气的性质(氨气与灼热的氧化铜反应,生成铜、水和氮气)来验证分子中氮、氢原子个数比,设计了如下实验流程:
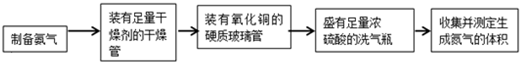
实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜.反应完成后,黑色的氧化铜转化为红色的铜.
下图A、B、C为甲、乙两小组制备氨气时可能用到的装置,D为盛有足量浓硫酸的洗气瓶.
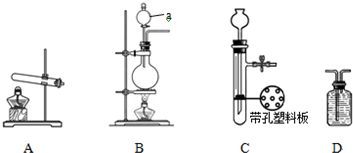
甲小组测得:反应前氧化铜的质量为m1g、氧化铜反应后转化成的铜的质量为m2g;生成的氮气在标准状况下的体积V1L(已知标准状况下,22.4L氮气的质量是28g).
乙小组测得:洗气前装置D的质量m3g、洗气后装置后D的质量m4g;生成的氮气在标准状况下的体积V2L.
请回答下列问题:
(1)写出仪器a的名称:
(2)检查A装置气密性的具体操作方法是
(3)甲、乙两小组选择了不同方法制备氨气,请将实验装置的字母编号和制备原理填写在下表空格中.
(4)甲小组用所测数据计算出氨分子中氮、氢的原子个数之比为
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比小于理论值,其原因是
查看习题详情和答案>>

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜.反应完成后,黑色的氧化铜转化为红色的铜.
下图A、B、C为甲、乙两小组制备氨气时可能用到的装置,D为盛有足量浓硫酸的洗气瓶.

甲小组测得:反应前氧化铜的质量为m1g、氧化铜反应后转化成的铜的质量为m2g;生成的氮气在标准状况下的体积V1L(已知标准状况下,22.4L氮气的质量是28g).
乙小组测得:洗气前装置D的质量m3g、洗气后装置后D的质量m4g;生成的氮气在标准状况下的体积V2L.
请回答下列问题:
(1)写出仪器a的名称:
分液漏斗
分液漏斗
(2)检查A装置气密性的具体操作方法是
连接导管,将导管插入水中,用手紧握试管,导管口有气泡产生;松开手后,导管内有水回流并形成一段稳定的水柱
连接导管,将导管插入水中,用手紧握试管,导管口有气泡产生;松开手后,导管内有水回流并形成一段稳定的水柱
.(3)甲、乙两小组选择了不同方法制备氨气,请将实验装置的字母编号和制备原理填写在下表空格中.
| 实验装置 | 实验药品 | 制备原理 | |
| 甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为 ① (NH4)2SO4+Ca(OH)2═2NH3↑+2H2O+CaSO4 (NH4)2SO4+Ca(OH)2═2NH3↑+2H2O+CaSO4 |
| 乙小组 | ② B B |
浓氨水、氢氧化钠 |
5V1:7(m1-m2)
5V1:7(m1-m2)
.(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比小于理论值,其原因是
洗气瓶D中的浓硫酸不但吸收了反应生成的水,还吸收了未反应的氨气,从而使计算的氢的量偏高
洗气瓶D中的浓硫酸不但吸收了反应生成的水,还吸收了未反应的氨气,从而使计算的氢的量偏高
. 为此,乙小组在原有实验流程的基础上,在洗气瓶D前
洗气瓶D前
的位置增加了一个装有足量药品的实验仪器,重新实验.根据实验前后该药品的质量变化及生成氮气的体积,也得出了合理的实验结果.该药品的名称是碱石灰(或无水硫酸铜、氢氧化钠、氧化钙等)
碱石灰(或无水硫酸铜、氢氧化钠、氧化钙等)
.
甲、乙两个研究性学习小组分别制备氨气,并利用氨气的性质(氨气与灼热的氧化铜反应,生成铜、水和氮气)来验证分子中氮、氢原子个数比,设计了如下实验流程:

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜.反应完成后,黑色的氧化铜转化为红色的铜.
下图A、B、C为甲、乙两小组制备氨气时可能用到的装置,D为盛有足量浓硫酸的洗气瓶.

甲小组测得:反应前氧化铜的质量为m1g、氧化铜反应后转化成的铜的质量为m2g;生成的氮气在标准状况下的体积V1L(已知标准状况下,22.4L氮气的质量是28g).
乙小组测得:洗气前装置D的质量m3g、洗气后装置后D的质量m4g;生成的氮气在标准状况下的体积V2L.
请回答下列问题:
(1)写出仪器a的名称:
(2)检查A装置气密性的具体操作方法是 .
(3)甲、乙两小组选择了不同方法制备氨气,请将实验装置的字母编号和制备原理填写在下表空格中.
(4)甲小组用所测数据计算出氨分子中氮、氢的原子个数之比为 .
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比小于理论值,其原因是 . 为此,乙小组在原有实验流程的基础上,在 的位置增加了一个装有足量药品的实验仪器,重新实验.根据实验前后该药品的质量变化及生成氮气的体积,也得出了合理的实验结果.该药品的名称是 . 查看习题详情和答案>>

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜.反应完成后,黑色的氧化铜转化为红色的铜.
下图A、B、C为甲、乙两小组制备氨气时可能用到的装置,D为盛有足量浓硫酸的洗气瓶.

甲小组测得:反应前氧化铜的质量为m1g、氧化铜反应后转化成的铜的质量为m2g;生成的氮气在标准状况下的体积V1L(已知标准状况下,22.4L氮气的质量是28g).
乙小组测得:洗气前装置D的质量m3g、洗气后装置后D的质量m4g;生成的氮气在标准状况下的体积V2L.
请回答下列问题:
(1)写出仪器a的名称:
(2)检查A装置气密性的具体操作方法是 .
(3)甲、乙两小组选择了不同方法制备氨气,请将实验装置的字母编号和制备原理填写在下表空格中.
| 实验装置 | 实验药品 | 制备原理 | |
| 甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为 ① |
| 乙小组 | ② | 浓氨水、氢氧化钠 |
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比小于理论值,其原因是 . 为此,乙小组在原有实验流程的基础上,在 的位置增加了一个装有足量药品的实验仪器,重新实验.根据实验前后该药品的质量变化及生成氮气的体积,也得出了合理的实验结果.该药品的名称是 . 查看习题详情和答案>>
甲、乙两个研究性学习小组分别制备氨气,并利用氨气的性质(氨气与灼热的氧化铜反应,生成铜、水和氮气)来验证分子中氮、氢原子个数比,设计了如下实验流程:

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜.反应完成后,黑色的氧化铜转化为红色的铜.
下图A、B、C为甲、乙两小组制备氨气时可能用到的装置,D为盛有足量浓硫酸的洗气瓶.

甲小组测得:反应前氧化铜的质量为m1g、氧化铜反应后转化成的铜的质量为m2g;生成的氮气在标准状况下的体积V1L(已知标准状况下,22.4L氮气的质量是28g).
乙小组测得:洗气前装置D的质量m3g、洗气后装置后D的质量m4g;生成的氮气在标准状况下的体积V2L.
请回答下列问题:
(1)写出仪器a的名称:______
(2)检查A装置气密性的具体操作方法是______.
(3)甲、乙两小组选择了不同方法制备氨气,请将实验装置的字母编号和制备原理填写在下表空格中.
(4)甲小组用所测数据计算出氨分子中氮、氢的原子个数之比为______.
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比小于理论值,其原因是______.为此,乙小组在原有实验流程的基础上,在______的位置增加了一个装有足量药品的实验仪器,重新实验.根据实验前后该药品的质量变化及生成氮气的体积,也得出了合理的实验结果.该药品的名称是______.
查看习题详情和答案>>

实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜.反应完成后,黑色的氧化铜转化为红色的铜.
下图A、B、C为甲、乙两小组制备氨气时可能用到的装置,D为盛有足量浓硫酸的洗气瓶.

甲小组测得:反应前氧化铜的质量为m1g、氧化铜反应后转化成的铜的质量为m2g;生成的氮气在标准状况下的体积V1L(已知标准状况下,22.4L氮气的质量是28g).
乙小组测得:洗气前装置D的质量m3g、洗气后装置后D的质量m4g;生成的氮气在标准状况下的体积V2L.
请回答下列问题:
(1)写出仪器a的名称:______
(2)检查A装置气密性的具体操作方法是______.
(3)甲、乙两小组选择了不同方法制备氨气,请将实验装置的字母编号和制备原理填写在下表空格中.
| 实验装置 | 实验药品 | 制备原理 | |
| 甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为 ①______ |
| 乙小组 | ②______ | 浓氨水、氢氧化钠 |
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比小于理论值,其原因是______.为此,乙小组在原有实验流程的基础上,在______的位置增加了一个装有足量药品的实验仪器,重新实验.根据实验前后该药品的质量变化及生成氮气的体积,也得出了合理的实验结果.该药品的名称是______.