摘要:4.对实验Ⅰ-Ⅳ的实验现象预测正确的是( ) A.实验Ⅰ:液体分层.下层呈无色 B.实验Ⅱ:烧杯中先出现白色沉淀.后溶解 C.实验Ⅲ:试管中溶液颜色变为红色 D.实验Ⅳ:放置一段时间后.饱和CuSO4溶液中出现蓝色晶体 解析:本题考查化学实验.意在考查考生对化学实验的操作和分析能力.实验Ⅰ中振荡静置.由于碘在CCl4中的溶解度大于在水中的溶解度.又CCl4的密度大于水的密度且二者互不相溶.故上层为水.几乎无色.下层为碘的四氯化碳溶液.显紫红色.A项错误,实验Ⅱ中NH4Cl和Ca(OH)2共热时生成NH3.NH3通入AlCl3溶液中产生Al(OH)3白色沉淀.但沉淀不溶于氨水.B项错误,实验Ⅲ中Fe3+遇到SCN-显红色.C项正确,实验Ⅳ中右边试管中CaO能够吸收左边试管中的水汽并与水反应.因此左边试管中饱和硫酸铜溶液中有蓝色晶体析出.D项正确. 答案:CD
网址:http://m.1010jiajiao.com/timu3_id_84842[举报]
某研究性学习小组的同学对Cl2使有色物质褪色的机理进行了探究.甲同学设计了如图所示的实验装置并进行实验:
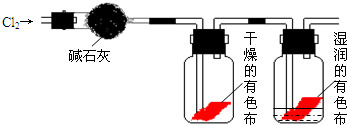
(1)甲同学实验后并没有得到预期的实验现象,请你帮助他分析实验失败的原因
(2)甲同学在实验失败后对设计的实验装置进行了改进,并重新进行了实验,结果得到了预期的实验现象.你认为他预期的实验现象是
(3)乙同学认为甲设计的实验装置即使改进后还缺少一部分.请你将乙认为缺少的部分在上图中的相应位置画出,并在添加的装置中标明需要放入的最合适的化学试剂的名称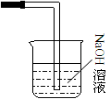
 .
.
(4)请你写出Cl2和“③”中“最合适的化学试剂”反应的离子方程式
查看习题详情和答案>>

(1)甲同学实验后并没有得到预期的实验现象,请你帮助他分析实验失败的原因
使用的干燥剂碱石灰将Cl2吸收
使用的干燥剂碱石灰将Cl2吸收
;(2)甲同学在实验失败后对设计的实验装置进行了改进,并重新进行了实验,结果得到了预期的实验现象.你认为他预期的实验现象是
干燥的有色布条不褪色,湿润的有色布条褪色
干燥的有色布条不褪色,湿润的有色布条褪色
,由此得出Cl2使有色物质褪色的机理是Cl2和水反应生成次氯酸,次氯酸具有漂白作用
Cl2和水反应生成次氯酸,次氯酸具有漂白作用
;(3)乙同学认为甲设计的实验装置即使改进后还缺少一部分.请你将乙认为缺少的部分在上图中的相应位置画出,并在添加的装置中标明需要放入的最合适的化学试剂的名称


(4)请你写出Cl2和“③”中“最合适的化学试剂”反应的离子方程式
Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
. 用98%的浓H2SO4(ρ=1.84g/cm3)配制 240mL0.5mol/L的稀H2SO4,请按要求填空:
用98%的浓H2SO4(ρ=1.84g/cm3)配制 240mL0.5mol/L的稀H2SO4,请按要求填空:(1)请写出该实验的实验步骤
①
计算
计算
,②量取
量取
,③溶解转移
溶解转移
,④洗涤转移
洗涤转移
,⑤定容摇匀
定容摇匀
.(2)所用浓H2SO4的物质的量浓度为
18.4mol/L
18.4mol/L
,配制时所需浓硫酸的体积为6.8
6.8
mL.(均保留一位小数)(3)实验中需要用到的定量仪器有(包括规格)
10mL量筒、250mL容量瓶
10mL量筒、250mL容量瓶
(4)若实验中出现下列现象对所配溶液的浓度有什么影响?(填“偏高”、“偏低”或“无影响”)
①浓硫酸溶解后未冷至室温即进行转移、定容.(
偏高
偏高
)②定容时俯视刻度线.(偏高
偏高
)(5)若定容时液面高于刻度线应采取的措施是
重新配制
重新配制
.(6)若实验操作全部无误,最后所得的溶液应存放在试剂瓶中,并贴上标签,请你帮助把标签上的内容写一下(如图).


某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入高锰酸钾溶液时,溶液褪色先慢后快,即反应速率由小变大.小组成员为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种,并为此设计实验进行探究验证.
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:….
【实验目的】探究草酸与高锰酸钾反应的速率变化“异常”原因;
【实验用品】仪器:试管、胶头滴管、量筒、药匙、玻璃棒等;
试剂:0.1mol/L H2C2O4溶液、0.05mol/L KMnO4(硫酸酸化)溶液等.
请你根据该兴趣小组的实验探究设计思路,补充完整所缺内容.
(1)草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为(已知:MnO4_还原产物是Mn2+) .
(2)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是 .
(3)猜想Ⅱ可能是 .要设计实验验证猜想Ⅱ,进行该实验还要补充一种试剂及一种仪器,分别是 .
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容.
查看习题详情和答案>>
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:….
【实验目的】探究草酸与高锰酸钾反应的速率变化“异常”原因;
【实验用品】仪器:试管、胶头滴管、量筒、药匙、玻璃棒等;
试剂:0.1mol/L H2C2O4溶液、0.05mol/L KMnO4(硫酸酸化)溶液等.
请你根据该兴趣小组的实验探究设计思路,补充完整所缺内容.
(1)草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为(已知:MnO4_还原产物是Mn2+)
(2)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是
(3)猜想Ⅱ可能是
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容.
| 试管A | 试管B | |
| 加入试剂 | ||
| (预期)实验现象 (褪色时间) |
||
| 结论 | 猜想Ⅱ正确 | |
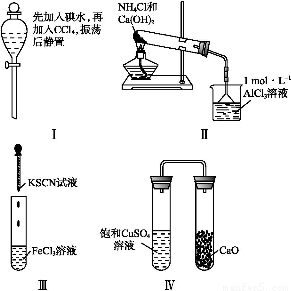
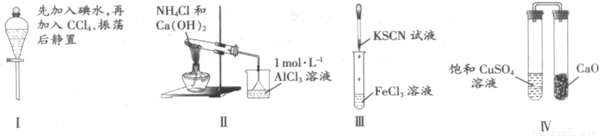 A 实验Ⅰ:液体分层,下层呈无色
A 实验Ⅰ:液体分层,下层呈无色